Structure de l'oxyde de Cerio (IV), propriétés, utilisations

- 2443
- 126
- Prof Noah Collet
Il Cério oxyde (IV) L'oxyde u zagique est un solide inorganique blanc pâle ou jaune qui est produit par l'oxydation du cérium (CE) par l'oxygène à son Valencia 4+. La formule chimique de l'oxyde zagique est PDG2 Et c'est l'oxyde le plus stable de la colline.
Cerio (CE) est un élément de la série Lanthanide, qui sont inclus dans le groupe du Lands-Ran. La source naturelle de cet oxyde est le minéral saltnasite. Dans le concentré commercial de ce minéral, le PDG2 Il peut être trouvé dans une proportion approximative jusqu'à 30% en poids.
 Un échantillon d'oxyde de Cerio (IV). Photo prise en août 2005 par l'utilisateur: Walkerma. Pd-self Source: Wikipedia Commons
Un échantillon d'oxyde de Cerio (IV). Photo prise en août 2005 par l'utilisateur: Walkerma. Pd-self Source: Wikipedia Commons Le PDG2 Il peut être facilement obtenu par chauffage dans l'air ou l'oxygène de la colline (III), CE (OH)3, ou tout sel de colline (iii), comme l'oxalate, le carbonate ou le nitrate.
Le PDG2 stoichiométrique peut être obtenue par réaction à haute température de l'oxyde de colline (III) avec de l'oxygène élémentaire. L'oxygène doit être excessivement et suffisamment de temps pour terminer la conversion des différentes phases non estrochiométriques qui se forment doivent être suffisantes pour terminer.
Ces phases comprennent des produits PDG de formule multicoloresX (où X varie entre 1,5 et 2.0). Ils sont également appelés PDG2-x, où x peut avoir une valeur allant jusqu'à 0,3. Le PDG2 C'est la forme EC la plus utilisée dans l'industrie. Il a une faible classification de toxicité, en particulier en raison de sa mauvaise solubilité dans l'eau.
 Échantillon de minéraux bastnasite. Rob Lavinsky, Irocks.com-cc-by-sa-3.0 [cc by-sa 3.0 (https: // CreativeCommons.Org / licences / by-sa / 3.0)] Source: Wikipedia Commons
Échantillon de minéraux bastnasite. Rob Lavinsky, Irocks.com-cc-by-sa-3.0 [cc by-sa 3.0 (https: // CreativeCommons.Org / licences / by-sa / 3.0)] Source: Wikipedia Commons [TOC]
Structure
Cério oxyde (IV) STOICHIOMETRIQUE cristallise dans le réseau cube de type fluorite (café2), avec 8 ions ou2- Dans une structure cubique coordonnée avec 4 ions CE4+.
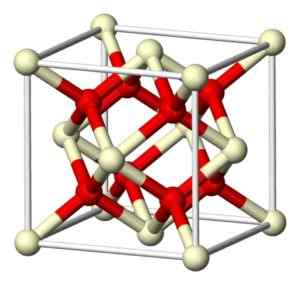 Structure cristalline de l'oxyde de colline (IV). Benjah-Bmm27 [Domaine public] Source: Wikipedia Commons
Structure cristalline de l'oxyde de colline (IV). Benjah-Bmm27 [Domaine public] Source: Wikipedia Commons Nomenclature
- Cério oxyde (IV).
- Oxyde zagique.
- Dioxyde de créo.
- Cèrie.
- Colline stoichiométrique: matériau entièrement formé par le PDG2.
- Oxyde de cério non éthique non éthique: matériau formé par des oxydes mixtes du PDG2 au PDG1.5
Propriétés
État physique
Solide jaune pâle. La couleur est sensible à la stoechiométrie et à la présence d'autres lanthanides. Les oxydes non stoichiométriques sont souvent bleus.
Dureté mohs
Environ 6-6.1.
Poids moléculaire
172.12 g / mol.
Point de fusion
2600 ºC approximativement.
Densité
7 132 g / cm3
Solubilité
Insoluble dans l'eau froide et chaude. Soluble dans l'acide sulfurique concentré concentré. Insoluble dans les acides dilués.
Indice de réfraction
2.2.
Autres propriétés
Le PDG2 C'est une substance inerte, il n'est pas attaqué ni par des acides forts ou des alcalis. Cependant, il peut être dissous par les acides en présence d'agents réducteurs, tels que le peroxyde d'hydrogène (H2SOIT2) ou étain (ii), entre autres, générant des solutions de Cerio (iii).
Peut vous servir: système hétérogènePrésente une stabilité thermique élevée. Ne subit pas de changements cristallographiques pendant les intervalles de chauffage habituels.
Son dérivé hydraté (PDG2.NH2O) est un précipité jaune et gélatine qui est obtenu lors du traitement des solutions de Cerio (IV) avec des bases.
Le PDG2 Il est mal absorbé par le tractus gastro-intestinal, il n'a donc aucun effet toxique.
Applications
- Dans l'industrie métallurgique
Le PDG2 Il est utilisé dans des électrodes de certaines technologies de soudage, telles que le soudage à l'arc au tungstène avec du gaz inerte.
L'oxyde est finement dispersé dans la matrice de tungstène. À basse tension ces particules de PDG2 donner une plus grande fiabilité que le tungstène uniquement.
- Dans l'industrie du verre
Polissage en verre
L'oxyde de Cerio est l'agent de polissage le plus efficace pour la plupart des compositions de verre commerciales. Le PDG2 a presque complètement remplacé d'autres oxydes de polissage, comme la foi2SOIT3, Silice et zro2, En raison de sa vitesse de polissage et de sa propreté plus élevées, qui augmentent en augmentant le degré de pureté de l'oxyde.
Les poulades commerciales pour le verre à base de poudres d'oxyde de cérium ont défini la taille des particules et la dispersibilité contrôlée dans les systèmes aqueux.
Le processus de polissage en verre nécessite de l'eau et ce qui est retiré ou une réforme est une couche de surface hydratée plus douce. L'agent de polissage doit avoir une dureté Mohs d'environ 6,5, près de la dureté de la plupart.
L'oxyde de Cerio dans l'eau contient le couple CE (IV) / EC (III) qui, avec leurs réactions de réduction d'oxyde peut fournir une assistance chimique pendant la rupture du réseau de silicate de verre.
Le PDG2 Avec un degré élevé de pureté, il est utilisé pour traiter les miroirs, les appareils télévisés, les lentilles ophtalmiques et le matériau optique de précision.
Décoloration du verre
Le PDG2 peut décolorer le verre soda-cal pour les bouteilles, les cruches et autres. Le CE (iv) oxyde les impuretés de la foi (ii), qui fournissent une couleur vert bleu, à la foi (iii) qui confère une couleur jaune 10 fois plus faible.
Verre résistant aux rayonnements
L'ajout de PDG à 1%2 Au verre supprime la décoloration ou l'assombrissement du verre causé par le bombardement des électrons à haute énergie dans le verre de télévision. La même chose se produit dans les fenêtres utilisées dans les cellules chaudes de l'industrie nucléaire, car elle supprime la décoloration induite par les rayons gamma.
On pense que le mécanisme de suppression dépend de la présence d'ions CE4+ et CE3+ Dans le réseau de verre.
Il peut vous servir: chimie nucléaire: histoire, domaine d'étude, zones, applicationsVerre photosensible
Certaines formulations de verre peuvent développer des images latentes qui peuvent ensuite être converties en structure ou couleur permanente.
Ce type de verre contient le PDG2 qui absorbe le rayonnement UV et libère des électrons dans la matrice de verre.
Grâce au traitement ultérieur, la croissance des cristaux d'autres composés dans le verre est générée, créant des modèles détaillés pour les utilisations électroniques ou décoratives.
- En émail
Pour son PDG de l'indice de réfraction élevé2 C'est un agent d'opacité dans les compositions d'émail utilisées comme revêtements protecteurs sur les métaux.
Sa stabilité thermique élevée et sa forme cristallographique unique tout au long de l'intervalle de température qui sont obtenues pendant le processus d'émail, ce qui le rend adéquat pour une utilisation dans les émails pour la porcelaine.
Dans cette application, le PDG2 Fournit la couverture blanche souhaitée pendant l'émail brûlé. C'est l'ingrédient qui fournit l'opacité.
- Dans Cirmonio Ceramics
La céramique de circonium est un isolant thermique et est utilisé dans des applications à haute température. Nécessite un additif pour avoir une résistance et une ténacité élevées. Ajout d'un PDG2 Un circonyde de circony.
Oxyde de zirch dopé au PDG2 Il est utilisé dans les revêtements pour agir comme barrière thermique sur les surfaces métalliques.
Par exemple, dans les parties des moteurs d'avion, ces revêtements protègent des températures élevées auxquelles les métaux seraient exposés.
 Moteur à réaction. Jeff Dahl, Traduction espagnole par Xavigivax [CC By-SA 4.0 (https: // CreativeCommons.Org / licences / by-sa / 4.0)] Source: Wikipedia Commons
Moteur à réaction. Jeff Dahl, Traduction espagnole par Xavigivax [CC By-SA 4.0 (https: // CreativeCommons.Org / licences / by-sa / 4.0)] Source: Wikipedia Commons - Dans les catalyseurs pour le contrôle des émissions de véhicules
Le PDG2 C'est un élément actif dans l'élimination des polluants des émissions de véhicules. Cela est en grande partie dû à sa capacité à stocker ou à libérer de l'oxygène en fonction des conditions qui l'entourent.
Le convertisseur catalytique des véhicules automobiles est situé entre le moteur et la sortie des gaz d'échappement. Il a un catalyseur qui doit oxyder les hydrocarbures non questionnos2, et réduire les oxydes d'azote, nonX, un2 je2.
 Convertisseur catalytique des gaz d'échappement du moteur à combustion interne d'un véhicule automobile. Ahanix1989 à l'anglais Wikipedia [Domaine public] Source: Wikipedia Commons
Convertisseur catalytique des gaz d'échappement du moteur à combustion interne d'un véhicule automobile. Ahanix1989 à l'anglais Wikipedia [Domaine public] Source: Wikipedia Commons En plus du platine et d'autres métaux catalytiques, la principale composante active de ces systèmes multifonctionnels est le PDG2.
Chaque convertisseur catalytique contient 50-100 g de PDG2 Finement divisé, qui remplit plusieurs fonctions. Les plus importants sont:
Il agit comme un stabilisateur de la haute surface d'alumine
L'alumine à surface élevée a tendance à Sinterar, perdant sa surface élevée pendant le fonctionnement à des températures élevées. Ceci est retardé par la présence du PDG2.
Peut vous servir: diméthylanylin: structure, propriétés, synthèse, utilisationsIl se comporte comme un libradeur de stockage d'oxygène
Pour sa capacité à former un PDG perchiométrique non-oriental2-x, L'oxyde de cérium (IV) fournit de l'oxygène élémentaire de sa propre structure pendant la période du pauvre cycle d'oxygène / riche en carburant.
Ainsi, l'oxydation des hydrocarbures non montés qui proviennent du moteur et de la conversion du CO peuvent continuer2, Même lorsque l'oxygène du gaz est insuffisant.
Ensuite, au cours de la période du cycle riche en oxygène, il reprend de l'oxygène et oxydé à nouveau, récupérant sa forme stoechiométrique du PDG2.
Autres
Il fonctionne comme une mauvaise capacité catalytique de la conduite dans la réduction des oxydes d'azote neX Azote et oxygène.
- Sur les réactions chimiques
Dans les processus de fissuration catalytique des raffineries, le PDG2 Il agit comme un oxydant catalytique qui aide à la conversion de SO2 À ainsi3 et favorise la formation de sulfate dans des pièges à processus spécifiques.
Le PDG2 Améliore l'activité du catalyseur basé sur l'oxyde de fer qui est utilisé pour obtenir l'étirement à partir de l'éthylbenzène. Cela est peut-être dû à l'interaction positive entre les couples d'oxyde de réduction (II) - Fe (III) et CE (III) - CE (IV).
- Dans les applications biologiques et biomédicales
Il a été constaté que les nanoparticules PDG2 Ils agissent en éliminant les radicaux libres, comme le superoxyde, l'hydrogène, l'hydroxyle et l'oxyde nitrique radical.
Ils peuvent protéger les tissus biologiques des dommages induits par les rayonnements, les dommages rétiniens induits par le laser, augmenter la gamme de vie des cellules photorécepteurs, réduire les lésions vertébrales, réduire l'inflammation chronique et favoriser l'angiogenèse ou la formation des vaisseaux sanguins.
De plus, certains nanofibres contenant des nanoparticules de PDG2 Ils se sont avérés toxiques contre les souches bactériennes, étant des candidats prometteurs à des applications bactéricides.
- Autres utilisations
Le PDG2 Il s'agit d'un matériau isolant électrique en raison de son excellente stabilité chimique, de son allocation relative élevée (il a une forte tendance à polariser avant l'application d'un champ électrique) et un réseau cristallin similaire au silicium.
A trouvé une application dans le condenseur et les couches d'amorti des matériaux de supraconducteur.
Il est également utilisé dans les capteurs de gaz, les matériaux pour les électrodes de pile à combustible à oxyde solide, les pompes à oxygène et les moniteurs d'oxygène.
Les références
- Coton, F. Albert et Wilkinson, Geoffrey. (1980). Chimie inorganique avancée. Quatrième édition. John Wiley & Sons.
- Danse, j.C.; Emeléus, h.J.; Sir Ronald Nyholm et Trotman-Deckenson, à.F. (1973). Chimie inorganique complète. Volume 4. Presse à pergamon.
- Kirk-othmer (1994). Encyclopédie de la technologie chimique. Volume 5. Quatrième édition. John Wiley & Sons.
- Encyclopédie de la chimie industrielle d'Ullmann. (1990). CINQUIÈME ÉDITION. Volume A6. VCH VERLAGSGELLSCHAFT MBH.
- Casals, Eudald et al. (2012). Analyse et risque de nanomatériaux dans les échantillons environnementaux et alimentaires. Dans la compréhension de la chimie analytique. Récupéré de ScienceDirect.com.
- MailAdil t. Sébastien. (2008). Aluminia, Titania, Ceria, Silicate, Tungstate et autres matériaux. Dans les matériaux diélectriques pour la communication sans fil. Récupéré de ScienceDirect.com.
- Afeesh Rajan Unnithan, et al. (2015). Échafaudages aux propriétés antibactériennes. Dans les applications de nanotechnologie pour l'ingénierie tissulaire. Récupéré de ScienceDirect.com.
- Gottardi V., et al. (1979). Polissage de la surface d'un verre étudié avec une technique nucléaire. Bulletin de la Spanish Ceramics and Glass Society, Vol. 18, non. 3. Récupéré des bulletins.Secv.est.
- « Structure de l'hydroxyde de cuivre (II), propriétés, nomenclature, utilisations
- Équation du directeur vectoriel de la ligne, exercices résolus »

