Structure de l'hydroxyde de cuivre (II), propriétés, nomenclature, utilisations

- 2828
- 623
- Adrien Remy
Il Hydroxyde de cuivre (II) o L'hydroxyde cuprique est un solide inorganique cristallin bleu verdâtre ou bleu dont la formule chimique est Cu (OH)2. Il est obtenu sous forme de précipité volumineux bleu en ajoutant un hydroxyde alcalin aux solutions cupriques (cela signifie qu'ils contiennent des ions Cu2+). C'est un composé instable.
Pour augmenter sa stabilité, il est préparé en présence d'ammoniac (NH3) ou phosphates.Si vous vous préparez en présence d'ammoniac, il y a un matériau avec une bonne stabilité et une grande taille de particules.
 Échantillon d'hydroxyde cuprique, Cu (OH)2. Samzane chez italien Wikipedia [Domaine public] Source: Wikipedia Commons
Échantillon d'hydroxyde cuprique, Cu (OH)2. Samzane chez italien Wikipedia [Domaine public] Source: Wikipedia Commons Lors de la préparation avec du phosphate de cuivre (II), Cu3(Po4)2, Une taille de particules plus fine et une surface plus grande sont obtenues. L'hydroxyde cuprique est largement utilisé comme fongicide et bactéricide dans l'agriculture et pour traiter le bois, prolongeant sa durée de vie utile.
Il est également utilisé comme complément de nourriture pour animaux. Il est utilisé comme matière première pour obtenir d'autres sels de cuivre (II) et en galvanoplastie pour couvrir les surfaces.
Des études sont en cours pour estimer leur potentiel pour lutter contre les infections bactériennes et fongiques dans l'être humain.
[TOC]
Structure
L'hydroxyde de cuivre (II) contient des ions de cuivre infinis (Cu2+) United pour les groupes hydroxyles (OH-).
Les chaînes sont tellement emballées que 2 atomes d'oxygène d'autres chaînes sont au-dessus et en dessous de chaque atome de cuivre, puis en adoptant une configuration octaédrique déformée, qui est courante dans la plupart des composés de cuivre (II).
Dans sa structure, quatre atomes d'oxygène sont à une distance de 1,93 A; Deux atomes d'oxygène sont de 2,63 A; Et la distance Cu-Cu est de 2,95 pour.
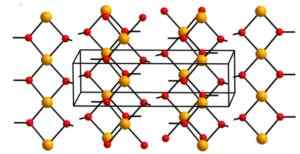 Structure cristalline de l'hydroxyde cuprique. Aleksandar Kondinski [CC BY-SA.0 (https: // CreativeCommons.Org / licences / by-sa / 4.0)]. Source: Wikipedia Commons
Structure cristalline de l'hydroxyde cuprique. Aleksandar Kondinski [CC BY-SA.0 (https: // CreativeCommons.Org / licences / by-sa / 4.0)]. Source: Wikipedia Commons Nomenclature
- Hydroxyde de cuivre (II).
- Hydroxyde de tasse.
- Dihydroxyde de cuivre.
Propriétés
État physique
Solide cristallin.
Poids moléculaire
99,58 g / mol.
Point de fusion
Il se décompose avant de fondre. Point de dégradation 229 ºC.
Peut vous servir: 25 exemples de solubilité dans la vie quotidienneDensité
3,37 g / cm3
Solubilité
Il est pratiquement insoluble dans l'eau: 2,9 microgrammes / L A 25 ºC. Rapidement soluble dans les acides, dans des solutions alcalines concentrées et de l'hydroxyde d'ammonium. Insoluble dans les solvants organiques. Dans l'eau chaude, il décompose la génération d'oxyde de cuivre (II), qui est plus stable.
Autres propriétés
Il est facilement soluble en acides forts et également dans des solutions concentrées alcalines d'hydroxydes, pour donner des anions bleu profond, probablement le type [Cun(OH)2n + 2]]2-.
Sa stabilité dépend de la méthode de préparation.
Il peut être décomposé en donnant un oxyde de cuivre (II) noir (CUO) s'il reste au repos quelques jours ou un chauffage bas.
En présence d'un excès d'alcali, il décompose plus de 50 ° C.
Applications
En agriculture
L'hydroxyde de cuivre (II) a une large application en tant que fongicide et antibactérienne dans les cultures agricoles. Voici quelques exemples:
- Il sert contre les taches bactériennes ( Erwinia) En laitue, en appliquant un traitement foliaire.
- Contre les taches bactériennes (de Xanthomonas Pruni) Dans les pêches, pour lesquelles un traitement latent et foliaire est appliqué.
- Il est utilisé contre la feuille et la tige des bleuets à travers des applications latentes.
- Contre la pourriture pendant le stockage des bleuets causés par Monilinia oxycocci, par application latente.
Pour l'application dans l'agriculture, l'hydroxyde de cuivre (II) est utilisé qui est préparé en présence de phosphates en raison de sa petite taille de particules.
 Culture de laitue. Source: Pixabay
Culture de laitue. Source: Pixabay Dans la préservation du bois
Le bois, en raison de la nature organique, est sensible à l'attaque des insectes et des micro-organismes. L'hydroxyde de cuivre (II) est utilisé comme biocide pour les champignons qui attaquent le bois.
Il est généralement utilisé à côté d'un composé d'ammonium quaternaire (NH4+). L'hydroxyde de cuivre agit comme un fongicide et le composé d'ammonium quaternaire fonctionne comme un insecticide.
De cette façon, le bois traité perd ou résiste aux conditions de service, atteignant le niveau de performance requis par l'utilisateur. Cependant, le bois traité avec ces composés a un haut niveau de cuivre et est très corrosif pour l'acier commun, donc un type d'acier inoxydable est nécessaire qui peut supporter le traitement du bois traité.
Peut vous servir: réaction réversible: caractéristiques et exemplesMalgré son utilité, l'hydroxyde de cuivre (II) est considéré comme un biocide légèrement dangereux.
Pour cette raison, il est à craindre qu'il soit libéré du bois traité dans l'environnement en quantités qui peuvent être nocives pour les micro-organismes naturellement présents dans les eaux (rivières, lacs, zones humides et mer) ou le sol.
Dans la fabrication de Rayón
Depuis le XIXe siècle, des solutions ammoniaciennes d'hydroxyde de cuivre (II) ont été utilisées pour dissoudre la cellulose. Ceci est l'une des premières étapes pour obtenir la fibre appelée Rayón à travers la technologie développée par Bemberg en Allemagne.
L'hydroxyde de cuivre (II) se dissout dans une solution d'ammoniac (NH3), formant un sel complexe.
De courtes fibres de coton raffinées sont ajoutées à la solution de cuivre ammoniacale contenant de l'hydroxyde de cuivre (II) sous forme de précipité solide.
Le coton cellulose forme un complexe avec l'hydroxyde de cuivre tétra-ammonium se dissolvant dans la solution.
Par la suite, cette solution est coagula tout en passant par un dispositif d'extrusion.
En raison de son coût élevé, cette technologie a déjà été surmontée par celle de Viscosa. La technologie de Bemberg est actuellement utilisée uniquement au Japon.
Dans l'industrie des aliments pour animaux
Il est utilisé comme traces dans l'alimentation animale, car c'est l'une des substances requises comme micronutriments pour la nutrition complète des animaux.
 Aliments concentrés pour le bétail. Thamizhpparithi maari [cc by-sa 3.0 (https: // CreativeCommons.Org / licences / by-sa / 3.0)]. Source: Wikipedia Commons
Aliments concentrés pour le bétail. Thamizhpparithi maari [cc by-sa 3.0 (https: // CreativeCommons.Org / licences / by-sa / 3.0)]. Source: Wikipedia Commons En effet, dans les êtres vivants supérieurs, le cuivre est un élément essentiel, requis pour l'activité d'une variété d'enzymes contenant du cuivre.
Par exemple, il est contenu dans l'enzyme qui participe à la production de collagène et à l'enzyme requise pour la synthèse de la mélanine, entre autres.
Peut vous servir: aminesIl s'agit d'un composé généralement reconnu comme une assurance lorsqu'il est ajouté à des niveaux conformes à une bonne pratique alimentaire.
 Vaches laiteuses. Source: Pixabay
Vaches laiteuses. Source: Pixabay Dans la fabrication d'autres composés de cuivre (II)
Précurseur actif dans la production des composés de cuivre suivants (II): cuivre (II), 2-otylhexanoate cuivre (II) et savons en cuivre et savons de cuivre. Dans ces cas, l'hydroxyde de cuivre (II) est utilisé qui est synthétisé en présence d'ammoniac.
Autres utilisations
Il est utilisé dans la stabilisation du nylon, dans les électrodes de batterie; comme fixateur de couleurs dans les opérations de teinture; comme pigment; dans les insecticides; dans le traitement du papier et la coloration; dans les catalyseurs, comme catalyseur dans la vulcanisation du caoutchouc polysulfure; comme un pigment anti-diffinant; et en électrolyse, en galvanoplastie.
Futures applications médicales
L'hydroxyde de cuivre (II) fait partie des composés en cuivre qui sont étudiés sous forme de nanoparticules pour l'élimination des bactéries telles que ET. coli, K. pneumoniae, p. Aeruginosa, Salmonella spp., entre autres, les causes des maladies en être humain.
Il a également été constaté que les nanoparticules de cuivre peuvent être efficaces contre Candida albicans, Un champignon qui est une cause commune des pathologies humaines.
Cela indique que la nanotechnologie en cuivre peut jouer un rôle important contre les bactéries et les champignons provoquant des infections humaines, et l'hydroxyde de cuivre (II) pourrait être très utile dans ces domaines.
Les références
- Coton, F. Albert et Wilkinson, Geoffrey. (1980). Chimie inorganique avancée. Quatrième édition. John Wiley & Sons.
- Kirk-othmer (1994). Encyclopédie de la technologie chimique. Volume 7. Quatrième édition. John Wiley & Sons.
- Encyclopédie de la chimie industrielle d'Ullmann. (1990). CINQUIÈME ÉDITION. Volume A7. VCH VERLAGSGELLSCHAFT MBH.
- Danse, j.C.; Emeléus, h.J.; Sir Ronald Nyholm et Trotman-Deckenson, à.F. (1973). Chimie inorganique complète. Volume 3. Presse à pergamon.
- Bibliothèque nationale de médecine. (2019). Cuivre (ii) hydroxyde. Récupéré de: pubchem.NCBI.NLM.NIH.Gouvernement
- Schiopu, n. et tiruta-brana, l. (2012). Conservateurs du bois. Dans la toxicité des matériaux de polissage. Chapitre 6. Récupéré de ScienceDirect.com.
- Mordorski, B. et Friedman, à. (2017). Nanoparticules de métal pour une infection microbienne. Dans les nanomatériaux fonctionnalisés pour la gestion de l'infection microbienne. Chapitre 4. Récupéré de ScienceDirect.com.
- Takashi Tsurumi. (1994). Solution tournante. Dans la technologie de rotation des fibres avancées. chapitre 3. Récupéré de ScienceDirect.com.
- « Fondation histochimique, traitement, coloration
- Structure de l'oxyde de Cerio (IV), propriétés, utilisations »

