Tripoliphosphate de sodium (NA5P3O10) Structure, propriétés, utilisations, impact
- 602
- 112
- Eva Henry
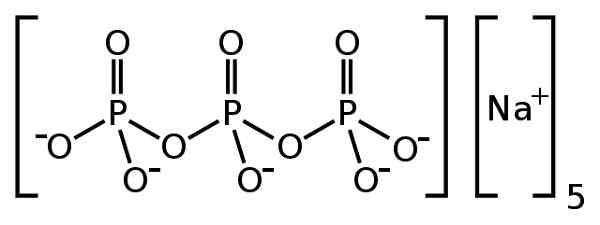
Il tripolyphosphate de sodium C'est un composé inorganique formé de cinq ions de sodium+ et un tripolifosphate p ion p3SOITdix5-. Sa formule chimique est na5P3SOITdix. L'ion tripolifosphate contient trois unités de phosphate liées les unes aux autres et est ce qu'on appelle un phosphate condensé.
L'anion tripolifosphate p3SOITdix5- Il a la capacité d'attraper des ions comme le calcium CA2+ Et magnésio mg2+, Par conséquent, Tripoliff de sodium.
 Sodium na tripolyphosphate5P3SOITdix. BenRR101 [domaine public]. Source: Wikimedia Commons.
Sodium na tripolyphosphate5P3SOITdix. BenRR101 [domaine public]. Source: Wikimedia Commons. Le tripoliphosphate de sodium est également utilisé comme source de phosphore dans l'alimentation des animaux de pâturage et dans le traitement de certaines maladies d'autres types d'animaux. Il sert également à épaissir et à donner de la texture à certains aliments transformés tels que les crèmes, les pudies et les fromages.
Dans l'industrie agricole, il est utilisé dans les engrais dans les granules pour les empêcher de se coller et peut rester lâche.
Bien qu'il y ait eu des discussions sur l'impact environnemental du tripoliphosphate de sodium qui est ajouté aux détergents, on estime actuellement qu'il ne contribue pas sensiblement à endommager l'environnement, au moins par le biais de détergents.
[TOC]
Structure chimique
Le tripoliphosphate de sodium fait partie des phosphates condensés So appelés car ce sont plusieurs unités de phosphate ensemble. Dans ce cas, l'ion tripolifosphate est un phosphate de condensat linéaire car il a une structure de type de chaîne linéaire, avec des liaisons phosphore-oxygène-phosphore (P-O-P) (P-O-P).
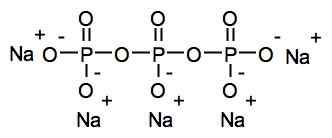 Structure chimique du tripoliphosphate de sodium. Roland.Chem [gfdl (http: // www.gnou.Org / copyleft / fdl.html)]. Source: Wikimedia Commons.
Structure chimique du tripoliphosphate de sodium. Roland.Chem [gfdl (http: // www.gnou.Org / copyleft / fdl.html)]. Source: Wikimedia Commons. Nomenclature
- Tripolyphosphate de sodium
- Triphosphate de sodium
- Pentasodio triffosphate
- STPP (acronyme anglais Tripolyphate de sodium)
Propriétés
État physique
Solide blanc cristallin.
Poids moléculaire
367,86 g / mol.
Point de fusion
622 ° C.
Densité
2,52 g / cm3
Solubilité
Soluble d'eau: 20 g / 100 ml à 25 ° C et 86,5 g / 100 ml à 100 ° C.
Peut vous servir: quelles sont les fonctions chimiques inorganiques?pH
Une solution à 1% de tripolifosphate de sodium a un pH de 9,7-9,8.
Propriétés chimiques
C'est un agent d'enlèvement d'Ion, c'est-à-dire qu'il peut attraper les ions et rester avec eux. Forme complexe avec de nombreux métaux.
Si une solution de tripolifosphate de sodium est chauffée pendant longtemps, elle a tendance à devenir orthophosphate de sodium3Pote4.
Autres propriétés
C'est légèrement hygroscopique. Façonner des hydrates stables, c'est-à-dire des composés qui ont des molécules d'eau (sans avoir réagi avec ceci) de formule na5P3SOITdix.NH2Ou où n peut valoir entre 1 et 6.
Selon certaines sources, une quantité de 20 mg de tripolifosphate de sodium dans un litre d'eau n'affecte pas l'odeur, la saveur ou le pH de ladite eau.
Obtention
Le tripoliphosphate de sodium est préparé par déshydratant des orthophosphates (comme le phosphate monosodique NAH2Pote4 Et dis-phfosphat na2HPO4) à des températures très élevées (300-1200 ° C):
Non2Pote4 + 2 Na2HPO4 → Na5P3SOITdix + 2 h2SOIT
Il peut également être obtenu par calcination contrôlée (cela signifie un chauffage à très haute température) d'orthophosphate de sodium Na3Pote4 Avec carbonate de sodium na2CO3 et l'acide phosphorique H3Pote4.
Applications
Dans les détergents
Le tripoliphosphate de sodium a la propriété de former des composés avec certains ions, les conservant. Il a également des propriétés de dispersion des particules sales et les maintient en suspension.
Pour cette raison, il est largement utilisé dans les formulations de détergent pour attraper et immobiliser les ions calcium CA2+ et magnésio mg2+ de l'eau (des eaux durs si appelées) et pour garder le sale dans l'eau suspendue.
Les ions susmentionnés interfèrent avec l'action de nettoyage. En les attrapant, le tripolifosphate empêche ces ions de précipiter avec l'agent de nettoyage ou de coller du sale dans le tissu empêchant la tache de décoller de ce.
Il est dit dans ce cas que le tripoliphosphate de sodium "adoucit" l'eau. Par conséquent, il est utilisé dans les détergents pour les vêtements et les détergents de lave-vaisselle automatique.
Peut vous servir: Syringe PascalPuisqu'il forme des hydrates stables, les détergents qui le possèdent dans leur formulation peuvent être séchés instantanément par pulvérisation (rosée très fine) formant des poudres sèches.
 Poussière de détergent qui peut contenir du tripoliphosphate de sodium. Auteur: Frank Habel. Source: Pixabay.
Poussière de détergent qui peut contenir du tripoliphosphate de sodium. Auteur: Frank Habel. Source: Pixabay. Pour un usage vétérinaire
Le tripoliphosphate de sodium est utilisé comme supplément dans les solutions liquides comme source de phosphore pour les bovins.
 L'alimentation sous vide peut être complétée par le tripolifosphate de sodium comme source de phosphore. Auteur: Herney Gómez. Source: Pixabay.
L'alimentation sous vide peut être complétée par le tripolifosphate de sodium comme source de phosphore. Auteur: Herney Gómez. Source: Pixabay. Il sert également à prévenir les calculs rénaux chez les chats, pour lesquels ces animaux sont fournis par voie orale. Cependant, l'attention doit être accordée à la dose car elle peut provoquer la diarrhée.
 Le tripoliphosphate de sodium à très faibles doses peut empêcher les reins chez les chats. Auteur: Scott Payne. Source: Pixabay.
Le tripoliphosphate de sodium à très faibles doses peut empêcher les reins chez les chats. Auteur: Scott Payne. Source: Pixabay. En médecine
Le tripoliphosphate de sodium a été utilisé dans la préparation de nanoparticules pour un transport adéquat et la libération de médicaments de chimiothérapie contre le cancer. Il a également été utilisé dans des nanoparticules pour le traitement des infections aux champignons dans les poumons.
 Le tripolyphosphate est testé dans la préparation des nanopharmacaux pour guérir les infections fongiques dans les poumons. Auteur: Vecteurs d'OpenClipart. Source: Pixabay.
Le tripolyphosphate est testé dans la préparation des nanopharmacaux pour guérir les infections fongiques dans les poumons. Auteur: Vecteurs d'OpenClipart. Source: Pixabay. Dans l'industrie alimentaire
Il est utilisé dans les produits laitiers tels que les podées, la crème fouettée, la crème sure et le fromage.
 Le crotteur aigre peut contenir un tripoliliff de sodium pour améliorer sa texture. Auteur: welikodub. Source: Pixabay.
Le crotteur aigre peut contenir un tripoliliff de sodium pour améliorer sa texture. Auteur: welikodub. Source: Pixabay. Dans d'autres aliments, il est utilisé comme kidnappeur d'ions, pour donner de la texture, comme épaississant et comme conservateur.
Autres utilisations
- Comme stabilisateur de peroxydes
- Dans les liquides de forage à huile, il fonctionne comme un émulsifiant et un dispersant pour contrôler la viscosité de la boue.
Peut vous servir: métaux ferreux- Dans l'agriculture, il est utilisé comme agent anti-pecling de certains engrais ou produits agricoles, cela signifie qu'ils les empêchent de se conformer les uns aux autres et l'engrais peut être facilement distribué. Il est également utilisé dans les formules de pesticides appliquées aux cultures croissantes.
 Usine d'engrais. Parfois Tripoliff de sodium de sodium. Van Twin [CC BY-SA 3.0 (https: // CreativeCommons.Org / licences / by-sa / 3.0)]. Source: Wikimedia Commons.
Usine d'engrais. Parfois Tripoliff de sodium de sodium. Van Twin [CC BY-SA 3.0 (https: // CreativeCommons.Org / licences / by-sa / 3.0)]. Source: Wikimedia Commons. Impact environnemental
L'utilisation de produits avec des phosphates a été identifiée comme l'un des contributeurs de l'eutrophisation des eaux sur la planète.
L'eutrophisation est la croissance exagérée et accélérée des algues végétales aquatiques et des espèces qui conduisent à une forte diminution de l'oxygène disponible dans l'eau, conduisant à la destruction de l'écosystème affecté (décès de la plupart des espèces animales).
 L'eutrofication est la croissance exagérée des algues dans un lac, une rivière ou une mer. F. Lamio (propre travail) [CC BY-SA 2.5 (https: // CreativeCommons.Org / licences / by-sa / 2.5)]. Source: Wikimedia Commons.
L'eutrofication est la croissance exagérée des algues dans un lac, une rivière ou une mer. F. Lamio (propre travail) [CC BY-SA 2.5 (https: // CreativeCommons.Org / licences / by-sa / 2.5)]. Source: Wikimedia Commons. Dans les années 1980, la controverse est survenue que l'utilisation du tripoliphosphate de sodium dans les détergents contribuait à l'eutrophisation.
De nos jours, il est connu que la limitation de l'utilisation de détergents avec un tripoliff de sodium.
En fait, il existe des pays qui considèrent le tripoliphosphate de sodium comme une composante respectueuse des détergents et promouvoir leur utilisation.
Des risques
Le tripoliphosphate de sodium est irritant la peau et les yeux. Le contact visuel peut endommager ces. Un contact de peau prolongé peut produire une dermatite.
S'il est ingéré en grande quantité, il peut provoquer des nausées, des vomissements et de la diarrhée, générant également une grave réduction de l'ion calcium dans le sang. Chez les animaux, il a provoqué une diminution du calcium des os.
Il est considéré comme un composé sûr chaque fois que les normes de fabrication du produit dans lesquelles il sont utilisées sont suivies.
Les références
- Liu, et. Et Chen, J. (2014). Cycle de phosphore. Module de référence dans les systèmes terrestres et les sciences de l'environnement. Encyclopédie de l'écologie (deuxième édition). Vol. 4, 2014, pp.181-191. Récupéré de ScienceDirect.com
- OU.S. Bibliothèque nationale de médecine. (2019). Tripolyphate de sodium. Centre national d'information sur la biotechnologie. Récupéré de pubchem.NCBI.NLM.NIH.Gouvernement.
- Mukherjee, b. et al. (2017). Administration pulmonaire de nanocarriers de médicaments biodégradables pour un traitement plus efficace des infections fongiques dans les poumons: idées basées sur les résultats récents. Dans des systèmes multifonctionnels pour la livraison combinée, la biodétection et le diagnostic. Récupéré de ScienceDirect.com.
- Kirk-othmer. (1991). Encyclopédie de la technologie chimique. 4e New York, John Wiley et Sons.
- Burckett St. Laurent, J. et al. (2007). Nettoyage des textiles à linge. Dans Handbook for Cleaning / Decontamination of Surfaces. Récupéré de ScienceDirect.com.
- Budavari, s. (Éditeur). (mille neuf cent quatre vingt seize). L'indice Merck. NJ: Merck and Co., Inc.
- Salahuddin, n. et Galal, à. (2017). Amélioration de l'administration de médicaments à la chimiothérapie par des outils de nanoprécision. En nanructures pour la thérapie contre le cancer. Récupéré de ScienceDirect.com.
- « Structure d'oxalate de sodium (Na2C2O4), propriétés, utilisations, risques
- Propriétés, usages, structures, risques, des usages, des structures, des risques, »

