Modèle atomique Heisenberg
- 1826
- 328
- Prof Noah Collet
Qu'est-ce que le modèle atomique de Heisenberg?
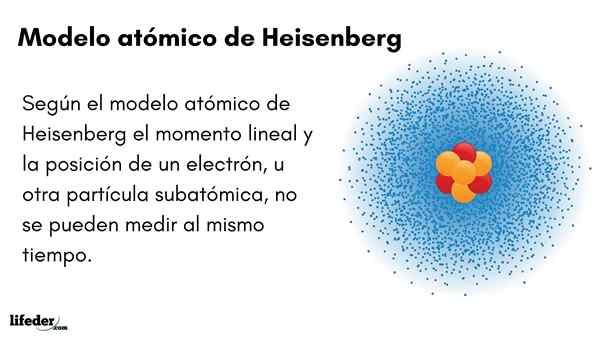
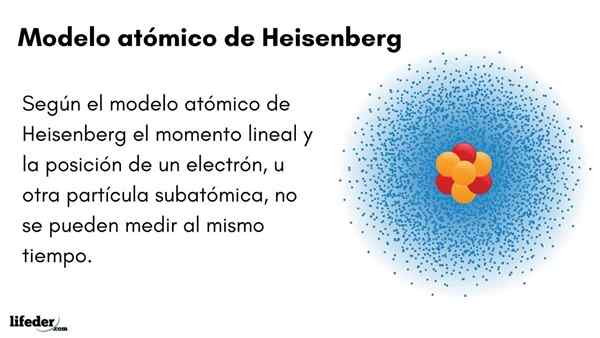
Il Modèle atomique Heisenberg (1927) introduit le principe d'incertitude des orbitales électroniques entourant le noyau atomique. Le physicien allemand exceptionnel a établi les fondements de la mécanique quantique pour estimer le comportement des particules subatomiques qui composent un atome.
Le principe d'incertitude de Werner Heisenberg indique qu'il n'est pas possible de savoir avec certitude la position linéaire d'un électron en même temps. Le même principe s'applique aux variables de temps et d'énergie; Autrement dit, si nous avons une indication sur la position de l'électron, nous ignorerons le moment linéaire de l'électron, et vice versa.
Bref, il n'est pas possible de prédire simultanément la valeur des deux variables. Ce qui précède n'implique pas que l'une des amplitudes mentionnées précédemment ne peut être connue avec précision. Chaque fois que c'est séparément, il n'y a aucun obstacle à l'obtention de la valeur d'intérêt.
Cependant, l'incertitude a lieu lorsqu'il s'agit de connaître simultanément deux amplitudes conjuguées, comme c'est le cas avec la position et le moment linéaires.
Ce principe survient en raison d'un raisonnement strictement théorique, comme la seule explication viable pour donner une raison sur les observations scientifiques.
Caractéristiques du modèle atomique Heisenberg
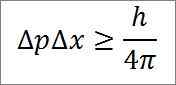 Werner Heisenberg
Werner Heisenberg En mars 1927, Heisenberg a publié son travail Sur le contenu perceptuel des cinématiques et de la mécanique quantique, où il a détaillé le principe de l'incertitude ou de l'indétermination.
Ce principe, fondamental dans le modèle atomique proposé par Heisenberg, est caractérisé par les éléments suivants:
- Le principe de l'incertitude survient comme une explication qui complète les nouvelles théories atomiques sur le comportement des électrons. Malgré l'utilisation d'instruments de mesure avec une haute précision et une sensibilité, l'indétermination est toujours présente dans tout essai expérimental.
- En raison du principe de l'incertitude, lors de l'analyse de deux variables connexes, si vous avez une connaissance précise de l'une d'entre elles, alors l'indétermination concernant la valeur de l'autre variable augmentera.
- Le moment linéaire et la position d'un électron, ou d'une autre particule subatomique, ne peuvent pas être mesurés en même temps.
- La relation entre les deux variables est donnée par une inégalité. Selon Heisenberg, le produit des variations du moment linéaire -3. 4 Jules x secondes) et 4π, comme détaillé dans l'expression mathématique suivante:
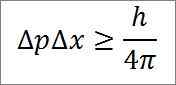
La légende correspondant à cette expression est la suivante:
∆p: indétermination du moment linéaire.
∆x: indétermination de la position.
H: constante de la planche.
π: Numéro PI 3.14.
- Compte tenu de ce qui précède, le produit des incertitudes a comme arrêt inférieur la relation h / 4π, qui est une valeur constante. Par conséquent, si l'une des amplitudes tend à zéro, l'autre doit augmenter dans la même proportion.
- Cette relation est valable pour toutes les paires d'amplitudes canoniques conjuguées. Par exemple: le principe d'incertitude de Heisenberg est parfaitement applicable au duo énergétique, comme détaillé ci-dessous:
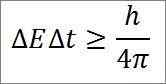
Dans cette expression:
∆E: Indétermination de l'énergie.
∆t: indétermination du temps.
H: constante de la planche.
π: Numéro PI 3.14.
- À partir de ce modèle, il s'ensuit que le déterminisme causal absolu dans les variables canoniques conjugués est impossible, car pour établir cette relation, la connaissance des valeurs initiales des variables d'étude doit être établie.
- Par conséquent, le modèle Heisenberg est basé sur des formulations probabilistes, en raison de l'aléatoire qui existe entre les variables aux niveaux subatomiques.
Tests expérimentaux
Le principe de l'incertitude de Heisenberg survient comme la seule explication possible aux tests expérimentaux qui ont eu lieu au cours des trois premières décennies du 21e siècle.
Avant que Heisenberg n'énonce le principe de l'incertitude, les préceptes en vigue.
Cela signifiait qu'ils étaient traités comme s'ils étaient de la physique classique; c'est-à-dire qu'une valeur initiale a été mesurée et la valeur finale a été estimée en fonction de la procédure pré-établie.
Peut vous servir: magnitude vectorielleCe qui précède signifiait définir un système de référence pour les mesures, l'instrument de mesure et la forme d'utilisation dudit instrument, selon la méthode scientifique.
Selon cela, les variables décrites par les particules subatomiques devaient se comporter de manière déterministe. C'est-à-dire que son comportement devrait être prédit exact et précisément.
Cependant, chaque fois qu'un essai de cette nature était effectué, il était impossible d'obtenir dans la mesure la valeur estimée théoriquement.
Les mesures ont été déformées en raison des conditions naturelles de l'expérience, et le résultat obtenu n'était pas utile pour enrichir la théorie atomique.
Exemple
Par exemple: s'il s'agit de mesurer la vitesse et la position d'un électron, l'assemblage de l'expérience doit contempler le choc d'un photon de lumière avec l'électron.
Cette collision induit une variation de la vitesse et de la position intrinsèques de l'électron, de sorte que l'objet de la mesure est modifié par des conditions expérimentales.
Par conséquent, le chercheur encourage l'occurrence d'une erreur expérimentale inévitable, malgré la précision et la précision des instruments utilisés.
Mécanique quantique autre que la mécanique classique
En plus de ce qui précède, le principe de l'indétermination de Heisenberg indique que, par définition, la mécanique quantique fonctionne différemment en ce qui concerne la mécanique classique.
Par conséquent, on suppose que la connaissance précise des mesures subatomiques est limitée par la ligne mince qui sépare la mécanique classique et quantique.
Limitations du modèle Heisenberg
Malgré l'explication de l'indétermination des particules subatomiques et assis aux différences entre la mécanique classique et quantique, le modèle atomique de Heisenberg n'établit pas d'équation unique pour expliquer le hasard de ce type de phénomènes.
Peut vous servir: énergie gravitationnelle: formules, caractéristiques, applications, exercicesDe plus, le fait que la relation soit établie par une inégalité implique que la gamme de possibilités pour le produit de deux variables canoniques conjuguées est indéterminée. Par conséquent, l'incertitude inhérente aux processus subatomiques est importante.
Articles d'intérêt
Modèle atomique Schrödinger.
Modèle atomique broglie.
Modèle atomique de Chadwick.
Modèle atomique perrin.
Modèle atomique Thomson.
Modèle atomique de Dalton.
Modèle atomique de Dirac Jordan.
Modèle atomique démocrite.
Modèle atomique de leucipo.
Modèle atomique bohr.
Modèle atomique Sommerfeld.
Modèle atomique actuel.
Les références
- Beyler, R. (1998). Werner Heisenberg. Encyclopædia Britannica, Inc. Récupéré de: Britannica.com
- Le principe de l'incertitude de Heisenberg (S.F.). Récupéré de: Hiru.EUS
- Garcia, J. (2012). Principe d'incertitude de Heisenberg. Récupéré de: Hiberus.com
- Modèles atomiques (s.F.). Université nationale autonome du Mexique. Mexico, Mexique. Récupéré de: Advisory.Cuautitlan2.Unam.mx
- Werner Heisenberg (S.F.).Récupéré de: l'histoire de l'atome.Wikispaces.com
- Wikipedia, Free Encyclopedia (2018). Planche à planche. Récupéré de: est.Wikipédia.org
- Wikipedia, Free Encyclopedia (2018). Relation de l'indétermination de Heisenberg. Récupéré de: est.Wikipédia.org

