TRYPANOSOMA CRUZI Caractéristiques, cycle de vie, maladies, symptômes
- 1593
- 381
- Raphaël Meyer
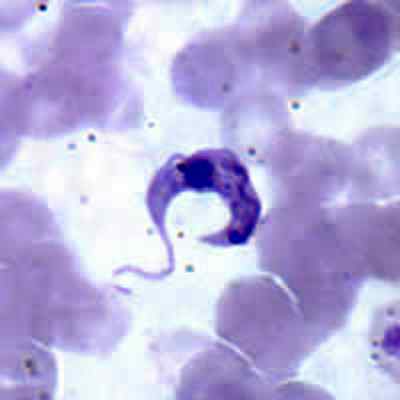
Trypanosoma cruzi Il s'agit d'un Euglénozoo (Phylum Euglenoozoa) de l'ordre de Kinetoplastida qui se caractérise par un parasite obligatoire de l'être humain et d'autres vertébrés. Il présente un fléau et une mitochondrie simple, dans laquelle se trouve le cinénasse, un organite spécialisé qui contient environ 25% de l'ADN de l'organisme.
Le cycle de vie de ce flagellate est compliqué, avec plus d'un hôte et plusieurs formes corporelles, qui sont identifiées en fonction de la position du cinétoplaste par rapport au noyau et avec le niveau de développement du fléau. Les formes corporelles reçoivent les noms de Tripomastigota, Epimastigota, Amastigota et Promastigota.
 Trypanosoma cruzi.Pris et édité à partir de: CDC [domaine public].
Trypanosoma cruzi.Pris et édité à partir de: CDC [domaine public]. Trypanosoma cruzi Il s'agit de l'agent causal de la maladie de Chagas, également connu sous le nom de tripanosomiase américaine ou de Mal de Chagas-Mazza, qui est transmis par les insectes de triathomin (Chipos). Il existe plus de 130 espèces d'insectes capables de transmettre le parasite et plusieurs espèces de mammifères qui servent d'hôtes.
Le mal de Chagas a une phase initiale asymptomatique, mais les symptômes apparaissent plus tard et peuvent se produire sous différentes formes, comme la fièvre, l'anorexie, la myocardite, la perte de poids, la myocardiopathie, la démence et même la mort de ne pas être traitée. Le traitement comprend le nifurtimox et le benzonidazole, qui ont plusieurs effets collatéraux.
[TOC]
Caractéristiques générales
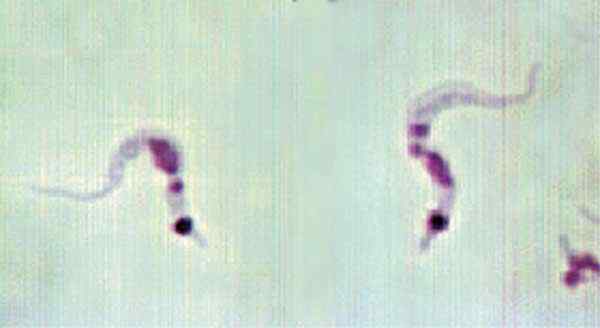 Trypanosoma Cruzi, Wikimedia Commons, Domaine public
Trypanosoma Cruzi, Wikimedia Commons, Domaine public Trypanosoma cruzi Il s'agit d'un parasite forcé de mammifères forcé de mammifères, dont l'homme, qui utilise les insectes comme hôtes intermédiaires, principalement ceux du groupe de triathomin.
Sa reproduction est asexuée par la fission et son cycle de vie présente plusieurs formes corporelles, il y a aussi le polymorphisme dans la phase Tripomastigota.
Trypanosoma cruzi Il ne peut pas être transmis par un contact occasionnel entre les hôtes finaux, mais par les transfusions et les transplantations d'organes, également par la consommation d'organismes contaminés, ainsi que par la mère du fœtus par le placenta et rarement par le lait maternel.
Le cinétoplaste de T. Cruzi Il est situé dans une expansion capsulaire des mitochondries, qui présente des crêtes, sauf dans la phase Tripomastigota, où elle est limitée à un petit canal dépourvu de crêtes.
La taille du cinétoplaste varie dans les différentes phases du parasite et est une structure discoïdale qui présente trois spirales de fibrill ADN, circulaire et a également environ 25 000 mini-culiraux dont la fonction est encore inconnue.
Cette espèce présente une membrane avec huit glycoprotéines superficielles dans lesquelles ils ont un cytosquelette organisé avec des microtubules qui participent à plusieurs fonctions, notamment la différenciation et la mobilité. Il participe également au processus de migration des tissus.
Peut vous servir: Pythium: caractéristiques, espèces, reproduction, nutritionMorphologie
La forme du corps de Trypanosoma cruzi Il changera tout au long de son cycle de vie, en distinguant chacun d'eux, principalement par la position relative du cinétoplaste par rapport au noyau, pour le degré de développement ou d'urgence du fléau et par la présence ou l'absence de membrane ondulée.
Tripomastigota
Il présente essentiellement une forme allongée, avec quelques variations, par exemple dans la largeur, apparemment corrélées avec ses caractéristiques biologiques. Le cinétoplaste est situé à l'arrière de l'animal, c'est-à-dire après le noyau.
Le fléau émerge du sac flagellaire, situé près du cinétoplaste et se replie vers la partie antérieure du corps, formant une membrane ondulée le long du parasite et émergeant librement à sa fin la plus distale. Dans l'être humain, il a une longueur de 20 μm de long par 1 μm de large et une forme qui peut ressembler à un C ou S.
Cette forme ne se reproduit pas, mais elle constitue la forme infectieuse. Il est situé extracellulaire dans le sang hôte.
Épimastigota
Dans cette phase, le cinéétoplaste est auparavant situé au noyau, au milieu de l'organisme. Il a une forme allongée, le fléau émergeant devant le noyau et formant une membrane ondulée de plus petite taille que celle trouvée sous la forme précédente.
Promastigota
À Cinetoplasto et au Détail sont situés dans la partie antérieure du parasite, et ce dernier émerge libre, sans développer une membrane ondulée.
Amastigota
Cette étape a une forme sphérique ou ovala, avec une taille approximative de 2 à 5 μm de diamètre. Le cinétoplaste apparaît comme une masse sombre près du noyau et le fléau est discret.
Cycle de vie de Trypanosoma cruzi
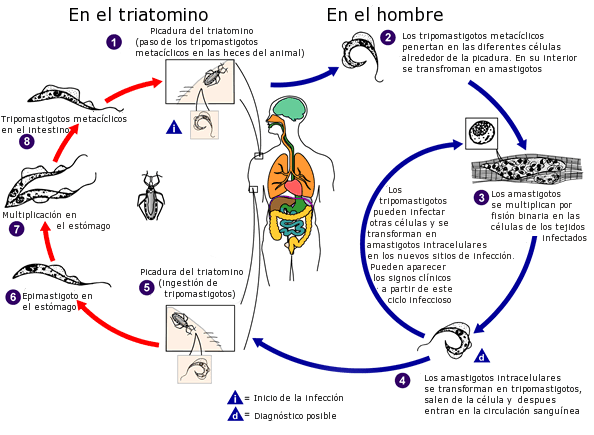 Cycle de vie de Trypanosoma Cruzi. Basquetteur [domaine public]
Cycle de vie de Trypanosoma Cruzi. Basquetteur [domaine public] Dans l'être humain
Le cycle de vie de Trypanosoma cruzi Il commence lorsque l'insecte vecteur pica à l'être humain, ou à tout autre mammifère et déféate par la suite. Le parasite a été déposé avec les selles sous la forme d'un trimotif métacyclique. Cela peut pénétrer le nouvel hôte à travers la plaie ou traverser les muqueuses à l'aide du fléau.
Il peut également pénétrer les rayures et les blessures que l'hôte se produit lors de la grattement. La surface cellulaire de l'hôte contient des macromolécules, y compris la laminine, la fibronectine et le sulfate d'héparine, qui sont essentiels pour permettre l'adhésion du parasite et pour le processus d'invasion cellulaire.
Lorsque le parasite pénètre les cellules hôtes, il subit une réduction du fléau et se transforme en amastigota. À cet endroit, la reproduction asexuée commence à travers la fission binaire, un processus similaire à celui qui se produit dans les bactéries.
Il peut vous servir: Agaricus campestris: caractéristiques, habitat, reproduction, nutritionAprès plusieurs reproductions, beaucoup d'amastigotes sont originaires, qui forment un pseudoquiste, par la suite les amastigotes sont à nouveau transformés en trimastigotas et la lyse cellulaire se produit.
Les trimastigotas qui ont été libérés de cette cellule pénètrent dans d'autres nouvelles cellules qui les infectent et répétent le cycle de reproduction.
Dans l'insecte
Lorsqu'un insecte vectoriel, qui est généralement un insecte de triathomine, ingère le sang d'un être humain, ou tout autre mammifère infecté, certains trimastigotas sont également ingérés.
Lorsque les parasites atteignent l'intestin de l'insecte, ils se transforment en épimastigotas, qui peuvent être reproduits par la mitose, constituant la deuxième phase de reproduction. Après 15 jours et un mois, les parasites migrent vers la ligne droite de l'insecte et se transforment en trimastigotas métacycliques.
Plus tard, lorsque l'insecte se nourrira à nouveau et s'en remet, les tripomastigotas seront déposés avec les excréments, et le cycle recommencera.
Maladies
Trypanosoma cruzi C'est l'agent causal du mal de Chagas, également appelé Trianosomiase américaine ou mal de Chagas-Mazza, qui est transmis par des insectes de triathomin, connus dans certains endroits tels que Chipos.
Cette maladie affecte plusieurs espèces de mammifères, en plus de l'homme, y compris les espèces sauvages et domestiques. Il ne peut pas être transmis par contact direct entre les mammifères, mais par la consommation d'animaux malades, d'insectes vectoriels ou de selles. Il peut également être acquis par transfusion et transplantation.
La maladie affecte principalement les personnes qui n'ont pas de logement adéquate et ont trois phases: aiguë, indéterminée et chronique. Aucun traitement approprié ne peut devenir mortel.
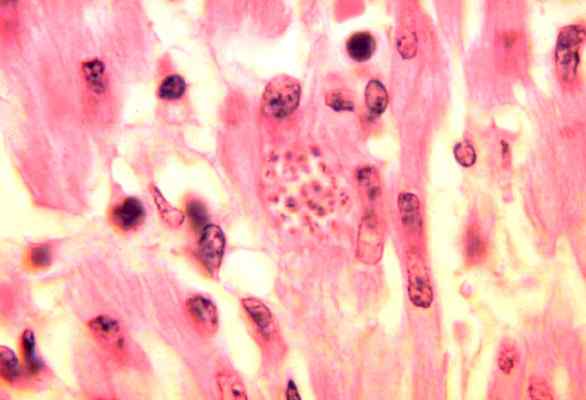 Trypanosoma cruzi dans mono coeur. Pris et édité à partir de: Crédit photo: Provideurs de contenu (s): CDC / DR. L.L. Moore, Jr. [Domaine public].
Trypanosoma cruzi dans mono coeur. Pris et édité à partir de: Crédit photo: Provideurs de contenu (s): CDC / DR. L.L. Moore, Jr. [Domaine public]. Symptômes
Les symptômes de la maladie varieront en fonction de la phase dans laquelle elle est trouvée. Trois phases sont généralement définies: aiguë, indéterminée et chronique. Dans le premier, les parasites peuvent être facilement trouvés dans le sang puis disparaître au stade indéterminé.
Phase aigüe
Les signes sont variables, avec un stade asymptomatique, en particulier chez les adultes. Si le revenu se produit par les yeux, le syndrome ou le signe de la romaña peut se produire, qui se compose d'un œdème indolore dans un ou deux yeux, une conjonctivite et une inflammation des ganglions lymphatiques et peut persister pendant un ou deux mois.
D'autres symptômes de la maladie peuvent inclure la faiblesse et l'inconfort général du corps, la fièvre, les maux de tête et les articulations, le manque d'appétit, les nausées, les vomissements, la diarrhée et la myalgie ou les douleurs musculaires.
Dans certains cas, des eèques généralisés ou limités peuvent être présentés au visage ou aux membres inférieurs, un divertissement anormal du foie ou de la rate, ainsi que de la lymphadénopathie généralisée ou localisée.
Peut vous servir: Erysipelothrix rhusiopathiaeLa maladie de cette phase peut être mortelle pour les enfants et pour les personnes atteintes du système immunitaire engagé.
Phase indéterminée
Cette phase peut durer jusqu'à 40 ans; Il se caractérise par la disparition des parasites des échantillons de sang et parce que les patients n'ont aucun symptôme de la maladie.
Phase chronique
Dans cette phase, il y a des insuffisances du cœur ou du système digestif. Dans le cas des défaillances cardiaques, des douleurs thoraciques, une insuffisance cardiaque dans le ventricule gauche ou les deux ventricules, anévrismes, œdème périphérique, divertissement du foie, congestion pulmonaire et difficulté respiratoire et difficulté à respiration peut se produire.
Il est également possible que des embolies pulmonaires, des accidents vasculaires cérébraux et même une mort subite se produisent.
Chagas Evil peut également provoquer le mégacolon, dont les symptômes incluent la constipation (constipation), l'obstruction intestinale, la distension abdominale asymétrique, entre autres.
Traitements
Le mal de Chagas, s'il n'est pas traité, peut causer la mort, il y a des antiparasiticiens qui peuvent être appliqués, mais nécessitent des traitements prolongés. Ils sont plus efficaces au stade aigu de la maladie et ont des effets collatéraux importants qui peuvent forcer la suppression du traitement.
Si la maladie dans sa phase aiguë est détectée et confirmée chez les enfants, le traitement recommandé se compose de nifurtimox, 8 mg / kg divisé en trois doses fournies par voie orale, pendant une période qui peut durer entre 50 et 120 jours.
Effets secondaires
Les effets négatifs de ce médicament comprennent une perte d'appétit, d'insomnie et de nervosité, des hallucinations ou des crises peuvent également se produire, ainsi que la névrite périphérique, auquel cas le traitement doit être suspendu.
Si les médecins détectent la maladie dans leur phase chronique, le traitement se compose de benzonidazol, 4 à 7 mg / kg, pendant deux mois. Les effets néfastes incluent les étourdissements, les nausées, les vomissements, les maux de tête ou l'abdomen, la perte d'appétit et le poids, la polyneurite, la diminution des thrombocytes, ainsi que le violet allergique.
Des soins particuliers doivent être accordés au traitement des patients ayant des antécédents de maladie cardiaque, comme l'arythmie ou l'atullection ventriculaire, ainsi que ceux qui souffrent de maladies digestives du tube.
Les références
- C. Lire. Mastigophora (flagellé): caractéristiques, taxonomie, morphologie, habitat, maladies. Récupéré de:.com.
- C. Cobelli. Cycle de vie de Trypanosoma cruzi: Les 8 phases principales. Récupéré de:.com.
- Z. Brener (1992). Trypanosoma cruzi: Taxonomie, morphologie et cycle de vie à: s. Wendel, Z. Brener, M.ET. Camargo et A. Rassi (EDT.). Maladie de Chagas - Trypanosomiase américaine: impact IST sur la transfusion et la médecine clinique. ISBT Brazil'92, Sao Paulo, Brésil.
- Trypanosoma cruzi. À Wikipedia. Récupéré de: dans.Wikipédia.org.
- J.POUR. Marin-Neto, E. Cunha-ento, b.C. Maciel & M.V. Simões (2007). Pathogenèse des maladies cardiaques chroniques de Chagas. Circulation.
- POUR.R.L. Teixeira, m.M. Actes, m.C. Guimaro, un.SOIT. Sousa & n. Nitz (2011). Pathogenèse de la maladie de Chagas: parasite persistant et set-immun. Revues de microbiologie clinique.

