Effets de substitution nucléophile aromatique, exemples
- 1105
- 19
- Noa Da silva
La Substitution nucléophile aromatique (SNAR) est une réaction qui se produit dans la chimie organique, qui consiste dans le déplacement d'un bon groupe sortant par un nucléophile entrant. Du point de vue de son mécanisme et de ses aspects électroniques, c'est la face opposée de la substitution électrophile aromatique (Sear).
Généralement, le groupe sortant est un halogène, qui sort comme Haluro x Anion-. Cette réaction ne peut avoir lieu que si l'anneau aromatique (principalement le benzène) est déficient dans les électrons; c'est-à-dire si vous avez des groupes de substituants d'attracteur d'électrons.
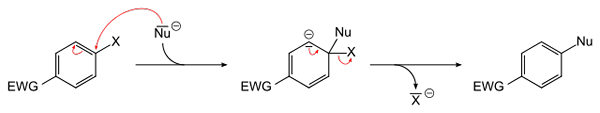
 Équation générale pour une substitution nucléophile aromatique. Source: Sponk [domaine public]
Équation générale pour une substitution nucléophile aromatique. Source: Sponk [domaine public] L'image supérieure schematise ce qui a été dit dans le paragraphe précédent. Le groupe d'attracteur EWG Electron (pour son acronyme en anglais: Groupe de retrait d'électrons), active l'anneau aromatique pour l'attaque nucléophile des espèces NU négatives-. On peut voir qu'un intermédiaire est formé (au centre), d'où le Haluro X est libéré ou libéré-.
Notez que en termes X simple, il est remplacé par Nu dans un anneau aromatique. Cette réaction est très polyvalente et nécessaire dans la synthèse de nouveaux médicaments, ainsi que dans les études de la chimie organique synthétique.
[TOC]
Aspects généraux
L'anneau aromatique peut être «chargé» ou «télécharger» à partir d'électrons en fonction de leurs substituants (ceux qui remplacent le lien C-H d'origine).
Lorsque ces substituants peuvent donner une densité électronique à l'anneau, il est dit qu'ils l'enrichissent des électrons; Si au contraire, ce sont des attracteurs de la densité électronique (l'EWG mentionné ci-dessus), il est alors dit qu'ils appauvrissent l'anneau électronique.
Dans tous les cas, l'anneau est activé pour une réaction aromatique spécifique, alors qu'elle est désactivée pour l'autre.
Par exemple, un anneau aromatique riche en électrons serait actif pour la substitution électrophile aromatique; C'est-à-dire que vous pouvez donner vos électrons à une espèce d'électrophilat et+. Cependant, il ne donnera pas d'électrons à une espèce NU-, Puisque les charges négatives se repousseraient.
Peut vous servir: théorie orbitale moléculaireMaintenant, si l'anneau est pauvre dans les électrons, il n'a pas comment les donner à l'espèce et+ (Sear ne se produit pas); Au lieu de cela, il est de la disponibilité d'accepter les électrons des espèces NU- (Snar se développe).
Différences avec la substitution électrophile aromatique
Clarifié les aspects généraux de l'entrée, certaines différences entre le SNAR et le Sear peuvent désormais être répertoriées:
- L'anneau aromatique agit comme un électrophile (pauvres électrons) et est attaqué par un nucléophile.
- Un groupe sortant X est remplacé de l'anneau; Pas un h+
- Aucune carbocation n'est formée, mais des intermédiaires avec une charge négative qui peut être déplacée par la résonance
- La présence de groupes plus attractifs dans l'anneau accélère la substitution au lieu de le ralentir
- Enfin, ces groupes n'exercent pas de directeurs sur l'endroit où (dans le carbone) le remplacement se produira. Le remplacement se produira toujours en carbone lié au groupe sortant x.
Le dernier point est également illustré dans l'image: le lien C-X est cassé pour former le nouveau lien C-NU.
Effets
Du nombre de substituants
Naturellement, plus les électrons sont les pauvres en anneau, plus le snar et le moins drastique seront les conditions nécessaires pour qu'il se produise. Considérez l'exemple suivant représenté dans l'image inférieure:
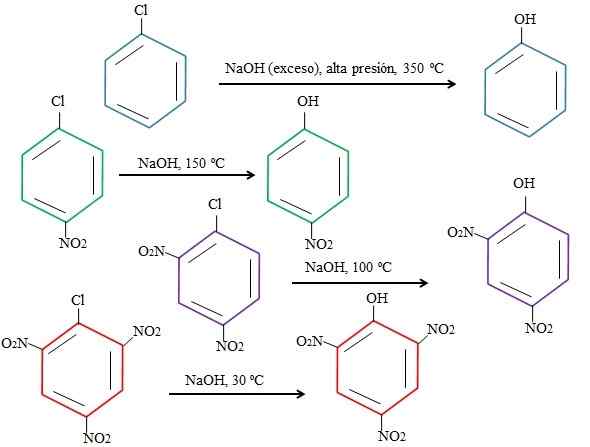 Effets des substituants sur les substitutions du 4-nitroclorobenzène. Source: Gabriel Bolívar.
Effets des substituants sur les substitutions du 4-nitroclorobenzène. Source: Gabriel Bolívar. Notez que le 4-nitroclorobenzène (anneau bleu) nécessite des conditions drastiques (haute pression et une température de 350 ºC) au remplacement du CL par. Dans ce cas, le chlore est le groupe sortant (CL-), et l'hydroxyde de nucléophiles (oh-).
Il peut vous servir: 4 périodes de chimie: de la préhistoire jusqu'à aujourd'huiLorsque le groupe n'apparaît pas2, qui est un attracteur d'électrons (anneau vert), la substitution peut être effectuée à une température de 150 ºC à pression ambiante. À mesure que le nombre de groupes augmente2 Présent (anneaux violets et rouges), le remplacement a lieu à des températures de plus en plus bas (100 ºC et 30 ° C, respectivement).
Par conséquent, les groupes ne2 Ils accélèrent le SNAR et l'illustration des électrons à l'anneau, le rendant plus sensible à l'attaque de OH-.
Les positions relatives du CL ne seront pas expliquées ici en ce qui concerne2 dans le 4-nitroclorobenzène, et comment ils modifient la vitesse de la réaction; Par exemple, les vitesses de réaction du 2-nitroclorobenzène et du 3-nitrochlorobenzène sont différentes, ce dernier étant le plus lent par rapport aux autres isomères.
Du groupe sortant
De retour au 4-nitroclorobenzène, sa réaction de substitution est plus lente si vous comparez celle de votre homologue fluorné:
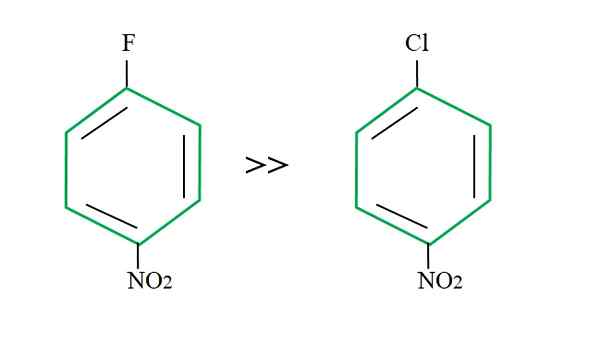 Effet de groupe sortant sur les réactions SNAR. Source: Gabriel Bolívar.
Effet de groupe sortant sur les réactions SNAR. Source: Gabriel Bolívar. L'explication de cela ne peut pas résider dans une autre variable que la différence entre F et Cl. Le fluor est un groupe sortant moche, car le lien C-F est plus difficile à briser que le lien C-CL. Par conséquent, la ventilation de ce lien n'est pas l'étape déterminante de la vitesse pour le SNAR, mais l'ajout de Nu- à l'anneau aromatique.
Le fluor pour être plus électronégatif que le chlore, l'atome de carbone qui lui est lié a une plus grande carence électronique (Cδ+-Fδ-). Par conséquent, le carbone de la liaison C-F est beaucoup plus susceptible d'être attaqué par Nu- que le lien C-CL. C'est pourquoi le remplacement de f par oh est beaucoup plus rapide que celui de Cl par oh.
Peut vous servir: sulfure de cuivre: structure, propriétés, utilisationsExemple
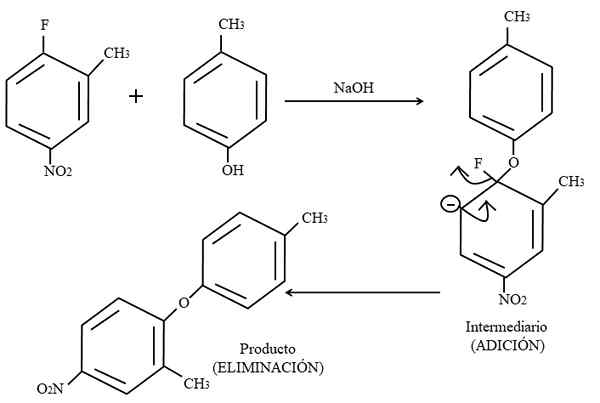 Remplacement électrophile aromatique. Source: Gabriel Bolívar.
Remplacement électrophile aromatique. Source: Gabriel Bolívar. Enfin, un exemple de ce type de réactions organiques dans l'image supérieure est illustré ci-dessous. Le para-coresol ne donne pas l'apparence d'être un nucléophile; Mais ayant un support de base, son groupe OH n'est pas protégé, laissant un anion phénoxyde, qui attaque le 2-méthyl-4-nitrofluorzène.
Lorsque cette attaque se produit, il est dit que le nucléophile est ajouté à l'électrophile. Cette étape peut être vue à droite de l'image, où le composé intermédiaire avec les deux substituants appartenant à l'anneau est formé.
En ajoutant du para-coresol, une charge négative apparaît qui déménage la résonance à l'intérieur de l'anneau (remarquez que ce cesse d'être aromatique).
Dans l'image, la dernière structure de résonance est à peine montrée, à partir duquel le fluor est fini comme F-; Mais en réalité, cette charge négative devient discocutée même dans les atomes d'oxygène du groupe2. Après l'ajout de l'élimination, le dernier, c'est-à-dire lorsque le produit est enfin formé.
Commentaire final
Le groupe no2 restant peut être réduit au groupe NH2, Et à partir de là, il est possible de faire plus de réactions de synthèse pour modifier la molécule finale. Cela montre le potentiel synthétique du SNAR, et que son mécanisme, en outre, se compose de deux étapes: l'une d'ajout et celle de l'élimination.
Actuellement, cependant, il existe des preuves expérimentales et informatiques que, en réalité, la réaction se déroule suite à un mécanisme concerté, où les deux étapes se produisent simultanément à travers un complexe activé et non un intermédiaire.
Les références
- Morrison, R. T. Et Boyd, R, n. (1987). Chimie organique. 5e édition. Éditorial Addison-Wesley Inter-American.
- Carey F. (2008). Chimie organique. (Sixième édition). Mc Graw Hill.
- Graham Salomons t.W., Craig B. Fryhle. (2011). Chimie organique. Amines. (10e édition.). Wiley Plus.
- Wikipédia. (2019). Substitution aromatique nucléophile. Récupéré de: dans.Wikipédia.org
- James Ashenhurst. (6 septembre 2019). Substitution aromatique nucléophile (NAS). Récupéré de: MasterOganicchemistry.com
- CHIMISTER BOOLISTexts. (5 juin 2019). Substitution aromatique nucléophile. Récupéré de: Chem.Bibliothèque.org
- « 50 blogs de jeux vidéo recommandés
- Historique de la circonium, propriétés, structure, risques, utilisations »

