Propriétés du silicate de calcium, structure, obtenant, utilisations

- 1408
- 307
- Mlle Ambre Dumont
Il silicate de calcium C'est le nom attribué à un groupe de composés chimiques formés à partir d'oxyde de calcium (CAO) et de silice (Sio2). La formule générale de ces composés est xcao • ySio2• ZH2SOIT.
Ce sont des solides blancs ou blancs jaunâtres. Ils peuvent être anhydre, c'est-à-dire sans eau (h2O) dans sa structure, ou ils peuvent le contenir. Ils font partie de plusieurs types de minéraux dans la nature.
 Minéral de silicate de calcium. Dave Dyet http: // www.Décollage.com http: // www.Teindre.com / domaine public. Source: Wikimedia Commons.
Minéral de silicate de calcium. Dave Dyet http: // www.Décollage.com http: // www.Teindre.com / domaine public. Source: Wikimedia Commons. Les silicates de calcium sont insolubles dans l'eau mais lorsqu'ils se joignent à cette forme des gels hydratés (matériaux tels que la gelée), alors lorsque le guinde est très dur, résistant et presque imperméable.
Cela a provoqué son utilisation dans l'industrie de la construction, car ils sont utilisés dans le ciment, les briques et les panneaux d'isolation d'humidité. Ils font également partie de matériaux pour guérir les perforations dans les dents et ont même été étudiés pour les utiliser dans la régénération osseuse, c'est-à-dire que le biomatériau.
Ils ont proposé de réduire la pollution générée par certaines industries métallurgiques. Ils sont également utilisés comme générateurs de frottements en freins et embrayages de véhicules.
[TOC]
Structure
Le silicate de calcium peut contenir une quantité variable d'oxyde de calcium (CAO) et de silice (Sio2). Sa formule générale est:
Xcao • ysio2• ZH2SOIT
où x, y, y z sont des nombres qui peuvent avoir diverses valeurs.
La quantité de CAO doit être comprise entre 3% et 35% (en poids sur la base sèche) et le contenu SIO2 Ce doit être de 50 à 95% (en poids de base sec). Ils peuvent être anhydre (sans eau dans leur structure, c'est-à-dire z = 0 dans la formule) ou peuvent être hydratés (avec de l'eau est leur conformation).
Nomenclature
- Silicate de calcium
- Sel de calcium d'acide sidéal
- Calcium et oxyde de silicium
Propriétés
État physique
Très fin blanc ou blanc blanc.
Poids moléculaire
Cao -Sio Calcium bustilicate2 ou casio3 = 116,16 g / mol
Point de fusion
Casio Calcium bustilicated3 = 1540 ° C
Densité
Casio Calcium bustilicated3 = 2,92 g / cc
Solubilité
Insoluble dans l'eau et l'éthanol.
pH
Une boue préparée avec un silicate de calcium à 5% peut avoir un pH de 8,4-12,5.
Autres propriétés
Le silicate de calcium peut être hydraté (avec de l'eau dans la molécule) ou anhydre (sans eau dans la molécule) avec plusieurs proportions de calcium sous forme d'oxyde de Cao et de silice sous forme de dioxyde de sio sio2.
Il a une capacité d'absorption d'eau élevée. Calcium bustilicate (Cao • sio2 ou casio3) se démarque de son éclat et de sa blancheur, de son faible humidité, de son faible teneur en volatile et de sa bonne absorption d'huile.
Peut vous servir: propriétés coligatives des solutions Casio Calcium bustilicated3. Ondřej Mangl / Pub Domain. Source: Wikimedia Commons.
Casio Calcium bustilicated3. Ondřej Mangl / Pub Domain. Source: Wikimedia Commons. Parmi les hydrates de silicate de calcium se distinguent par ceux formés en ajoutant de l'eau à l'AC2Sio5 et à ca3Sio5. Les produits d'hydratation de ces deux composés sont les plus abondants dans certains types de ciment.
Obtention
Le silicate de calcium est obtenu de plusieurs manières en réagissant au matériau siliceux (comme les diatomateurs) et en composés calciques (tels que l'hydroxyde de calcium (CA (OH)2).
Le silicate de calcium peut être préparé, par exemple, le calcination de l'oxyde de calcium (CAO) avec de la silice (Sio2) à des températures élevées.
Lorsque la réaction est faite à une raison molaire 1: 1 (cela signifie qu'il y a le même nombre de molécules CaO que de SiO2) Il en résulte des buts de calcium3 O Cao • Sio2:
Cao + Sio2 + Chauffer → Casio3
Applications
En obtenant des briques
Avec du silicate de calcium, des unités ou des briques sont fabriquées pour la construction. Ils sont obtenus avec un siliceo fin et un matériau de citron vert vivant ou un cal hydraté. Vous pouvez ajouter des pigments inertes pour donner une couleur différente à la brique.
Les unités sont moulées sous pression et guérissent en autoclave (four à vapeur) à 170 ° C pendant 4 à 6 heures. Pendant la guérison, quelque chose du citron.
 Briques de silicate de calcium. Holger.Ellgaard / cc by-sa (https: // CreativeCommons.Org / licences / by-sa / 3.0). Source: Wikimedia Commons.
Briques de silicate de calcium. Holger.Ellgaard / cc by-sa (https: // CreativeCommons.Org / licences / by-sa / 3.0). Source: Wikimedia Commons. Cependant, les briques de silicate de calcium ont tendance à se développer et à rétrécir plus que les briques d'argile, ce qui peut parfois provoquer une fissuration de maçonnerie.
Cela a attiré l'attention et a été considéré comme potentiellement dangereux.
Dans le ciment Portland
Les silicates de calcium font partie du ciment Portland, qui est un matériau largement utilisé dans l'industrie de la construction.
Le ciment Portland est un ciment hydraulique qui est produit par la pulvérisation des matériaux principalement pour les silicates de calcium hydratés et le boîtier de sulfate de calcium4 (et ainsi).
 Surface du ciment. Le ciment contient des silicates de calcium dans sa composition. Auteur: Pexels. Source: Pixabay.
Surface du ciment. Le ciment contient des silicates de calcium dans sa composition. Auteur: Pexels. Source: Pixabay. Il durcit rapidement en raison de la réaction d'hydratation générée par un gel de calcium hydraté. Il en résulte un matériau fort, dense et peu perméable (qui ne laisse pas l'eau passer)).
Les silicates qu'il contient sont du silicate de CA trichalcal3Sio5 ou 3cao.Sio2 et le silicato dicale ca2Sio4 ou 2cao.Sio2.
Pour immobiliser les ordures radioactives
Les silicates de calcium dans le ciment peuvent varier en pourcentage en poids. La composition du ciment Portland peut changer en fonction du type de structure de construction à laquelle il est prévu.
Peut vous servir: hydrocarbures insaturésCertains types de ce ciment sont utilisés pour l'immobilisation radioactive des ordures afin de ne pas endommager les personnes ou l'environnement.
Comme isolant pour les bâtiments
Le silicate de calcium sert à obtenir des planches en mousse minérale ou des panneaux minéraux isolants.
 Calcium silicates feuilles. Achim Hern / CC par (https: // CreativeCommons.Org / licences / par / 3.0). Source: Wikimedia Commons.
Calcium silicates feuilles. Achim Hern / CC par (https: // CreativeCommons.Org / licences / par / 3.0). Source: Wikimedia Commons. Ceux-ci servent à isoler les murs d'humidité. Ils mélangent Cao et Sio2 Avec de l'eau et 3 à 6% de cellulose est ajoutée, ce qui améliore la flexibilité et la stabilité des bords.
La boue résultante est versée dans des moules puis chauffée avec de la vapeur à haute pression et à la température dans un four spécial avec de la vapeur appelée autoclave.
Le résultat est une mousse rigide, des pores très finement coupés en feuilles ou en planches et traités avec des additifs spéciaux afin que l'eau puisse repousser.
La mousse de silicate de calcium est utilisée dans le secteur de la construction, en particulier pour isoler les murs et améliorer la protection de l'humidité, étant utile en particulier dans le renouvellement des anciens bâtiments.
Pour réduire la pollution dans l'industrie métallurgique
Le dicálcico silicato ca2Sio4 ou 2cao.Sio2 qui se trouve dans les scories ou les déchets de production d'acier ont été utilisés pour précipiter les métaux dissous dans les acides d'effluent d'autres processus métallurgiques.
Le précipité signifie que le métal dissous fait partie d'un composé solide qui va au bas du récipient et peut être collecté.
 Une certaine industrie des déchets a des silicates de calcium utiles pour précipiter les solutions acides. Auteur: Skeze. Source: Pixabay.
Une certaine industrie des déchets a des silicates de calcium utiles pour précipiter les solutions acides. Auteur: Skeze. Source: Pixabay. La CA2Sio4 Présent dans le laitier en acier réagit avec l'eau et produit du CA (OH)2 qui a la capacité de neutraliser l'acidité des solutions acides des métaux d'autres processus:
2 CA2Sio4 + 4 h2O → 3CAO.22.3h2O + ca (oh)2
En plus de la neutralisation, le composé de silicate de calcium peut adsorber certains des ions métalliques m2+ Par échange avec l'ion calcio ca2+. Vous trouverez ci-dessous un schéma:
≡Si-o-ca + m2+ → ≡Si-o-m + ca2+
Le composé solide contenant le métal peut ensuite être utilisé à un autre but et n'est pas jeté. Ceci est un exemple d'écologie industrielle.
Dans les biomatériaux
Les silicates de calcium ont commencé à essayer les biomatériaux depuis 1990. Ils ont été étudiés pour une utilisation potentielle dans la régénération des tissus osseux car ils ont une bioactivité supérieure à d'autres matériaux.
Ceci est attribué au fait qu'ils ont du silicium (Si), qui joue un rôle essentiel dans les mécanismes qui conduisent à une nouvelle formation osseuse.
Peut vous servir: acide sulfurique (H2SO4)Les ciments basés sur les silicates de calcium ont la capacité d'induire un revêtement de phosphate de calcium / apatite lorsqu'ils sont submergés dans des fluides biologiques et favorisent la régénération tissulaire.
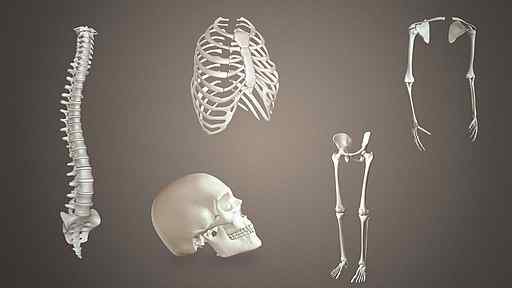 Les silicates de calcium peuvent fonctionner comme une base pour les biomatériaux qui permettent la réparation des os. https: // www.Scientifanimations.com // cc by-sa (https: // CreativeCommons.Org / licences / by-sa / 4.0). Source: Wikimedia Commons.
Les silicates de calcium peuvent fonctionner comme une base pour les biomatériaux qui permettent la réparation des os. https: // www.Scientifanimations.com // cc by-sa (https: // CreativeCommons.Org / licences / by-sa / 4.0). Source: Wikimedia Commons. Pour ces raisons, il est considéré comme un matériau approprié pour la réparation des os.
En biodétine
Le silicate de calcium fait partie de la biodente. Il s'agit d'un matériau qui est utilisé pour réparer les percations de dents, les réabsorption osseuse et comme remplissant l'extrémité des racines des dents.
La biodétine est un ciment bioactif avec peu de porosité qui a une force mécanique ou une dureté supérieure aux autres matériaux et qui ressemble à la dentine.
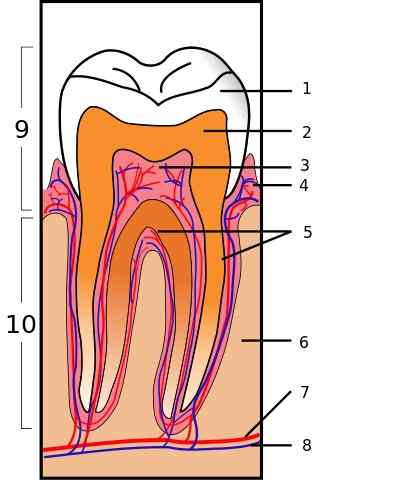 Les silicates de calcium font partie des matériaux qui servent à couvrir les perforations des dents. Domaine Jak / pub. Source: Wikimedia Commons.
Les silicates de calcium font partie des matériaux qui servent à couvrir les perforations des dents. Domaine Jak / pub. Source: Wikimedia Commons. Il est formé par le silicate Triccal (CA3Sio5), Silicate dicale (CA2Sio5), carbonate de calcium (Caco3) et l'oxyde de zirchon. Lors du mélange avec de l'eau, les silicates de calcium forment un gel hydraté collant qui, après un temps de solidification, créant une structure dure.
Il exerce un effet positif sur les cellules de pulpe dentaire et accélère la formation de ponts dans la dentine, où il met en évidence la résistance de ses liaisons, sa microduction et sa résistance à la compression.
 Tube avec silicate de calcium pour guérir les dents. Shaimaa abdelatif / cc by-sa (https: // CreativeCommons.Org / licences / by-sa / 4.0). Source: Wikimedia Commons.
Tube avec silicate de calcium pour guérir les dents. Shaimaa abdelatif / cc by-sa (https: // CreativeCommons.Org / licences / by-sa / 4.0). Source: Wikimedia Commons. Autres applications
Les silicates de calcium sont également utilisés comme agents antia-listes et assistants de filtration.
Casio Calcium bustilicated3 Il est utilisé dans la céramique, dans des appareils où une frottement est nécessaire, comme les freins et les griffes de véhicules, et dans l'obtention de métaux.
Pour sa haute brillance et son blanc le casio3 Il est utilisé dans le remplissage des peintures et des plastiques.
Les références
- Ropp, r.C. (2013). Groupe 14 (C, SI, GE, SN et PB) Composés de la Terre alcaline. Silicates de calcium. Dans l'encyclopédie des composés terrestres alcalins. Récupéré de ScienceDirect.com.
- FAO (2015). Silicate de calcium. Spécifications préparées au 80e JECFA (2015) et publié dans FAO JECFA Monographies 17. Récupéré de la FAO.org.
- Harrisson, un.M. (2019). Constitution et spécification du ciment Portland. Hydrate de silicate de calcium. Dans Lea's Chemistry of Cement and Concrete (cinquième édition). Récupéré de ScienceDirect.com.
- Gellert, R. (2010). Matériaux minéraux inorganiques pour l'isolation dans les bâtiments. Mousse de silicate de calcium et mousse minérale. Dans les matériaux pour l'efficacité énergétique et le confort thermique dans Bildings. Récupéré de ScienceDirect.com.
- Goudouri, O-M. et al. (2016). CARACTÉRISATION DU COMPORT DE DÉGRADATION DES ÉCHAFAGES BIOCÉRIQUES. Échafaudages d'apatite / wollastonite. Dans la caractérisation et la conception d'échafaudages tissulaires. Récupéré de ScienceDirect.com.
- Rani, P. et al. (2019). Nanocomposites de plafonnement de la pulpe dentaire. Biodentine. Dans les applications des matériaux nanocomposites en dentisterie. Récupéré de ScienceDirect.com.
- Ingham, J.P. (2013). Produits en béton. Unités de silicate de calcium. Dans les géomatériaux sous le microscope. Récupéré de ScienceDirect.com.
- Eyovan, m.Toi. Et Lee, W.ET. (2005). Immobilisation des déchets radioactifs dans le ciment. Ciment hydraulique. Dans une introduction à l'immobilisation des déchets nucléaires. Récupéré de ScienceDirect.com.
- Ramachandra Rao, S. (2006). Récupération des ressources et recyclage à partir de déchets métallurgiques. Silicate de calcium comme précipitant pour les métaux dissous. Dans les séries de gestion des déchets. Récupéré de ScienceDirect.com.
- Prati, c. et gandolfi, m.g. (2015). Ciments bioactifs de silicate de calcium: perspectives biologiques et applications cliniques. Dent Mater, 2015 AP; 31 (4): 351-70. NCBI a récupéré.NLM.NIH.Gouvernement.
- « Structure de sulfure de calcium (CAS), propriétés, obtention, utilisations
- Explication de la loi de Coulomb, formule et unités, exercices, expériences »

