Particules subatomiques
- 1314
- 294
- Mlle Ambre Dumont
 Principales particules subatomiques
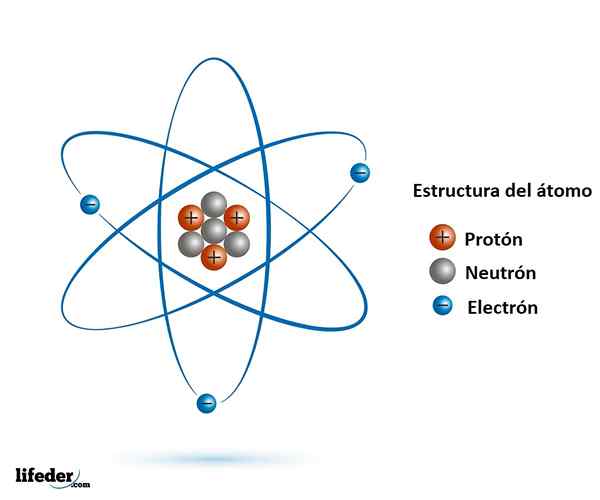
Principales particules subatomiques Que sont les particules subatomiques?
Le Particules subatomiques Ils sont plus petits que l'atome et se trouvent dans la nature, presque tous en faisant partie. Nous connaissons bien le principal et le plus stable, qui sont l'électron, le proton et le neutron.
Toute la matière est composée de ces particules, bien qu'il y en ait d'autres, bien que pendant longtemps son existence ait été ignorée. Les premiers modèles atomiques, datant de quelques siècles avant le Christ, supposaient que les atomes étaient indivisibles, quelque chose comme des billes qui, combinées d'une certaine manière, ont donné naissance aux différents éléments.
Quand on a appris qu'il ne l'était pas, grâce aux découvertes de l'électron au 19e siècle et au noyau atomique au début du 20e siècle, les scientifiques se sont demandé si ces particules avaient une structure interne.
Il s'est avéré que le proton et le neutron sont des particules composées encore plus petites, qui n'ont pas de structure interne: ce sont les particules élémentaires.
C'est pourquoi les particules subatomiques sont divisées en:
- Particules composites.
- Particules élémentaires.
Les particules élémentaires sont des quarks, des glluons et des leptones. Les quarks et les glluons composent des protons et des neutrons, tandis que l'électron, une particule élémentaire, est un Lepton.
Découverte de particules subatomiques
Les découvertes des particules subatomiques ont commencé à partir du XIXe siècle et la première à trouver était l'électron.
En 1890, les physiciens étaient très occupés à étudier le rayonnement et la transmission des ondes électromagnétiques. J. J. Thomson était l'un d'eux et a mené de nombreuses expériences avec un tube auquel l'air avait été extrait et mis sur quelques électrodes.
 J. J. Thomson
J. J. Thomson Lorsqu'une tension a été appliquée, des rayons mystérieux ont été produits, appelés Rays de Cathode, dont la nature était inconnue, jusqu'à J jusqu'à J. J. Thomson (1856-1940) a découvert qu'ils étaient constitués de particules chargées négativement.
Thomson a obtenu le quotient entre la charge et la masse de ces particules: 1.76 x 108 C / G, où C signifie coulomb, L'unité de charge électrique dans le système international des unités et G est Gram.
Peut vous servir: Réfraction légère: éléments, lois et expérienceEt il a trouvé deux choses très importantes, la première que la masse des particules était extrêmement petite, et deuxièmement, que cette valeur était la même pour chacune, peu importe ce que les électrodes ont été faites.
La valeur de la charge a été trouvée peu de temps après, au début des années 1900, par le physicien américain Robert Millikan (1868-1953) et ses collaborateurs, grâce à l'expérience de La chute d'huile.
Le noyau atomique: protons et neutrons
 Portrait Henri Becquerel
Portrait Henri Becquerel À la fin du XIXe siècle, Henri Becquerel (1852-1908) avait découvert le phénomène de la radioactivité naturelle, qui a intrigué d'autres physiciens tels que les conjoints Marie et Pierre Curie, ainsi que le néozygous Ernest Rutherfordford.
Ces derniers ont trouvé trois types différents de rayonnement à partir d'échantillons d'uranium, un élément radioactif bien connu. Il les a nommés avec les trois premières lettres de l'alphabet grec: α, β et γ.
Expériences de dispersion de Rutherford
 Le jeune Ernest Rutherford
Le jeune Ernest Rutherford En utilisant les particules α, très énergique et chargée positivement, Rutherford Bombard.
Mais curieusement, une petite fraction de particules a été détournée et quelques-unes ont même rebondi dans la direction opposée. Ce dernier était inimaginable, car comme l'a dit Rutherford, c'était comme tirer avec un fusil un mince mouchoir et voir que les balles reviennent.
La raison pour laquelle les particules α s'écartent est que dans la feuille, il y a quelque chose qui les repousse et doit donc être chargé positivement. C'est le noyau atomique, de taille minuscule, mais qui contient presque toute la masse de l'atome.
La découverte de neutrons
 James Chadwick
James Chadwick Le neutron a pris un peu plus de temps et était dû au physicien anglais James Chadwick (1891-1974), étudiant de Rutherford. Rutherford lui-même avait proposé l'existence d'une particule sans charge dans le noyau, pour expliquer pourquoi cela n'est pas désintégré à cause de la répulsion électrostatique.
Les expériences de Chadwick ont révélé en 1932 l'existence d'une masse de masse très similaire à celle du proton, mais sans charge. C'est pourquoi ils l'appelaient neutron et à côté du proton, ils sont les composants essentiels du noyau atomique.
Peut vous servir: énergie électromagnétique: formule, équations, utilisations, exemplesLes principales particules subatomiques
En général, les particules subatomiques sont caractérisées par:
- Masse.
- Charge électrique.
- Rotation.
Le spin est une qualité analogue à la rotation sur l'axe, mais de nature entièrement quantique. Et d'un autre côté, il y a des particules avec charge et masse 0, comme le photon.
Électron
L'électron est une particule subatomique stable, chargée négativement et appartenant au groupe Leptones, étant celle avec la masse la plus basse. C'est une partie essentielle de l'atome, mais elle peut exister isolé de cela, sous la forme de électrons libres.
En fait, c'est la plus petite charge électrique qui peut être trouvée dans la nature, donc tout autre est le multiple de l'électron, selon le principe de quantification de la charge.
Ses principales caractéristiques sont:
- Messe: 9.1 x 10-31 kg
- Charge: E = -1.6 x 10-19 C
- Spin: ± ½
- Antiparticule: positron.
L'électron est responsable de la formation de liaisons chimiques, ainsi que de la conduction électrique et thermique. Et grâce à la mécanique quantique, nous savons que l'électron a un double comportement: onde et particule en même temps.
Proton
C'est une particule à charge électrique, dont la charge est la même ampleur que celle de l'électron, mais du signe opposé.
Le proton n'est pas une particule élémentaire comme l'électron, mais est composé de trois quarks unis par Gluones Et c'est beaucoup plus massif que l'électron.
Contrairement à cela, le proton se limite au noyau atomique, et sa quantité détermine de quel élément elle est, ainsi que ses propriétés.
- Messe: 1.672 x 10-27 kg
- Charge: E = +1.6 x 10-19 C
- Spin: ½
- Antiparticule: antiproton.
Neutron
Le neutron à côté du proton forme le noyau atomique et se compose également de trois quarks: deux du type Bas et un de type EN HAUT.
- Messe: 1.675 x 10-27 kg
- Pas de charge nette.
- Spin: ½.
C'est une particule stable dans le noyau atomique, mais en tant que particule libre, il diminue avec une demi-vie d'environ 10.Environ 3 minutes. Sa masse est à peine supérieure à celle du proton et comme nous l'avons dit, il manque de charge nette.
Peut vous servir: chaleur latenteLe nombre de neutrons d'un atome est important, car bien qu'il ne détermine pas la nature de l'élément, comme le fait le proton, il détermine la classe isotopique.
Les isotopes d'un élément sont des variantes de la même chose et leur comportement peut être très différent les uns des autres. Il y a stable et instable, par exemple l'hydrogène a comme isotopes le deutérium et le tritium.
Bombardant les atomes de neutrons de certains composés d'uranium et de plutonium, le noyau est de la fourrure. La réaction en chaîne nucléaire qui se produit est capable d'émettre une grande quantité d'énergie.
Quarks

Ce sont les constituants des protons et des neutrons. Jusqu'à présent, 6 types de quarks ont été trouvés, mais aucune comme une particule libre, mais associée à la formation d'autres particules composites.
La preuve de son existence a été obtenue par des expériences réalisées depuis les années 60, avec l'accélérateur linéaire de Stanford puis au Cern.
- Charge: + 2/3E, -1 / 3E
- Spin: ½
- Antiparticule: antiquark.
Autres particules
À partir de 1930, les découvertes de nouvelles particules ont suivi, beaucoup prédits par la théorie. Le modèle de particules standard envisage l'existence de 17 types de particules fondamentales, entre les quarks, les leptones, les bosons et le boson de Higgs.
Ils ont également leurs antiparticules respectifs qui, lors de l'interaction, sont anéantis, générant de nouvelles particules. En voici quelques uns:
-Positron, identique à l'électron mais avec une charge positive.
-Neutrino, sans charge.
-méson.
-Bosones, qui sont les porteurs des interactions fondamentales, sauf la gravité.
-Le boson de Higgs, responsable de la masse.
-Gravitón, est une particule proposée pour expliquer la gravité, mais il n'y a toujours aucune preuve qu'il y a.
Les références
- Chang, R. 2013. Chimie. 11va. Édition. Mc Graw Hill Education.
- Cobian, J. Le modèle de particules standard. Récupéré de: sne.est.
- Fernández de Sala, P. Particules élémentaires, particules composées et particules virtuelles. Récupéré de: ific.UV.est.
- Giambattista, un. 2010. La physique. 2e. Élégant. McGraw Hill.
- Olmo, m. Protons et neutrons. Récupéré de: hyperphysique.Phy-asch.GSU.Édu.

