Métaux alcalinétres
- 4095
- 58
- Prof Noah Collet
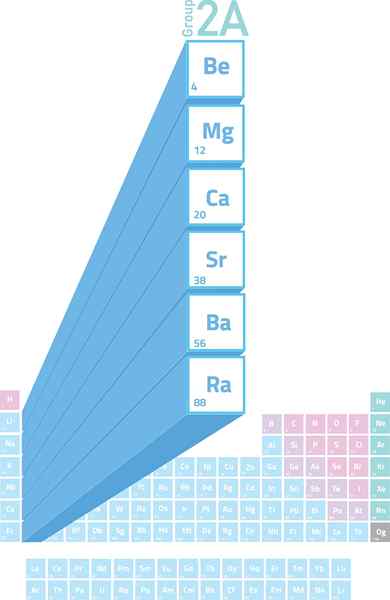
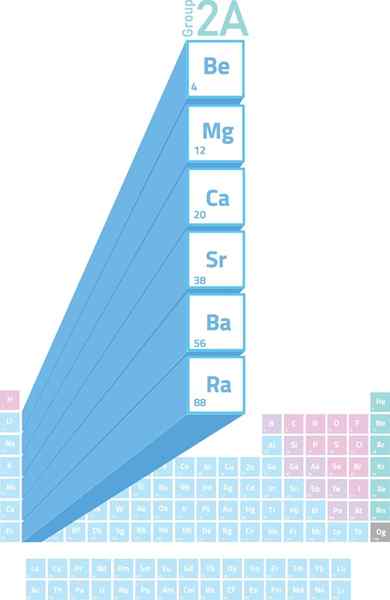 Emplacement des métaux alcalinotherres dans le tableau périodique
Emplacement des métaux alcalinotherres dans le tableau périodique Que sont les métaux alcaline?
Les Métaux alcalinétres Ce sont les éléments du groupe 2 (anciennement appelé groupe 2A) du tableau périodique. C'est-à-dire qu'ils sont formés par les 6 éléments de la deuxième colonne du tableau périodique allant du béryllium (be) à la radio (RA).
Ils sont un groupe d'éléments métalliques assez réactifs et relativement communs. Ils n'ont que deux électrons de valence situés dans une orbitale S. Pour cette raison, ils appartiennent aux blocs du tableau périodique.
Le nom "alcalinoterreo" vient de l'union des mots "alcalins", qui est une autre façon de dire de base, et de la terre, c'est ainsi qu'on leur a dit avant les oxydes. Donc, les métaux alcalinotherres signifient littéralement des métaux qui forment des oxydes de base.
Ces métaux ont de nombreuses applications qui les rendent importantes dans notre société actuelle, en particulier le magnésium. Ces applications sont dues à leurs propriétés particulières, qui sont décrites ci-dessous.
Propriétés des métaux alcalinotherres
Ils ont l'apparence du métal
Tous les métaux alcalinotherres ont une couleur argentée avec une luminosité métallique. Le radon est également radioactif, donc il brille dans l'obscurité en émettant une lumière verte caractéristique.
Ce sont de peu de métaux denses
Tous les métaux alcalinotherres sont plus denses que l'eau, mais sont moins denses que la plupart des autres éléments métalliques du tableau périodique.
Les densités de ce groupe varient de 1,54 g / cm3 Pour le calcium jusqu'à 5,5 g / cm3 Pour la radio, ce qui est considérablement inférieur aux densités d'autres métaux tels que le fer (7,9 g / cm3), cuivre (9,0 g / cm3), plomb (11,3 g / cm3) et El Mercurio (13,5 g / cm3), pour n'en nommer que quelques-uns.
Ils ont des points de fusion et d'ébullition relativement bas
Étant des métaux, ses points de fusion et d'ébullition sont supérieurs à ceux de la plupart des non-métaux. Cependant, ils sont inférieurs aux points de fusion et d'ébullition de la plupart des autres métaux, à quelques exceptions.
Peut vous servir: équation d'ArrheniusIls ont Valencia +2
En raison de leur configuration électronique, ces métaux ont tendance à perdre deux électrons lorsqu'ils réagissent avec d'autres éléments tels que les non-métaux. Pour cette raison, son seul Valence est +2.
Ils sont relativement réactifs
Les métaux alcalinotherres sont beaucoup plus réactifs que les métaux tels que le fer ou le cuivre, mais sont moins réactifs que les métaux alcalins (les éléments du groupe 1). Plus le groupe est bas, plus le métal est réactif.
Par exemple, le béryllium (le premier du groupe) ne réagit pas avec l'eau tandis que les deux suivants peuvent réagir avec de l'eau chaude et les derniers peuvent même réagir à l'eau froide.
Réagir avec l'air pour former des oxydes de base
Ces métaux ont tendance à former des oxydes de base lorsqu'ils réagissent avec l'oxygène d'air. En fait, c'est pourquoi ils sont appelés alcaliners. Ces oxydes, lors de la dissolution dans l'eau, deviennent des hydroxydes qui produisent des solutions alcalines ou de base.
Applications de métaux alcalinotherres
Dans l'industrie de la technologie
Certains des métaux alcalinotherres sont utilisés dans la fabrication de semi-conducteurs. Ceux-ci sont essentiels dans la construction de circuits électroniques tels que ceux qui contiennent pratiquement tous les appareils électriques modernes, des ordinateurs et des téléphones portables aux machines à laver, aux voitures et autres.
Dans l'industrie alimentaire
Le calcium est un nutriment essentiel pour la vie. Il fait partie de la structure des os et a d'autres fonctions importantes dans le corps. Pour cette raison, cet élément est ajouté en tant que fortifier à de nombreux aliments, des céréales aux produits laitiers. De plus, il est également utilisé dans la fabrication du fromage.
Il peut vous servir: circonium: histoire, propriétés, structure, risques, utilisationsDans l'industrie automobile
Certains des métaux alcalinotherres ont de très bonnes propriétés mécaniques, ce qui signifie qu'ils sont durs et résistants. De plus, ils sont résistants à la corrosion, ils sont donc fréquemment utilisés dans la fabrication de roues de luxe pour les voitures ainsi que dans d'autres parties d'entre elles.
Dans l'industrie militaire
En raison de leurs propriétés mécaniques et de leur faible densité, des métaux tels que le magnésium et le béryllium sont utilisés dans la construction d'avions de combat, de satellites et d'hélicoptères.
De plus, en raison de leurs propriétés électriques, ils sont également utilisés dans la fabrication de différents types de capteurs et de systèmes optiques et électroniques que l'industrie militaire utilise pour créer des armes et des systèmes de communication.
Les six métaux alcalins
Il n'y a que six métaux alcalins. Ensuite, il y a une brève description de chacun d'eux:
Béryllium (be)
C'est l'élément numéro 4 du tableau périodique et le premier du groupe de métaux alcalinotherres. C'est un métal très léger et fort avec des propriétés uniques qui le rendent utile dans la fabrication de semi-conducteurs.
Magnésium (mg)
Le magnésium est un métal argenté relativement léger, avec un point de fusion et d'ébullition faible (par rapport aux autres métaux). Il est très dur et résistant et est fréquemment utilisé dans la fabrication de pièces automobiles et comme additif dans la préparation d'alliages tels que certains types d'acier.
Il s'agit du deuxième métal alcalin et numéro 12 du tableau périodique. Comme d'autres éléments de ce groupe, c'est un nutriment essentiel pour la vie.
Calcium (CA)
Le calcium est le 5ème élément le plus abondant du cortex terrestre. Il se trouve comme carbonate de calcium dans de nombreux minéraux et roches et est également un élément essentiel pour la vie en raison de sa participation à la formation d'os et de son importance dans le système nerveux.
Peut vous servir: chlorure de strontium (SRCL2)Ce métal est l'élément numéro 20 du tableau périodique, en quatrième période et est le troisième métal alcalinher.
Strontium (SR)
L'élément numéro 38 et quatrième métal alcalin est le strontium. Il est plus lourd que le calcium, mais il semble beaucoup en termes de propriétés chimiques et physiques. En fait, le strontium peut remplacer le calcium dans les os.
Ceci est particulièrement problématique lorsque nous nous exposons à un strontium radioactif qui se produit après une réaction nucléaire, car, lorsque vous adhérez aux os, il est très difficile d'éliminer du corps et nous empoisonne avec un rayonnement peu à peu.
Barium (BA)
Cet élément a le numéro atomique 56 et a également des propriétés assez similaires à celles du calcium et du strontium. C'est un métal plutôt doux et très réactif qui n'est pas de nature élémentaire. C'est l'un des métaux alcalinotherres avec un plus grand caractère métallique.
Radio (RA)
Le dernier élément du groupe Alcalinoterreos est la radio, un métal radioactif (d'où son nom) qui émet une légère lumière verte qui est facile à observer dans l'obscurité.
Il était beaucoup utilisé dans la préparation de peintures qui brillent dans l'obscurité, mais après la découverte du danger de santé, son utilisation a été interdite.

