Hydroxyde de strontium (SR (OH) ₂)

- 1245
- 328
- Mlle Ambre Dumont
 Hydroxyde de strontium
Hydroxyde de strontium Qu'est-ce que l'hydroxyde de strontium?
Il Hydroxyde de strontium (Sr (OH) ₂) est un composé chimique inorganique formé par un ion strontium (SR) et deux ions hydroxyde (OH). Ce composé est obtenu en combinant un sel de strol avec une base forte, résultant en un composé de nature alcaline dont la formule chimique est SR (OH)2.
En général, pour la préparation de l'hydroxyde de strontium, l'hydroxyde de sodium (NaOH) ou l'hydroxyde de potassium (KOH) est utilisé comme base forte. D'un autre côté, le sel de strontium (ou ion strontium) qui réagit avec la base forte est le nitrate de strontium SR (non3)2 Et le processus est décrit par la réaction chimique suivante:
2koh + sr (non3)2 → 2kno3 + SR (OH)2
En solution le cation strontium (sr+) Il entre en contact avec l'hydroxyde anion (oh-) Former un sel de strontium ionique basique. Étant donné que le strontium est un métal alcalin, l'hydroxyde de strontium est considéré comme un composé alcali caustique.
Obtention de l'hydroxyde de strontium
En plus du processus expliqué précédemment, on peut dire qu'une fois la réaction réalisée, SR (OH)2 précipiter dans la solution. Ensuite, cela est soumis au processus de lavage et de séchage, obtenant enfin une très fine poudre blanche.
Une autre méthode pour obtenir l'hydroxyde de strontium provient du chauffage du carbonate de strontium (SRCO3) ou sulfate de strontium (SRSO4), avec de la vapeur à une température allant entre 500 ° C et 600 ° C. La réaction chimique se produit comme indiqué ci-dessous:
SRCO3 + H2O → SR (OH)2 + CO2
SRS + 2H2O → SR (OH)2 + H2S
Peut vous servir: acide soufréStructure chimique et propriétés physicochimiques
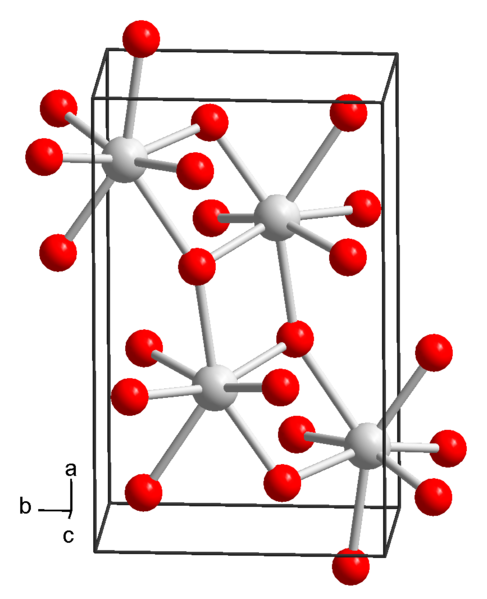 Structure chimique de l'hydroxyde de strontium. Source: Wikimedia Commons
Structure chimique de l'hydroxyde de strontium. Source: Wikimedia Commons À l'heure actuelle, 3 formes d'hydroxyde de strontium sont connues: octahydrate, monohydrate et anhydre.
Hydroxyde de strontium octobre
Des solutions dans des conditions de température et de pression normales (25 ° C et 1 atm), l'hydroxyde de strontium précipite d'une manière octahydratée, dont la formule chimique est SR (OH)2∙ 8h2SOIT.
Ce composé a une masse molaire de 265,76 g / mol, une densité de 1,90 g / cm et précipite sous forme de cristaux tétragonaux (avec groupe spatial P4 / NCC) de l'apparence prismatique quadrangulaire et.
De même, l'hydroxyde de strontium octonisé a la capacité d'absorber l'humidité atmosphérique, car il s'agit d'un composé facilement délicieux.
Hydroxyde de strontium monohydraté
Selon les études de microscopie optique (réalisée par la technique de diffraction des rayons x), en augmentant la température à environ 210 ° C - une pression atmosphérique constante - le SR (OH)2∙ 8h2O Il est déshydraté et transformé en hydroxyde de strontium monohydraté (SR (OH)2∙ H2SOIT).
Cette forme du composé a une masse molaire de 139,65 g / mol et sa température de fusion est de -73,15 ° C (375K). En raison de sa configuration atomique, cela présente moins de solubilité dans l'eau que celle décrite dans sa forme d'octahydrate.
Hydroxyde de strontium anhydre
En continuant avec l'augmentation de la température du système à environ 480 ° C, la déshydratation est prolongée jusqu'à un hydroxyde d'étirement anhydre.
Contrairement à ses formes hydratées, il a une masse molaire de 121,63 g / mol et une densité de 3 625 g / cm3. Son point d'ébullition est atteint à 710 ° C (1 310 ° F ou 983 K) tandis que le point de fusion est à 535 ° C (995 ° F ou 808 K).
Peut vous servir: ididio 192Solubilité
L'hydroxyde d'octahydrate de strontium a une solubilité dans l'eau de 0,91 gramme par 100 millilitres (mesuré à 0 ° C), tandis que sa forme anhydre dans des conditions de température similaires a une solubilité de 0,41 gramme pour 100 millilitres.
De même, cette substance est considérée comme insoluble dans l'acétone et totalement soluble dans les acides et le chlorure d'ammonium.
Réactivité chimique
L'hydroxyde de strontium n'est pas inflammable, sa réactivité chimique reste stable à des températures et des pressions modérées, et est capable d'absorber le dioxyde de carbone de l'air atmosphérique, le transformant en carbonate de strontium.
De plus, c'est un composé gravement irritant si vous entrez en contact avec la peau, les voies respiratoires ou d'autres muqueuses.
Utilisation de l'hydroxyde de strontium
En raison de ses caractéristiques hygroscopiques et de ses propriétés de base, l'hydroxyde de strontium est utilisé pour différentes applications dans l'industrie:
- Extraction de Moice et raffinage de sucre à partir de la betterave.
- Stabilisateur en plastique.
- Graisses et lubrifiants.
Extraction de mice et raffinage de sucre de betterave
Au début du 21e siècle, en Allemagne, l'hydroxyde d'étirement a commencé à être utilisé pour le raffinage de la betterave de la betterave, à travers le processus breveté de Carl Schebler en 1882.
Cette procédure consiste en le mélange d'hydroxyde de strontium et de pulpe sucrée de betterave, ce qui se traduit par un disaccharide insoluble. Cette solution est séparée par décantation et une fois le processus de raffinage effectué, le sucre est obtenu en tant que produit final.
Bien que cette procédure soit encore utilisée, il existe d'autres méthodes avec beaucoup plus de demande pour être moins chère, qui sont utilisées dans la grande majorité des raffineries de sucre mondiales. Par exemple, la méthode Barsil, qui utilise le silicate de baryum, ou la méthode Steffen, en utilisant la chaux comme agent d'extracteur.
Peut vous servir: carbone anomérique: ce qui est, les caractéristiques, les exemplesGraisses de strontium
Ce sont des graisses lubrifiantes qui contiennent de l'hydroxyde de strontium. Ceux-ci sont capables d'adhérer fortement aux surfaces avec des caractéristiques métalliques, sont résistantes à l'eau et de supporter des changements de température soudains.
En raison de leur bonne stabilité physique et chimique, ces graisses sont utilisées comme lubrifiants industriels.
Stabilisateur en plastique
La grande majorité des plastiques, exposés à des facteurs climatiques tels que le soleil, la pluie et l'oxygène atmosphérique, modifier leurs propriétés et dégrader.
En raison de sa résistance considérable à l'eau, l'hydroxyde de strontium est ajouté à ces polymères - pendant la phase de fusion - agissant comme un stabilisateur dans la fabrication de produits en plastique pour prolonger sa durée de vie utile.
Autres applications
- Dans l'industrie de la peinture, il est utilisé comme additif essentiel pour accélérer le processus de séchage dans les peintures commerciales et industrielles.
- D'après l'hydroxyde de strontium, les sels ou les ions strontium sont obtenus, qui sont utilisés comme matière première pour la production d'articles pyrotechniques.
Les références
- Wikipedia (n.d.). Hydroxyde de strontium. Récupéré de.Wikipédia.org
- Pubchem (s.F.). Hydroxyde de strontium. Obtenu à partir de pubchem.NCBI.NLM.NIH.Gouvernement
- Honeywell (s.F.). Hydroxyde de stontium octahydrate. Récupéré de Honeywell.com

