Caractéristiques de la phénylalanine, fonctions, biosynthèse, nourriture
- 1926
- 432
- Adam Mercier
La Phénylalanine (Phe, f) est l'un des 9 acides aminés essentiels, c'est-à-dire qu'il n'est pas synthétisé de manière endogène par le corps humain. Dans sa chaîne latérale, cet acide aminé a un composé aromatique non polaire qui le caractérise.
L'acide propionique phénylalanine, ou β-phényl-α-aminé a été identifié pour la première fois en 1879 par les scientifiques J. H. Schulze et m. Barbieri d'une plante de la famille Fabaceae connue sous le nom Lupinus luteus ou "Altramuz jaune".
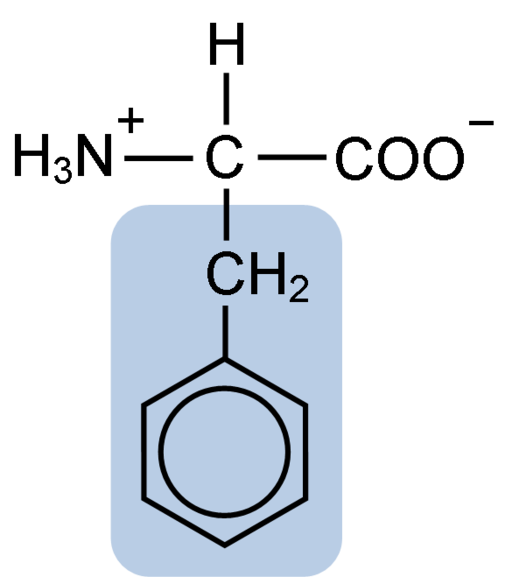
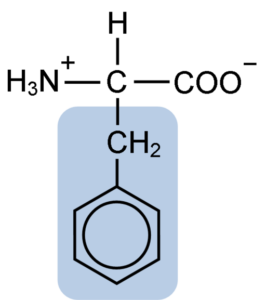 Structure chimique de la phénylalanine des acides aminés (Source: Clavecin [CC BY-SA 4.0 (https: // CreativeCommons.Org / licences / by-sa / 4.0)] via Wikimedia Commons)
Structure chimique de la phénylalanine des acides aminés (Source: Clavecin [CC BY-SA 4.0 (https: // CreativeCommons.Org / licences / by-sa / 4.0)] via Wikimedia Commons) Le dipeptide L-Fenylalanin-L-Aspartil est connu sous le nom d'Aspartame ou "Nutrasweet", qui est un édulcorant produit synthétique et largement utilisé dans les restaurants et les cafés, généralement pour sucrer des boissons telles que le café, le thé, la limonade et d'autres boissons.
Chez les fruits avec des caractéristiques chauffées, la conversion de la L-phénylalanine dans les esters phénoliques tels que l'eugénol et ses dérivés métilaux est ce qui donne naissance à l'odeur florale douce ou similaire au miel typique des bananes et des fruits de bananes lorsqu'il est mature.
Selon la forme, la phénylalanine peut avoir des saveurs différentes. Par exemple, la forme de la L-Fénylalanine a un arôme et une saveur sucrés, tandis que la D-Fénylalanine est légèrement amer et généralement TOOD.
Puisqu'il a un fort caractère hydrophobe, la phénylalanine est l'un des principaux constituants de nombreuses résines dans la nature, comme le polystyrène. Ces résines, lorsqu'ils entrent en contact avec des molécules d'eau, forment une structure de protection ou de couverture appelée "clatrato".
Les gènes qui codent pour la voie de biosynthèse de la phénylalanine sont utilisés par les botanistes comme montres évolutives, car il a été constaté que ceux-ci sont liés à la diversification morphologique des plantes terrestres.
[TOC]
Caractéristiques et structure
La phénylalanine partage tous. De plus, bien sûr, il a une chaîne latérale ou un groupe R caractéristique.
La phénylalanine est l'un des trois acides aminés qui ont des anneaux aromatiques ou benzène comme substituants dans les chaînes latérales. Ces composés ne sont pas polaires et, par conséquent, sont très hydrophobes.
L'acide aminé en question est particulièrement hydrophobe, car, contrairement à la tyrosine et au tryptophane (les deux autres acides aminés avec des anneaux aromatiques) n'a pas de groupes amino ou hydroxyle unis à son anneau de benzène.
Le groupe aromatique, benzoïque ou sandylalanine de phénylalanine a la structure benzène typique: l'anneau cyclique est structuré par 6 atomes de carbone qui ont une résonance entre eux en raison de la présence de trois doubles liaisons et de trois liaisons simples à l'intérieur.
Contrairement à la tyrosine et au tryptophane, qui peuvent acquérir une charge positive et négative, respectivement, la phénylalanine conserve sa charge neutre, car le cycle de benzène n'est pas ionisé et les charges de groupes carboxyle et aminés se neutralisent mutuellement.
Classification
Les acides aminés sont classés en différents groupes en fonction des caractéristiques de leurs chaînes latérales ou de leurs groupes R, car ils peuvent varier en taille, en structure, en groupes fonctionnels et même en charge électrique.
Comme mentionné, la phénylalanine est classée dans le groupe d'acides aminés aromatiques, ainsi que la tyrosine et le tryptophane. Tous ces composés ont des anneaux aromatiques dans leur structure, cependant, la tyrosine et le tryptophane ont des groupes ionisables dans les substituants de leurs groupes R.
Peut vous servir: Spéciation allopatrique: concept, processus et exemplesLes caractéristiques d'absorption de la lumière des protéines à une longueur d'onde de 280 nm sont dues à la présence des acides aminés classés dans le groupe phénylalanine, car ils absorbent facilement la lumière ultraviolette à travers leurs anneaux aromatiques.
Cependant, il a été démontré que la phénylalanine absorbe beaucoup moins que la tyrosine et le tryptophane, donc dans l'analyse de certaines protéines, son absorbance est prévisible.
Stéréochimie
Tous les acides aminés ont un carbone étrange central, qui a quatre atomes ou groupes unis et, comme déjà dit, cet atome est identifié comme le carbone α. Sur la base de ce carbone, au moins deux stéréoisomères de chaque acide aminé peuvent être trouvés.
Les stéréoisomères sont des molécules avec des images spéculaires, qui ont la même formule moléculaire, mais qui ne se chevauchent pas, comme, par exemple, les mains et les pieds. Les composés qui tournent expérimentalement le plan d'éclairage polarisé droit sont indiqués avec la lettre D, et ceux qui le font à gauche, avec la lettre L.
Il est important de dire que la distinction entre les formes de la D-phénylalanine et de la L-Fénylalanine est essentielle pour comprendre le métabolisme de cet acide aminé dans le corps des vertébrés.
La forme de la L-phénylalanine est métabolisée et exploitée pour la construction de protéines cellulaires, tandis que la D-Fénylalanine a été trouvée dans la circulation sanguine en tant qu'agent protecteur contre les espèces réactives de l'oxygène (ROS).
Les fonctions
Dans les années 90, on pensait que la phénylalanine n'était que dans certaines espèces végétales. Cependant, aujourd'hui, il est connu qu'il est présent dans presque tous les domaines hydrophobes des protéines, en fait, la phénylalanine est le principal composant des espèces chimiques aromatiques des protéines.
Chez les plantes, la phénylalanine est un composant essentiel de toutes les protéines; De plus, c'est l'un des précurseurs de métabolites secondaires tels que les phénylpropanoïdes (qui font partie des pigments) des molécules défensives, des flavonoïdes, des biopolymères tels que la lignine et la subérine, entre autres.
La phénylalanine est la structure de base pour former de nombreuses molécules qui maintiennent l'homéostasie neuronale, parmi lesquelles des peptides tels que la vasopressine, la mélanotrophine et l'encéphaline. De plus, cet acide aminé est directement impliqué dans la synthèse de l'hormone adrénocortopique (ACTH).
Comme une grande partie des acides aminés protéiques, la phénylalanine fait partie du groupe des acides aminés cétogènes et glucogéniques, car il fournit le squelette de carbone des intermédiaires du cycle de Krebs, nécessaire au métabolisme énergétique cellulaire et corporel.
En excès, la phénylalanine est transformée en tyrosine et par la suite en fumarate, un intermédiaire du cycle de Krebs.
Biosynthèse
La phénylalanine est l'un des rares acides aminés à ne pas être synthétisé par la plupart des organismes vertébrés. À l'heure actuelle, seules les routes biosynthétiques sont connues pour cet acide aminé dans les organismes procaryotes, dans les levures, dans les plantes et dans certaines espèces de champignons.
Les gènes responsables de la route de synthèse sont très conservés entre les plantes et les micro-organismes, par conséquent, la biosynthèse a des étapes similaires dans presque toutes les espèces. Même certaines enzymes sur l'itinéraire sont présentes chez certains animaux, mais celles-ci ne sont pas en mesure de la synthétiser.
Biosynthèse de la phénylalanine chez les plantes
Chez les espèces végétales, la phénylalanine est synthétisée par une voie métabolique interne dans les chloroplastes appelés "route prédéténat" ". Cette route est métaboliquement liée à "la route Shikimato", à travers le l-arogenato, l'un des métabolites produits au cours de la seconde.
Peut vous servir: topoisomérase: quelles sont les caractéristiques, les fonctions, les typesLes inhydratasa Arewood Enzyme catalysent une réaction à trois étapes, dans laquelle il transforme l'anneau aromatique de l'arogénate en anneau benzénique caractéristique de la phénylalanine.
Cette enzyme catalyse une transamination, une déshydratation et un décarn.
La prédéhéate à côté du phénylpyruvate accumulé à l'intérieur (la lumière) du chloroplaste, peut être convertie en phénylalanine par réaction catalysée par l'enzyme aminotransférase propenato, qui transfère un groupe amino à la phénylpyruvate pour qu'elle soit reconnue par l'arogénat déhydratase et est incorporée à la synthèse de la phénylalanine.
Dans certaines espèces de Pseudomonas Des voies alternatives ont été décrites à celles du Profenato, qui utilisent différentes enzymes mais dont les substrats pour la synthèse de la phénylalanine sont également le prédéténat et l'arogène.
Dégradation
La phénylalanine peut être métabolisée de plusieurs manières à partir de la nourriture. Cependant, la plus grande quantité d'études se concentre sur leur destination sur les cellules du tissu nerveux central et les tissus rénaux.
Le foie est l'organe principal pour la dégradation ou le catabolisme de la phénylalanine. Dans les hépatocytes, il existe une enzyme connue sous le nom d'hydroxylase phénylalanine, capable de transformer la phénylalanine en tyrosine ou dans le composé L-3,4-dihydroxyphénylalanine (L-DOPA).
Le composé L-Dopa est un précurseur de la noradrénaline, de l'épinéphrine et d'autres hormones et des peptides avec une activité dans le système nerveux.
La phénylalanine peut être oxydée dans les cellules cérébrales au moyen de l'enzyme hydroxylase tyrosine, qui est responsable de la catalyse de la conversion de la phénylalanine en dopacrome en présence d'acide l-ascorbique.
Auparavant, on pensait que la tyrosine hydroxylase tyrosine hydroxylase unique.
À l'heure actuelle, il est connu que des proportions élevées de tyrosine inhibent l'activité enzymatique de l'hydroxylase tyrosine, mais la même chose n'est pas vraie pour la phénylalanine.
Aliments riches en phénylalanine
Tous les aliments riches en protéines ont une teneur en phénylalanine entre 400 et 700 mg pour la partie des aliments ingérés. Les aliments tels que l'huile de morue, le thon frais, les homards, les huîtres et autres bivalves contiennent plus de 1.000 mg par portion de nourriture ingérée.
La viande bovine et de porc a également des niveaux élevés de phénylalanine. Cependant, ils ne sont pas aussi élevés que les concentrations présentes chez les animaux marins. Par exemple, le bacon, le bœuf, le foie, le poulet et les produits laitiers ont entre 700 et 900 mg de phénylalanine par ration de nourriture.
Les noix telles que les arachides et les noix de différents types sont d'autres aliments qui ont une bonne quantité de phénylalanine. Les grains tels que le soja, les pois chiches et autres légumineuses peuvent fournir entre 500 et 700 mg de phénylalanine par partie.
En tant que source alternative, la phénylalanine peut être métabolisée à partir d'aspartame.
Avantages de votre apport
La phénylalanine se trouve dans tous les aliments riches en protéines que nous consommons. La consommation quotidienne minimale pour les adultes et la taille moyenne est d'environ 1000 mg, nécessaire à la synthèse des protéines, des hormones telles que la dopamine, de différents neurotransmetteurs, etc.
Il peut vous servir: quelle est la diversité naturelle de la terre?La consommation de cet excès d'acide aminé est prescrite pour les personnes souffrant de troubles dépressifs, de douleurs articulaires et de maladies cutanées, car sa consommation augmente la synthèse des protéines et la transmission de biomolécules telles que l'épinéphrine, la noradéphrine et la dopamine.
Some studies suggest that phenylalanine consumed in excess does not produce significant improvements in any of these disorders, but their conversion into tyrosine, which is also used for the synthesis of signaling molecules, can explain the positive effects on cell signaling in the nervous system in the système nerveux.
Les médicaments formulés contre la constipation ont des noyaux structurés par la phénylalanine, la tyrosine et le tryptophane. Généralement, ces médicaments contiennent des mélanges de ces trois acides aminés sous leurs formes-.
Troubles de la carence
Les niveaux de phénylalanine sanguine sont importants pour maintenir le bon fonctionnement du cerveau, car la phénylalanine, la tyrosine et le tryptophane sont les substrats pour l'assemblage de différents neurotransmetteurs.
Certains troubles se rapportent plutôt avec des déficits dans le métabolisme de cet acide aminé, qui en génère un excès, au lieu d'une carence.
La phénylcétonurie, une maladie héréditaire inhabituelle chez les femmes, affecte l'hydroxylation hépatique de la phénylalanine et rend les niveaux plasmatiques de cet acide aminé excessif, de sorte qu'une apoptose neuronale est induite et affecte le développement normal du cerveau.
Si une femme atteinte de phénylcetonurie tombe enceinte, le fœtus peut présenter ce que l'on appelle le "syndrome fœtal de l'hyperphénylalaninémie maternelle".
En effet, le fœtus a des concentrations élevées de phénylalanine dans le sang (presque le double des normes), dont l'origine est liée à l'absence d'hépatique hydroxylase phénylalanine du fœtus, qui ne se développe pas avant les 26 semaines de gestation.
Le syndrome fœtal par hyperphénylalaninémie maternelle, produit une microcéphalie fœtale, des avortements récurrents, des maladies cardiaques et même des malformations rénales.
Les références
- Biondi, r., Brancorrsini, s., Poli, g., Egidi, m. g., Capodicasa, e., Bottiglieri, L.,… & Micu, R. (2018). Détection et piégeage du radical hydroxyle via une hydroxylation de la D-phénylalanine dans les fluides humains. Talanta, 181, 172-181
- Cho, m. H., Corée, O. R., Yang, H., Bedgar, D. L., Laskar, D. D., Antérola, un. M.,… & Kang, C. (2007). Biosynthèse de la phénylalanine dans Arabidopsis thalien Identification et caractéristique des argenate déshydratas. Journal of Biological Chemistry, 282 (42), 30827-30835.
- Fernstrom, J. D., & Fernstrom, m. H. (2007). Tyrosine, phénylalanine et synthèse et fonction de la cathocholamine dans le cerveau. The Journal of Nutrition, 137 (6), 1539S-1547S.
- Hou, J., Vázquez-González, M., Fadeev, m., Liu, x., Lavi, R., & Willner, je. (2018). Oxydation catalysée et électrocatalysée de la L-tyrosine et de la L-phénylalanine au dopachrome par les nanozymes. Nano Letters, 18 (6), 4015-4022.
- Nelson, D. L., Lehninger, un. L., & Cox, M. M. (2008). Principes de lehninger de la biochimie. Macmillan.
- Perkins, R., & Vaida, V. (2017). La phénylalanine augmente la perméabilité des membranes. Journal of the American Chemical Society, 139 (41), 14388-14391.
- Plimmer, R. H. POUR. (1912). La constitution chimique des protéines (vol. 1). Longmans, vert.
- Tensley, G. (2018). Healthline. Récupéré le 5 septembre 2018 de www.Healthline.com / nutrition / phénylalanine
- Tohge, t., Watanabe, m., Hoefgen, R., & Fernie, à. R. (2013). Biosynthèse shikimate et phénylalanine dans la lignée verte. Frontiers in Plant Science, 4, 62.
- « Caractéristiques d'isoleucine, fonctions, biosynthèse, nourriture
- Caractéristiques du front national, objectifs, présidents »

