Facteur de dilution
- 2092
- 203
- Justine Charpentier
 Dilution en série
Dilution en série Quel est le facteur de dilution?
Il Facteur de dilution (FD) est un nombre qui indique les temps où une solution doit être diluée pour obtenir une concentration plus faible. La solution peut avoir dissous un soluté solide, liquide ou gazeux.
Par conséquent, sa concentration dépend du nombre de particules du soluté et du volume total V.
Dans le domaine de la chimie, de nombreuses expressions de concentration sont utilisées: pourcentage, molaire (m), normal (n), entre autres. Chacun d'eux dépend d'une quantité finie de soluté; Des grammes, des kilogrammes ou des taupes à.
Cependant, lors de la diminution de ces concentrations, la FD s'applique à toutes ces expressions.
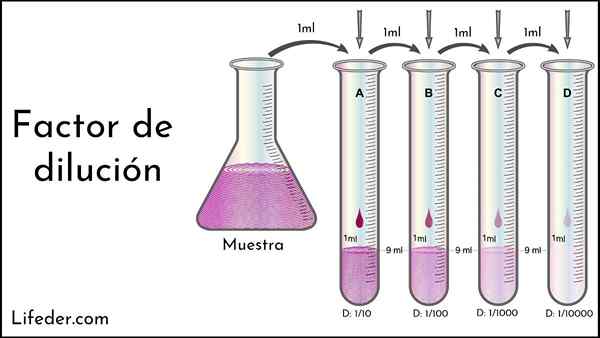
Dans l'image supérieure, il y a un exemple de dilution successive. Notez que de gauche à droite, la couleur violette devient plus claire; qui est égal à une concentration plus faible de l'échantillon.
Le facteur de dilution permet de déterminer à quel point le dernier navire est dilué par rapport à la première. Ainsi, au lieu de propriétés organoleptiques simples, l'expérience peut être répétée à partir du même FD à partir de la même bouteille de solution mère ou d'échantillon, de sorte qu'il est assuré que les concentrations des nouveaux vaisseaux sont égales.
La concentration peut être exprimée dans n'importe quelle unité; Cependant, le volume des vaisseaux est constant et pour faciliter les calculs, il est simplement utilisé aux volumes de l'échantillon dissous dans l'eau. La somme de celles-ci sera égale à V: le volume du liquide total dans le verre.
Comme pour l'exemple d'échantillon, cela se produit en laboratoire avec tout autre réactif. Des solutions concentrées de mères sont préparées, dont les aliquotes sont prises et diluées pour obtenir des solutions plus diluées. Cela cherche à réduire les risques de laboratoire et les pertes de réactifs.
Quel est le facteur de dilution?
Dilution
La dilution est une procédure qui permet une diminution de la concentration d'une solution ou de sa densité. L'action pour réduire l'intensité des couleurs dans une solution de colorant peut également être considérée comme une dilution.
Pour diluer avec succès une solution à une certaine concentration, la première chose qui doit être faite est de savoir combien de fois la concentration de la solution mère est plus élevée par rapport à la concentration de la solution diluée.
Il peut vous servir: dichromate de potassium: formule, propriétés, risques et utilisationsAinsi, les temps où la solution initiale doit être diluée pour obtenir une solution avec la concentration souhaitée. Le nombre de fois est ce que l'on appelle le facteur de dilution. Et cela consiste, dans une fraction sans dimension, qui indique une dilution.
Facteurs
Il est courant de trouver une dilution exprimée, par exemple, comme suit: 1/5, 1/10, 1/100, etc. Cela indique que pour obtenir une solution avec la concentration souhaitée, la solution mère que le dénominateur de la fraction nommée.
Si, par exemple, une dilution 1/5 est utilisée, la solution initiale doit être diluée pour obtenir une solution avec cette concentration 5 fois. Par conséquent, le numéro 5 est le facteur de dilution. Cela se traduit comme suit: La solution 1/5 est cinq fois plus diluée que la mère.
Comment préparer cette solution? Si 1 ml de la solution mère est prise, ce volume doit être quintuple, de sorte que la concentration du soluté est diluée par un facteur 1/5. Ainsi, s'il doit être dilué avec de l'eau (comme dans l'exemple), 1 ml de cette solution doit être ajouté 4 ml d'eau (1 + 4 = 5 ml de volume final VF).
Ensuite, il sera commenté comment déduire et calculer la FD.
Comment obtenir le facteur de dilution?
Déduction
Pour préparer une dilution, une solution initiale ou une mère est emmenée dans un ballon aggravé, où de l'eau est ajoutée pour compléter la capacité de mesure du ballon susmentionné.
Dans ce cas, lorsque de l'eau est ajoutée au ballon agricole, la masse du soluté n'est pas ajoutée. Ensuite, la masse de soluté ou la solution reste constante:
mToi = mF (1)
mToi = masse du soluté initial (dans la solution concentrée).
Et MF = masse du soluté final (dans la solution diluée).
Mais, m = v x c. Remplacement dans l'équation (1), vous avez:
VToi x cToi = VF x cF (2)
VToi = volume de la mère ou une solution initiale qui a été prise pour dilution.
CToi = concentration de la mère ou solution initiale.
VF = volume de la solution diluée qui a été préparée.
CF = concentration de la solution diluée.
L'équation 2 peut être écrite comme suit:
CToi / CF = VF / VToi (3)
Deux expressions valides pour FD
Mais cToi / CF Par définition est le Facteur de dilution, car il indique les temps où la concentration de la mère ou de la solution initiale est plus élevée par rapport à la concentration de la solution diluée.
Par conséquent, indique la dilution à effectuer pour préparer la solution diluée à partir de la solution mère.
Peut vous servir: eau distilléeDe même, d'après l'observation de l'équation 3, on peut conclure que la relation VF / VToi C'est une autre façon d'obtenir le Facteur de dilution. C'est-à-dire que l'une des deux expressions (cToi/ CF, VF/ VToi) sont valables pour calculer le FD. L'utilisation de l'une ou de l'autre dépendra des données disponibles.
Exemples
Exemple 1
Une solution de NaCl de 0,3 m a été utilisée pour préparer une solution diluée de 0,015 m. Calculez la valeur du facteur de dilution.
Le facteur de dilution est de 20. Cela indique que pour préparer la solution diluée de NaCl 0,015 m, la solution de NaCl de 0,3 m a dû être diluée 20 fois:
Fd = cToi / CF
0,3 m / 0,015 m
vingt
Exemple 2
Sachant que le facteur de dilution est de 15: quel volume d'eau doit être ajouté à 5 ml d'une solution de glucose concentrée pour faire la dilution souhaitée?
Comme première étape, le volume de la solution diluée est calculé (vF). Une fois calculé, le volume d'eau ajouté est calculé pour faire la dilution.
FD = VF / VToi.
VF = Fd x vToi
15 x 5 ml
75 ml
Volume d'eau ajouté = 75 ml - 5 ml
70 ml
Ensuite, pour préparer la solution diluée avec un facteur de dilution de 15, 5 ml de la solution concentrée, 70 ml d'eau ont été ajoutés pour compléter le volume final de 75 ml.
Exemple 3
La concentration d'une solution de mère fructose est de 10 g / L. Il est souhaité en préparer une solution de fructose avec une concentration de 0,5 mg / ml. Prendre de la solution mère de 20 ml à la dilution: quel devrait être le volume de la solution diluée?
La première étape pour résoudre le problème consiste à calculer le facteur de dilution (FD). Une fois obtenu, le volume de la solution diluée sera calculé (vF).
Mais avant de faire le calcul augmenté, il est nécessaire de faire l'observation suivante: vous devez placer les quantités de concentrations de fructose dans les mêmes unités. Dans ce cas particulier, 10 g / L équivalent à 10 mg / ml, illustrant cette situation à travers la transformation suivante:
(mg / ml) = (g / l) x (1.000 mg / g) x (L / 1.000 ml)
Donc:
10 g / L = 10 mg / ml
Continue avec les calculs:
Peut vous servir: aminesFd = cToi / CF
FD = (10 mg / ml) / (0,2 mg / ml)
cinquante
Mais comme VF = Fd x vToi
VF = 50 x 20 ml
1.000 ml
Ainsi, 20 ml de la solution de fructose de 10 g / L, 1 L.
Exemple 4
Une méthode pour faire des dilutions en série sera illustrée. Il existe une solution de glucose avec une concentration de 32 mg / 100 ml, et à partir de celui-ci, il est souhaité / 100 ml, 2 mg / 100 ml et 1 mg / 100 ml.
Procédure
5 tubes à essai sont étiquetés pour chacune des concentrations indiquées dans l'instruction. Dans chacun, 2 ml d'eau sont placés, par exemple.
Ensuite, au tube 1 avec de l'eau, 2 ml de la solution mère sont ajoutés. Le contenu du tube 1 est agité et 2 ml de son contenu est transféré dans le tube 2. À son tour, le tube 2 est agité et 2 ml de son contenu sont transférés dans le tube 3; procéder de la même manière avec les tubes 4 et 5.
Explication
Au tube 1 sont ajoutés 2 ml d'eau et 2 ml de la solution mère avec une concentration de glucose de 32 mg / 100 ml. La concentration finale du glucose dans ce tube est donc de 16 de mg / 100 ml.
Au tube 2 sont ajoutés 2 ml d'eau et 2 ml de la teneur en tube 1 avec une concentration de glucose de 16 mg / 100 ml. Ensuite, dans le tube 2, la concentration du tube 1 est diluée 2 fois (FD). Ainsi, la concentration finale de glucose dans ce tube est de 8 mg / 100 ml.
Au tube 3 2 ml d'eau et 2 ml de teneur en tube 2 sont ajoutés, avec une concentration de glucose de 8 mg / 100 ml. Et comme les deux autres tubes, la concentration est divisée en deux: 4 mg / 100 ml de glucose dans le tube 3.
Pour la raison expliquée ci-dessus, la concentration finale de glucose dans les tubes 4 et 5 est, respectivement, 2 mg / 100 ml et 1 mg / 100 ml.
La FD des tubes 1, 2, 3, 4 et 5, par rapport à la solution mère, est: 2, 4, 8, 16 et 32, respectivement.
Les références
- Aus et tute. (s.F). Calculs du facteur de dilution. Pris de: AUSETUT.com.Au
- J.T. (s.F.). Facteur de dilution. [PDF]. Pris de: CSUS.Édu
- Aide des dilutions (s.F.). Pris de: uregina.CA
- Joshua (2011). Différence entre la dilution et le facteur de dilution. Différence entre.filet. Récupéré de: différence entre les deux.filet
- Whitten, Davis, Peck & Stanley. Chimie (8e Ed.). Cengage Learning.
- Innovarte (2014). Dilutions en série. Récupéré de: 3.Uah.est

