Concept d'électrolyte fort, caractéristiques, exemples

- 2213
- 133
- Adam Mercier
UN Électrolyte fort C'est toute cette substance qui s'est dissoute dans l'eau, ou dans un solvant spécifique, est complètement dissociée sur les ions. Par conséquent, il ne devrait pas y avoir de solution sous forme de molécules neutres, ou comme des solides insolubles. Un électrolyte fort peut être un sel, un acide ou une base, à condition qu'ils se dissocient ou complètement ioniques.
L'exemple le plus représentatif d'un électrolyte est le sel commun, le chlorure de sodium, le NaCl. En solution aqueuse, les cristaux de NaCl se dissocient dans leur intégralité pour produire+ et cl-, qui finissent par les molécules d'eau environnantes. On dit ensuite qu'un sel se comporte comme un électrolyte fort lorsque sa solubilité est très élevée dans l'eau.
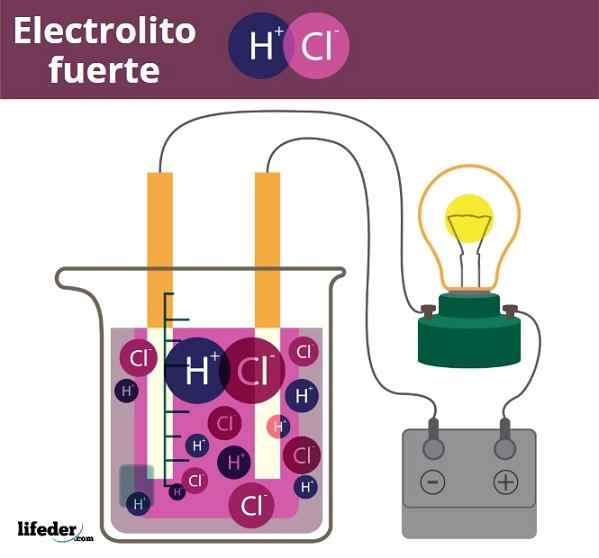 Exemple d'électrolite FUERO. HCl, acide chlorhydrique, libérez H3O + et CL ions-
Exemple d'électrolite FUERO. HCl, acide chlorhydrique, libérez H3O + et CL ions- Un peu similaire est le cas des acides et des bases. Lorsque ceux-ci sont forts, leurs solutions dans l'eau produisent la quantité maximale possible d'ions H3SOIT+ ou oh-, Les changements de pH sont donc brusques. Des exemples d'acides et de bases forts sont l'acide nitrique, HNO3, et hydroxyde de potassium, KOH, respectivement.
Il est important de savoir comment identifier des électrolytes forts lors de la préparation des solutions très ioniques, ou des moyens très forts ou de base.
[TOC]
Caractéristiques des électrolytes forts
Solubilité
Les électrolytes forts se caractérisent par des substances d'eau extrêmement solubles. Qu'il soit solide ou gaz. Si un sel, par exemple, est peu soluble dans l'eau, peut être jeté comme un électrolyte fort.
Conductivité ionique
Les électrolytes forts sont non seulement très solubles dans l'eau, mais génèrent également un grand nombre d'ions. Grâce aux charges électriques de ces ions, les électrons peuvent parcourir confortablement les solutions. Cela se reflète dans une augmentation de la conductivité ionique en ce qui concerne l'eau pure. C'est pourquoi les solutions ioniques mènent très bien l'électricité.
Peut vous servir: chlore: histoire, propriétés, structure, risques, utilisationsNeutralité saline
De nombreux électrolytes forts salins, lors de la dissolution dans l'eau, ne produisent aucun changement de pH. Cela signifie que les solutions de ces sels ne sont ni acides ni basiques, mais neutres, avec un pH proche de 7.
Cependant, il peut y avoir des sels d'acide ou de base qui sont facilement dissous dans l'eau, et qui génèrent également des ions complets. Par exemple, carbonate de sodium2CO3, se dissout pour générer des ions NA+ et Cie32-, Mais le pH de la solution est basique.
Exemples d'électrolytes forts
 Le chlorure de sodium est l'exemple le plus représentatif d'un électrolyte fort. Source: Cristian V. / Cc by-sa (https: // creveVecommons.Org / licences / by-sa / 4.0)
Le chlorure de sodium est l'exemple le plus représentatif d'un électrolyte fort. Source: Cristian V. / Cc by-sa (https: // creveVecommons.Org / licences / by-sa / 4.0) Les électrolytes forts, en étant tant, sont divisés en trois classifications: des acides forts, des bases fortes et un produit de sels solubles de neutralisations entre les deux premiers.
Acides forts
Les acides forts lors de la dissolution dans l'eau, sans aucun problème, doivent produire la quantité maximale possible de H3SOIT+, L'acide doit donc être complètement ionique; c'est-à-dire qu'il ne devrait pas exister en tant que molécule neutre avec des protons acides sans libérer.
Des exemples de ces acides sont:
-HCl, acide chlorhydrique, libère des ions H3SOIT+ et cl-
-HF, acide fluorhorique, libère des ions H3SOIT+ et f-
-HNO3, Acide nitrique, libérer les tonnes h3SOIT+ et non3-
-Hclo4, acide perclorique, libère les ions h3SOIT+ et Clo4-
-Hio4, acide périódique, libère des ions h3SOIT+ et Io4-
-H2Swin4, acide sulfurique, libérer les tonnes h3SOIT+ Et ainsi42-
La raison pour laquelle l'ion hydrum, h3SOIT+, Il est toujours présent (d'une manière ou d'une autre), c'est parce que l'hydrogène qu'ils donnent est reçu par une molécule d'eau:
HCL + H2O → H3SOIT+ + CL-
La réaction est directe et irréversible. Ceci est une caractéristique d'un acide fort, qui à son tour est un électrolyte fort en raison de son ionisation complète dans l'eau.
Peut vous servir: hydrocarbures aliphatiques: propriétés, nomenclature, réactions, typesBases fortes
Bases fortes, dissolvant dans l'eau sans aucun problème, doit libérer les ions OH- à partir des mêmes cristaux, ou irréversiblement une malfratie une molécule d'eau pour les générer.
De nombreuses bases fortes sont constituées d'ions et de solides non moléculaires. Quelques exemples de ces bases qui se comportent comme des électrolytes forts sont:
-Lioh, hydroxyde de lithium, libère des ions oh- et li+
-NaOH, hydroxyde de sodium, libère des ions OH- et na+
-RBOH, Rubidio Hydroxyde, libère des ions OH- et RB+
-Ca (oh)2, Hydroxyde de calcium, libèrez des ions OH- et CA2+
-SR (OH)2, Hydroxyde de strontium, libérez les ions OH- et M2+
-Ba (oh)2, hydroxyde de baryum, libérer des ions oh- et ba2+
-Non, l'hydrure de sodium, libère des ions oh- et l'hydrogène gazeux, h2
-Nanh2, sodium amiduro, libérer les ions oh- et gaz d'ammoniac, NH3
Vous sortez
Les électrolytes forts hallobasi lors de la dissolution dans l'eau doivent être complètement ioniques. Beaucoup d'entre eux ne produisent pas de changements de pH. En effet, leurs ions sont très stables, donc ils ne participent pas aux soldes d'hydrolyse pour changer la nature. Des exemples de ces sels sont:
-NaCl, chlorure de sodium, libère des ions na+ et cl-
-Agno3, Nitrate d'argent, libérez les ions AG+ et non3-
-Grand frère3, nitrate de sodium, libèrez des ions NA+ et non3-
-K2Swin4, sulfate de potassium, libère des ions+ Et ainsi42-
-MGCL2, Chlorure de magnésium, libère des ions Mg2+ et cl-
-Cuso4, Sulfate cuprique, libère les ions Cu2+ Et ainsi42-
-KBR, bromure de potassium, libère des ions k+ et br-
-NH4Cl, chlorure d'ammonium, libère des ions NH4+, CL-, H3SOIT+ et gaz d'ammoniac
Il peut vous servir: Chlorure de mercure (ii): structure, propriétés, obtention, utilisations-NACN, cyanure de sodium, libère des ions na+ et CN-
-N / A3Pote4, phosphate de sodium, libère des ions na+ et po43-
-CRCL3, Chlorure chromique, libère des ions3+ et cl-
-Aub3, Bromide aurique, libère des ions au3+ et br-
-Snso4, Estany sulfate, libère les ions sn2+ Et ainsi42-
Le NH4Cl est un exemple contradictoire: il est complètement ionisé, mais en même temps, il génère des molécules neutres d'ammoniac car c'est un sel acide.
Différences entre électrolyte fort et faible
Bien que les différences entre un électrolyte fort d'un faible aient été établie indirectement, celles-ci seront présentées ci-dessous comme une conclusion:
-Les électrolytes forts sont très solubles dans les eaux; Les électrolytes faibles ne sont pas.
-L'ionisation d'un électrolyte faible est partielle, ce qui signifie qu'il peut y avoir des molécules neutres en solution. Au lieu de cela, des électrolytes forts existent exclusivement sous forme d'ions.
-Les acides et bases faibles, qui à leur tour sont des électrolytes faibles, ne se dissocient pas complètement dans l'eau, de sorte qu'ils génèrent moins d'ions h3SOIT+ ou oh- Que pourrait être attendu.
-HALTH -HALIN Les électrolytes forts ne sont presque pas hydrolysés par rapport aux électrolytes faibles. Par conséquent, les solutions des premiers ont tendance à être neutres, sauf lorsqu'elles traitent des sels acides ou de base.
Les références
- Whitten, Davis, Peck & Stanley. (2008). Chimie. (8e Ed.). Cengage Learning.
- Fhiver & Atkins. (2008). Chimie inorganique. (Quatrième édition). Mc Graw Hill.
- Wikipédia. (2020). Électrolyte fort. Récupéré de: dans.Wikipédia.org
- Helmestine, Anne Marie, Ph.D. (11 février 2020). Définition et exemple d'électrolyte solide. Récupéré de: Thoughtco.com
- Chung & Chieh. (5 juin 2019). Électrolytes. CHIMISTER BOOLISTexts. Récupéré de: Chem.Bibliothèque.org
- « Caractéristiques d'évaluation externes, types (tests), exemples
- Platon Biographie, philosophie et contributions »

