Caractéristiques de la Valine, fonctions, aliments riches, avantages
- 979
- 172
- Mlle Ambre Dumont
La Valina Il appartient aux 22 acides aminés identifiés comme les composants "de base" des protéines; Il est identifié avec l'acronyme "Val" et avec la lettre "V". Cet acide aminé ne peut pas être synthétisé par le corps humain, par conséquent, il est catalogué dans le groupe de neuf acides aminés essentiels pour l'homme.
De nombreuses protéines globulaires ont un intérieur riche en déchets de valine et de leucine, car les deux sont associés à des interactions hydrophobes et sont indispensables pour le repliement de la structure et la conformation à trois dimensions des protéines.
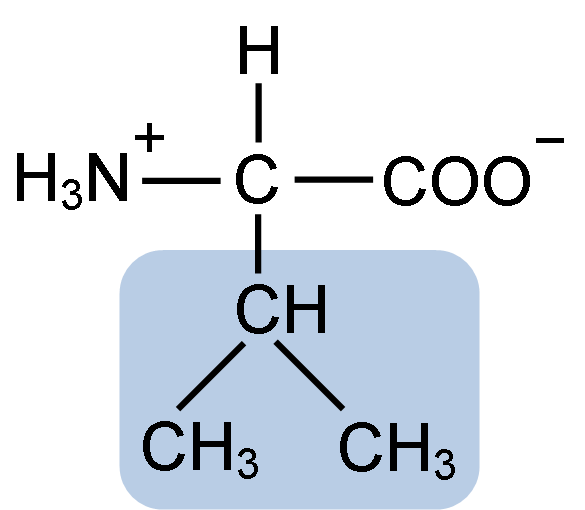
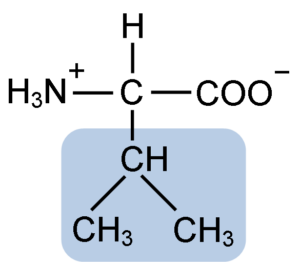 Structure chimique de la valine d'acide aminé (source: clavecine [CC BY-SA 4.0 (https: // CreativeCommons.Org / licences / by-sa / 4.0)] via Wikimedia Commons)
Structure chimique de la valine d'acide aminé (source: clavecine [CC BY-SA 4.0 (https: // CreativeCommons.Org / licences / by-sa / 4.0)] via Wikimedia Commons) La Valina a été purifiée pour la première fois en 1856 par V. Grup-Besanez à partir d'un extrait aqueux du pancréas. Cependant, le nom "Valina" a été inventé par E. Fisher en 1906, lorsqu'il a réussi à le synthétiser artificiellement et a observé que sa structure était très similaire à celle de l'acide valorant, trouvée dans les plantes communément appelées "valérites".
La valine est l'un des acides aminés trouvés dans les positions conservées dans certaines protéines partagées par les vertébrés, par exemple, dans la position 80 du cytochrome c des vertébrés, la leucine, la valine, l'isoleucine et la méthodine dans le même ordre dans le même ordre.
Dans les tissus ou les biomatériaux avec des caractéristiques résistantes, dures et élastiques telles que les ligaments, les tendons, les vaisseaux sanguins, les fils ou les web, il existe de grandes quantités de valine, qui offre une flexibilité et une résistance grâce à ses interactions hydrophobes avec d'autres acides aminés.
Remplacement d'un résidu de glutamate par l'un de Valine dans la chaîne β de l'hémoglobine, la protéine responsable du transport de l'oxygène par le sang provoque une mauvaise formation dans la structure des protéines, qui provoque l'hémoglobine "S".
Cette mutation produit une anémie falciforme ou une drepanocytose, une affection pathologique dans laquelle les globules rouges acquièrent une forme de croissant ou de caractéristique Hoz, qui les différencie de l'apparence normale, arrondie et aplatie.
Certains des herbicides les plus utilisés ont actuellement des composés actifs de la sulfonylurée et du méthyl sulfomètre, qui endommagent l'enzyme acétolactate synthase, nécessaire pour la première étape de la synthèse de la valine, de la leucine et de l'isoleucine. Les dommages causés par ces pesticides empêchent les herbes et les mauvaises herbes peuvent normalement se développer.
[TOC]
Caractéristiques
Valina est un acide aminé avec un squelette à cinq carbone et appartient au groupe d'acides aminés avec des chaînes latérales aliphatiques. Son caractère hydrophobe est tel qu'il peut être comparé à celui de la phénylalanine, celui de la leucine et celui de l'isoleucine.
Les acides aminés qui ont des chaînes d'hydrocarbures dans leurs chaînes R R ou latérales sont communément connues en bibliographie sous le nom d'acides aminés à chaîne ramifiée ou ramifiée. Dans ce groupe se trouvent la valine, la phénylalanine, la leucine et l'isoleucine.
Généralement, les acides aminés de ce groupe sont utilisés comme éléments structurels internes dans la synthèse des protéines, car ceux-ci peuvent être associés les uns aux autres par le biais d'interactions hydrophobes, "fuyant" l'eau et établissant le repliement structurel caractéristique de nombreuses protéines.
Son poids moléculaire est d'environ 117 g / mol et, comme son groupe de chaîne R ou latérale est un hydrocarbure ramifié, il n'a pas de charge et que son abondance relative dans les structures protéiques est peu supérieure à 6%.
Structure
La Valina partage la structure générale et les trois groupes chimiques typiques de tous les acides aminés: le groupe carboxyle (COOH), le groupe amino (NH2) et un atome d'hydrogène (-H). Dans son groupe de chaîne R ou latérale, il a trois atomes de carbone qui lui donnent des caractéristiques très hydrophobes.
Peut vous servir: êtres inertes: caractéristiques, exemples, différences avec les êtres vivantsComme c'est vrai pour tous les composés chimiques classés comme "acides aminés", la valine a un atome de carbone central qui est chiral et qui est connu sous le nom de carbone α, auquel les quatre groupes chimiques mentionnés.
Le nom IUPAC de la Valine est 2-3-amino-3-butanóic.
Tous les acides aminés peuvent être trouvés sous la forme D ou L et la valine ne fait pas exception. Cependant, la forme de valeur L est beaucoup plus abondante que la forme d-valléine et, en outre, elle est spectroscopiquement plus active que la forme d.
La valeur en L est la forme utilisée pour la formation de protéines cellulaires et est donc, des deux, la forme biologiquement active. Il remplit des fonctions telles que le nutraceutique, le micronutriment pour les plantes, le métabolite pour l'homme, les algues, les levures et les bactéries, entre autres fonctions.
Les fonctions
Valina, bien qu'il soit l'un des neuf acides aminés essentiels, ne joue pas de rôle supplémentaire dans sa participation à la synthèse des protéines et en tant que métabolite dans sa propre voie de dégradation.
Cependant, les acides aminés volumineux tels que la valine et la tyrosine sont responsables de la flexibilité des fibroine, la principale composante protéique des fils de soie produites par l'espèce de l'espèce Bombyx Mori, communément appelés vers de soie ou de mûrier.
Les tissus tels que les ligaments et les verres de sang artériel sont composés d'une protéine fibreuse connue sous le nom d'élastine. Cela se compose de chaînes polypeptidiques avec des séquences répétées de glycine, d'aliéments d'alanine et de valine, le résidu le plus important avec des protéines.
Valina participe aux principales routes de synthèse des composés responsables de l'odeur caractéristique des fruits. Les molécules de valine sont transformées en dérivés méthylés et ramifiés d'esters et d'alcools.
Dans l'industrie alimentaire
Il existe de nombreux additifs chimiques qui utilisent la valine en combinaison avec le glucose pour obtenir des odeurs appétissantes dans certaines préparations culinaires.
À une température de 100 ° C, ces additifs ont une odeur de seigle caractéristique et plus de 170 ° C dans le chocolat chaud, ils sont donc populaires dans la production alimentaire dans l'industrie du boulanger et de la pâtisserie (pâtisserie).
Ces additifs chimiques utilisent la L-Valin synthétisée artificiellement.
Biosynthèse
Tous les acides aminés de chaîne ramifiés tels que la valine, la leucine et l'isoleucine sont principalement synthétisés dans les plantes et les bactéries. Ce qui signifie que les animaux comme l'être humain et les autres mammifères doivent ingérer des aliments riches en ces acides aminés pour pouvoir répondre à leurs besoins nutritionnels.
Habituellement, la biosynthèse de la valine commence par le transfert de deux atomes de carbone du pyrophosphate d'hydroxyéthyl-tyamine au pyruvate par l'action de l'acide enzymatique acide à l'acide réductase d'acide isomère réduct.
Les deux atomes de carbone dérivent d'une seconde molécule de pyruvate par une réaction dépendante du TPP très similaire à celle catalysée par l'enzyme pyruvate de discarboxylase, mais qui est catalysée par la dihydroxy-acide déshydratase.
L'enzyme valine aminotransférase, enfin, intègre un groupe amino au composé cétoacide résultant de la décarboxylation antérieure, qui forme la L-Valine. Les acides aminés de leucine, de l'isoleucine et de la valine ont une grande similitude structurelle, et c'est parce que de nombreux intermédiaires et enzymes partagent sur leurs voies biosynthétiques.
Il peut vous servir: flore et faune de sala: espèces plus représentativesLe cétoacide produit pendant la biosynthèse de la L-Valine régule certaines étapes enzymatiques par une rétroaction négative ou une régulation alostérique sur la voie biosynthétique de la leucine et d'autres acides aminés apparentés.
Cela signifie que les routes biosynthétiques sont inhibées par un métabolite généré en eux qui, lorsqu'il est accumulé, donne aux cellules un signal spécifique qui leur dit qu'un certain acide aminé est excessivement et que sa synthèse peut donc arrêter.
Dégradation
Les trois premières étapes de dégradation de la valine sont partagées sur la voie de dégradation de tous les acides aminés de chaîne ramifiée.
Valina peut entrer dans le cycle de l'acide citrique Krebs à transformer en succinyl-CoA. La route de dégradation est constituée d'une transamination initiale, catalysée par une enzyme connue sous le nom d'aminotransférase des acides aminés à chaîne ramifiée (BCAT).
Cette enzyme catalyse une transamination réversible qui parvient à convertir les acides aminés de la chaîne ramifiée en leur chaîne ramifiée correspondante α-zo-pivoles.
Dans cette réaction, la participation du couple de glutamate / 2-zotoglutarate est essentielle, car le 2-zotoglutarate reçoit le groupe amino qui est retiré de l'acide aminé qui est métabolisé et devient glutamate.
Cette première étape de réaction du catabolisme de la Valine produit le 2-Céthoisavalerate et s'accompagne de la conversion du pyridoxal 5'-phosphate (PLP) dans la pyridoxamine 5'-phosphate (PMP).
Ensuite, le 2-Céthoisvalate est utilisé comme substrat d'un complexe enzymatique mitochondrial, appelé α-α-zo-stare de chaîne ramifiée, qui ajoute une partie coash et forme l'isobutiril-coa, qui est censée déshydrogéné et transformée en métacrililille, qui est ensuite déshydrogénée et transformée en métacrililille, -Coa.
Le méthacrylil-CoA est traité en aval dans 5 étapes enzymatiques supplémentaires qui impliquent l'hydratation, l'élimination de la partie coash, l'oxydation, l'ajout d'une autre partie Coash et la réorganisation moléculaire, qui se terminent par la production de succinyl-CoA, qui entre immédiatement dans le cycle de Krebs.
Aliments riches en Valina
Les protéines contenues dans les graines de sésame ou de sésame sont riches en valine, avec près de 60 mg d'acide aminé pour chaque gramme de protéines. Pour cette raison, les biscuits, les biscuits et les barres de sésame ou Nougat sont recommandés pour les enfants ayant une alimentation déficiente de cet acide aminé.
Les grains de soja, en général, sont riches en tous les acides aminés essentiels, même à Valina. Cependant, ils sont pauvres en métitionne et en cystéine. La protéine ou la texturation du soja a des structures quaternaires très complexes, mais qui sont faciles à dissoudre et à séparer en sous-unités plus petites en présence de jus gastriques.
La caséine, qui est généralement dans le lait et ses dérivés, est riche en séquences répétées de valine. Comme le soja, cette protéine est facilement dégradée et absorbée dans le tractus intestinal des mammifères.
Il a été estimé que pour 100 grammes de protéines de soja, environ 4,9 grammes de valine sont ingérés; Tandis que pour 100 ml de lait, environ 4,6 ml de Valina sont ingérés.
D'autres aliments riches dans lesdits acides aminés sont le bœuf, le poisson et divers types de légumes et de légumes.
Avantages de votre apport
La valine, comme une grande partie des acides aminés, est un acide aminé glycogène, c'est-à-dire qu'il peut être incorporé dans la voie gluconéogène, et de nombreux neurologues affirment que leur apport aide à maintenir la santé mentale, la coordination musculaire et réduire le stress.
Peut vous servir: les 5 branches de la biotechnologie principaleDe nombreux athlètes consomment comprimé comprimé à Valina, car ils aident la régénération des tissus, en particulier les tissus musculaires. Être un acide aminé capable de rejoindre la gluconéogenèse aide la production d'énergie, ce qui est non seulement important pour l'activité physique mais pour le fonctionnement nerveux.
Les aliments Valina aident à maintenir l'équilibre des composés d'azote dans le corps. Cet équilibre est essentiel pour la production d'énergie à partir des protéines ingérées, pour la croissance corporelle et la guérison.
Sa consommation empêche les dommages au foie et à la vésicule biliaire, et contribue à l'optimisation de nombreuses fonctions corporelles.
L'un des compléments alimentaires les plus populaires entre les athlètes pour augmenter le volume musculaire et la récupération musculaire est le BCAA.
Ces types de comprimés sont constitués de comprimés avec des mélanges de différents acides aminés parmi lesquels sont généralement inclus des acides aminés tels que la L-Valine, la L-isoleucine et la L-leucina; Ils sont également riches en vitamine B12 et autres vitamines.
Certaines expériences avec des porcs ont montré que les exigences de valine sont beaucoup plus élevées et plus limitantes pour les mères pendant le stade de l'allaitement, car cet acide aminé aide à sécréter le lait et produit des améliorations du taux de croissance des nouveau-nés pour nourrissons.
Troubles de la carence
L'apport quotidien de valine recommandé pour les nourrissons est d'environ 35 mg pour chaque gramme de protéines consommé, tandis que pour les adultes, la quantité est un peu plus faible (environ 13 mg).
La maladie la plus courante liée à la valine et à d'autres acides aminés de la chaîne ramifiée est connue sous le nom de «maladie urinaire avec sirop ARCE» ou «kétoaciduria».
Il s'agit d'une condition héréditaire causée par un défaut des gènes qui codent pour les enzymes déshydrogènes des α-zo-acides dérivées de la leucine, de l'isoleucine et de la valine, qui sont nécessaires pour les métaboliser.
Dans cette maladie, l'organisme ne peut assimiler aucun de ces trois acides aminés lorsqu'ils sont obtenus à partir de l'alimentation, par conséquent, les cétoacides dérivés s'accumulent et sont expulsés dans l'urine (ils peuvent également être détectés dans le sérum sanguin et dans le liquide céphalorachique).
D'un autre côté, une mauvaise alimentation à Valina a été liée à des pathologies neurologiques telles que l'épilepsie. Il peut également entraîner une perte de poids, la maladie de Huntington et peut même se retrouver dans le développement de certains types de cancer, car le système de réparation des tissus et la synthèse des biomolécules sont compromis.
Les références
- Abu-Baker, S. (2015). Revue de la biochimie: concepts et connexions
- Nelson, D. L., Lehninger, un. L., & Cox, M. M. (2008). Principes de lehninger de la biochimie. Macmillan.
- Plimmer, R. H. POUR., & Phillips, H. (1924). L'analyse des protéines. III. Estimation de l'histidine et de la tyrosine par bomination. Journal biochimique, 18 (2), 312
- Plimmer, R. H. POUR. (1912). La constitution chimique des protéines (vol. 1). Longmans, vert.
- Torii, k. POUR. Z. OU. SOIT., & Iitaka, et. (1970). La structure cristalline de la L-Valine. Crystallographica Section B: Crystallographie structurale et chimie cristalline, 26 (9), 1317-1326.
- Tosti, V., Bertozzi, b., & Fontana, L. (2017). Avantages pour la santé du régime méditerranéen: mécanismes métaboliques et moléculaires. The Journals of Gerontology: Series A, 73 (3), 318-326.
- « Formules d'énergie gravitationnelles, caractéristiques, applications, exercices
- Les 115 meilleures phrases sur l'élégance »

