Trioxyde d'arsenic (AS2O3)
- 4479
- 10
- Eva Henry
Il trioxyde d'arsenic C'est un composé inorganique dont la formule chimique est ainsi2SOIT3. L'arsenic dans son état métallique est rapidement transformé en cet oxyde, qui est un poison très toxique qui peut avoir des manifestations aiguës et chroniques.
Étant des éléments d'arsenic et d'oxygène du bloc P, avec une différence d'électronégativité relativement faible, l'ACE est attendue2SOIT3 être composé de nature covalente; c'est-à-dire que les liaisons AS-O prédominent dans leurs interactions solides, sur les interactions électrostatiques entre les ions ACE3+ je2-.
Un empoisonnement aigu avec un trioxyde d'arsenic est produit par l'admission ou l'inhalation, étant les manifestations les plus importantes de ceci: de forts troubles gastro-intestinaux, des crampes, un effondrement circulatoire et un œdème pulmonaire.
Cependant, malgré sa toxicité, il a été utilisé industriellement; Par exemple, dans la conservation du bois, dans l'élaboration des pigments, des semi-conducteurs, etc. De même, il a été autrefois utilisé dans le traitement de nombreuses maladies.
Le trioxyde d'arsenic est un composé amphotérique, soluble dans les acides et les alcalis dilués, insoluble dans les solvants organiques et relativement soluble dans l'eau. Il est présenté comme une solide (image supérieure), avec deux formes cristallines: cubique et monoclinique.
Structure du trioxyde d'arsenic
Claudetita
À température ambiante, l'as2SOIT3 Cristallise dans deux polymorphes monocliniques, tous deux trouvés dans le minéral Claudetita. Il y a des unités de pyramide trigonale ASO3, qui se lient par leurs atomes d'oxygène pour compenser la carence électronique de l'unité seule.
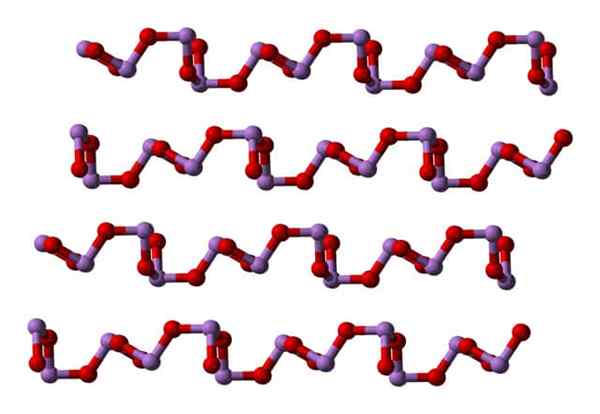
Dans un polymorphe les unités ASO3 Ils sont liés à former des lignes (Claudetita I), et dans l'autre, ils sont liés comme s'ils tissaient un réseau (Claudetita II):
Peut vous servir: matériaux agglomérants Claudetita Polymorfo Structure I. Source: Ben Mills [domaine public].
Claudetita Polymorfo Structure I. Source: Ben Mills [domaine public].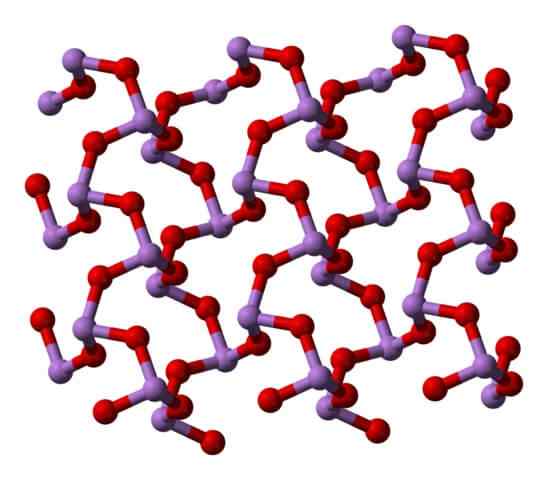 Claudetita Polymorfo Structure II. Source: Ben Mills [domaine public].
Claudetita Polymorfo Structure II. Source: Ben Mills [domaine public].
Liquide et gazeux
Lorsque toutes ces structures qui définissent les cristaux monocliniques sont chauffés, les vibrations sont telles que plusieurs liaisons telles que sont brisées et finissent par râler une molécule plus petite:4SOIT6. Dans l'image inférieure, sa structure est montrée.
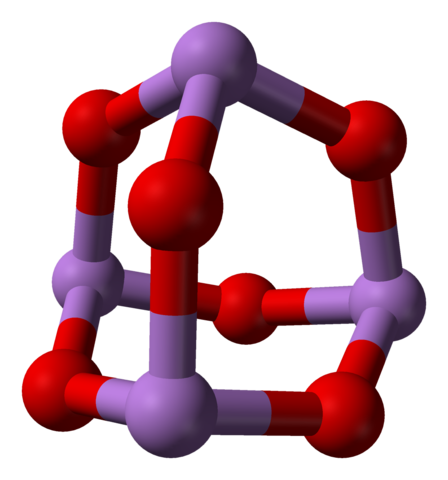 Molécule AS4O6. Source: Ben Mills [domaine public]
Molécule AS4O6. Source: Ben Mills [domaine public] On pourrait dire qu'il se compose d'un jour de As2SOIT3. Sa stabilité est telle qu'elle prend en charge 800 ° C dans une phase gazeuse; Mais, au-dessus de cette température, il est fragmenté sous forme de molécules2SOIT3.
Arsénolite
Le même que4SOIT6 peut interagir les uns avec les autres pour cristalliser dans un solide cube, dont la structure se trouve dans le minéral arsénolite.
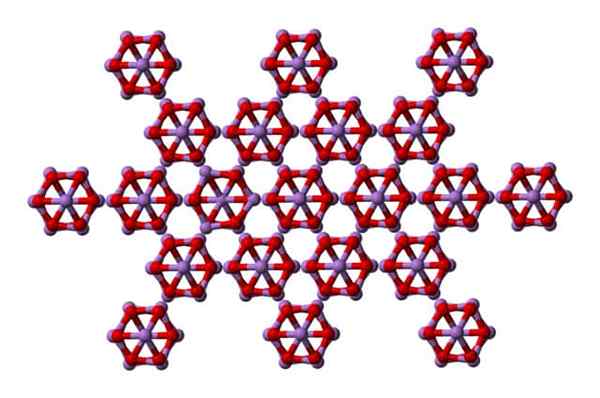 Molécules AS4O6 dans le solide arsénolite. Source: Ben Mills [domaine public]
Molécules AS4O6 dans le solide arsénolite. Source: Ben Mills [domaine public] Notez que dans l'image, la structure est montrée à partir d'un plan supérieur. Par rapport à Claudetita, sa différence structurelle avec l'arsénolite est évidente. Ici, ce sont des molécules discrètes4SOIT6 que les unités sont maintenues par les forces de van der Waals.
Propriétés
Appellations commerciales
-Arsénolite
-Arsodent
-Trisenox
-Claudetita
Poids moléculaire
197,84 g / mol.
Aspect physique
-Cristaux cubiques blancs (arsénolite).
-Cristaux incolores monocliniques (Claudetita).
-Blanc ou transparent solide, vitré, grumeaux amorphes ou poussière cristalline.
Odeur
Toilettes.
Saveur
Insipide.
Point d'ébullition
460 ºC.
Point de fusion
-313 ºC (Claudetita).
-274 ºC (arsénolite).
point d'allumage
485 º C (Sublima).
Solubilité dans l'eau
17 g / L A 18 ºC (20 g / L A 25 ºC).
Solubilité
Acide soluble (en particulier dans l'acide chlorhydrique) et les alcalis. Pratiquement insoluble dans le chloroforme et l'éther.
Peut vous servir: centrifugationDensité
-3,85 g / cm3 (cristaux cubes);
-4,15 g / cm3 (cristaux rhombiques).
La pression de vapeur
2 47 · 10-4 mmhg à 25 ºC.
Décomposition
Ce n'est pas du carburant, mais en raison du réchauffement, il peut provoquer une fumée toxique qui peut inclure Arsina.
Corrosivité
En présence d'humidité, il peut être corrosif pour les métaux.
Chaleur de vaporisation
77 kJ / mol.
Constante de dissociation (KA)
1.1 · 10-4 à 25 ºC.
Indice de réfraction
-1 755 (arsénolite)
-1.92-2.01 (Claudetita).
Réactivité
-Le trioxyde d'arsenic est un composé amphotérique, mais il fonctionne de préférence en tant qu'acide.
-Il peut réagir avec de l'acide chlorhydrique ou avec de l'acide fluorhorique, formant du trifluride d'arsenic ou du trifourur d'arsenic.
-Il réagit également avec de forts oxydants, comme l'acide nitrique, provoquant de l'acide d'arsenic et de l'oxyde nitreux.
-Le trioxyde d'arsenic peut réagir avec l'acide nitrique, produisant de l'arsine ou de l'arsenic, selon les conditions de réaction.
As2SOIT3 + 6 Zn +12 HNO3 => 2 cendres3 + 6 Zn (non3)2 + 3 h2SOIT.
Cette réaction a servi de base à la création du test des marais, utilisée pour la détection de l'empoisonnement en arsenic.
Nomenclature
À2SOIT3 Il peut être nommé selon les nomenclatures suivantes, sachant que l'arsenic travaille avec Valence +3:
-Oxyde d'Arsenioso (nomenclature traditionnelle).
-Oxyde d'arsenic (III) (nomenclature des stocks).
-Trioxyde de diarrénique (nomenclature systématique).
Applications
Industriels
-Il est utilisé dans la fabrication de verre, en particulier en tant qu'agent décoloré. Il est également utilisé dans l'élaboration des céramiques, des produits électroniques et des feux d'artifice.
-Il est ajouté comme composant mineur aux alliages à base de cuivre, pour augmenter la résistance à la corrosion des métaux en alliage.
-Le comme2SOIT3 Il s'agit du matériau de départ pour la préparation de l'arsenic élémentaire, pour améliorer les articulations électriques et l'élaboration des semi-conducteurs d'Arsenuros
Il peut vous servir: chimie nucléaire: histoire, domaine d'étude, zones, applications-Le comme2SOIT3, Ainsi que le cuivre arseniato, ils sont utilisés comme conservateurs en bois. Il a été utilisé en combinaison avec de l'acétate de cuivre pour l'élaboration du pigment vert de Paris, utilisé dans l'élaboration des peintures et des raticides.
Médecins
-Le trioxyde d'arsenic est un composé qui est utilisé depuis des siècles dans le traitement de nombreuses maladies. Il a été utilisé comme tonique dans le traitement des troubles nutritionnels, de la névralgie, des rhumatismes, de l'arthrite, de l'asthme, de la Corée, du paludisme, de la syphilis et de la tuberculose.
-De même, il a été utilisé dans le traitement local des maladies de la peau, utilisé pour détruire certains épithéliomes superficiels.
-La solution de Fowler a été utilisée dans le traitement des maladies de la peau et de la leucémie. L'utilisation de ce médicament est interrompue.
-Dans les années 1970, le chercheur chinois, Zhang Tingdong, a développé une enquête sur l'utilisation du trioxyde d'arsenic dans le traitement de la leucémie promecytaire aiguë (APL). Qui a conduit à la production du médicament Trisenox, qui a été approuvé par la FDA des États-Unis.
-Trisenox a été utilisé chez les patients atteints de PLA qui ne répondent pas au traitement de la «première ligne», composé de tous les acides transivatiques (attra). Il a été démontré que le trioxyde d'arsenic induit des cellules cancéreuses à souffrir d'apoptose.
-Le trisenox est utilisé comme cytostatique dans le traitement du sous-type promisélocytaire réfractaire (M3) de l'application.
Les références
- Trioxyde d'arsenic. Le Sevier. Récupéré de: ScienceDirect.com
- Oxyde d'arsenic (iii). Récupéré de: pubchem.NCBI.NLM.NIH.Gouvernement
- « Anthraceno ce qui est, la structure, les propriétés, les utilisations
- Biographie, style et œuvres de Dámaso Alonso »

