Anthraceno ce qui est, la structure, les propriétés, les utilisations
- 5079
- 1142
- Adam Mercier
Il Anthracène Il s'agit d'un hydrocarbure aromatique polycyclique (HAP) qui est formé par la fusion de trois anneaux de benzène. C'est un composé incolore, mais sous l'irradiation de la lumière ultraviolette acquiert une couleur bleu fluorescent. L'anthracène sublime facilement.
C'est un solide blanc, mais il peut également se produire sous forme de cristaux incolores non coloriques, d'une odeur aromatique douce. L'anthracène solide est pratiquement insoluble dans l'eau et est partiellement soluble dans les solvants organiques, en particulier dans le disulfure de carbone, CS2.
Il a été découvert en 1832 en août Laurent et Jean Dumas, en utilisant le goudron comme matière première. Ce matériau continue d'être utilisé dans la production d'anthracène, car il contient 1,5% du composé aromatique. Il peut également être synthétisé à partir de la benzoquinone.
Il se trouve dans l'environnement en tant que produit de la combustion partielle des hydrocarbures fossiles. Il a été trouvé dans l'eau potable, dans l'air atmosphérique, dans les évasions des véhicules à moteur et dans la fumée des cigarettes. Apparaît sur la liste de l'EPA (Agence américaine de protection de l'environnement) des polluants environnementaux les plus importants.
Structure anthracène
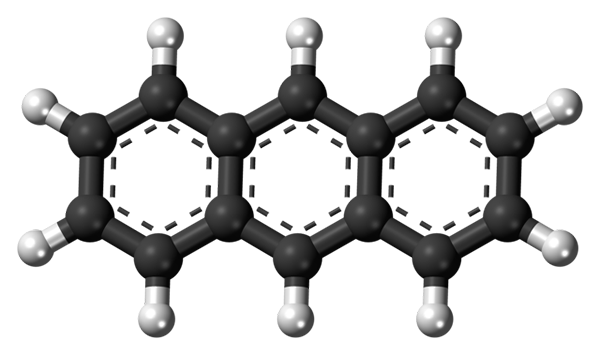 Les trois anneaux aromatiques de l'anthracène. Source: Jynto [CC0]
Les trois anneaux aromatiques de l'anthracène. Source: Jynto [CC0] L'image supérieure montre la structure de l'anthracène représenté avec un modèle de sphères et de barres. Comme on peut le voir, il y a trois anneaux aromatiques à six carbone; Ce sont des anneaux de benzène. Les lignes pointillées indiquent l'aromaticité présente dans la structure.
Tous les carbones ont une hybridation SP2, Donc la molécule est dans le même plan. Par conséquent, l'anthracène peut être considéré comme une petite feuille aromatique.
Notez que les atomes d'hydrogène (sphères blanches), sont pratiquement découvertes devant une série de réactions chimiques.
Forces intermoléculaires et structure cristalline
Anthracène. Par exemple, vous pouvez voir que deux de ces "feuilles" se joignent et déplacent les électrons de leur nuage π (les centres aromatiques des anneaux), ils parviennent à rester ensemble.
Une autre interaction possible est que les hydrogènes, avec une certaine charge partielle positive, sont attirés par les centres négatifs et aromatiques des molécules anthractes voisines. Et par conséquent, ces attractions exercent un effet directionnel qui guide les molécules anthracènes dans l'espace.
Peut vous servir: vitesse constanteAinsi, l'anthracène est ordonné de telle manière qu'il adopte un motif de structure à long terme; Et par conséquent, il peut cristalliser dans un système monoclinique.
Vraisemblablement, ces cristaux présentent un produit de colorations jaunâtres de leur oxydation en antraquinona; qui est dérivé de l'anthracène dont le solide est jaune.
Propriétés
Noms chimiques
-Anthracène
-Paranaftalène
-Anthracine
-Huile verte
Formule moléculaire
C14Hdix ou (c6H4Ch)2.
Poids moléculaire
178 234 g / mol.
Description physique
Solide blanc ou jaune pâle. Cristaux monocliniques Produit de recristallisation dans l'alcool.
Couleur
Quand c'est pur, l'anthracène est incolore. Avec des cristaux jaune jaune jaune donne la fluorescence d'une couleur bleue. Vous pouvez également présenter certains tons jaunâtres.
Odeur
Aromatique doux.
Point d'ébullition
341,3 ºC.
Point de fusion
216 ºC.
point d'allumage
250 ºF (121 ºC), tasse fermée.
Solubilité dans l'eau
Pratiquement insoluble dans l'eau.
0.022 mg / L d'eau à 0 ºC
0044 mg / L d'eau à 25 ° C.
Solubilité en éthanol
0,76 g / kg à 16 ° C
3,28 g / kg à 25 ° C. Notez comment est plus soluble dans l'éthanol que dans l'eau à la même température.
Solubilité en hexano
3,7 g / kg.
Solubilité dans le benzène
16,3 g / L. Sa plus grande solubilité dans le benzène montre sa grande affinité pour lui, car les deux substances sont aromatiques et cycliques.
Solubilité du disulfure de carbone
32,25 g / L.
Densité
1,24 g / cm3 à 68 ºF (1,25 g / cm3 à 23 ° C).
Densité de vapeur
6,15 (avec l'air pris comme référence égale à 1).
La pression de la vapeur
1 mmHg à 293 ºF (Sublima). 6,56 x 10-6 mmhg à 25 ºC.
La stabilité
Il est stable s'il est stocké dans les conditions recommandées. Il est triboluminescent et triboélectrique; Cela signifie qu'il émet de la lumière et de l'électricité quand il se frotte. L'anthracène s'assombrit lorsqu'il est exposé au soleil.
Auto-direction
1.004 ºF (540 ºC).
Décomposition
Des composés dangereux par combustion (oxydes de carbone) sont produits. Il se décompose lorsqu'il est chauffé sous l'influence de forts oxydants, produisant un acre et de la fumée toxique.
Il peut vous servir: Nitrobenzène (C6H5N2): structure, propriétés, utilisations, risquesChaleur de combustion
40,110 kJ / kg.
Capacité calorique
210,5 J / mol · k.
Longueur d'onde d'absorption maximale (lumière visible et ultraviolet)
Λ maximum 345,6 nm et 363,2 nm.
Gelée
-0,602 CPOISE (240 ºC)
-0,498 CPOISE (270 ºC)
-0,429 CPOISE (300 ° C)
Comme on peut le voir, sa viscosité diminue à mesure que la température augmente.
Nomenclature
Anthracen est une molécule polycyclique uniforme, et selon la nomenclature établie pour ce type de système, son vrai nom devrait être Tricen. Le préfixe Tri est dû au fait qu'il y a trois anneaux de haricot. Cependant, le nom trivial Anthracène a étendu et enraciné dans la culture populaire et scientifique.
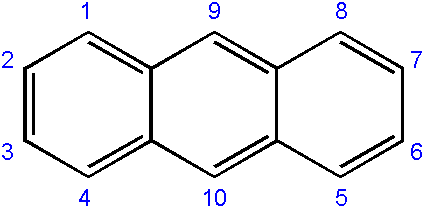
La nomenclature des composés en dérive est généralement quelque peu complexe et dépend du carbone où le remplacement se produit. Ce qui suit montre la numérotation respective des carbones pour anthracte:
 Numéro de carbones en anthracène. Source: EDGAR181 [Domaine public]
Numéro de carbones en anthracène. Source: EDGAR181 [Domaine public] L'ordre de numérotation est dû à la priorité de réactivité ou de sensibilité desdits carbones.
Les carbones des extrémités (1-4 et 8-5) sont les plus réactifs, tandis que ceux du milieu (9-10) réagissent dans d'autres conditions; Par exemple, oxydatif, pour former l'antraquinone (9, 10-dioxontracene).
Toxicité
En contact avec la peau, il peut provoquer une irritation, des démangeaisons et des brûlures, qui aggravent avec la lumière du soleil. Anthracène est le photosensibilisateur, ce qui améliore les dommages cutanés causés par le rayonnement UV. Il peut provoquer une dermatite aiguë, une téangiectasie et des allergies.
En contact avec les yeux, il peut provoquer une irritation et une brûlure. La respiration de l'anthracène peut irriter le nez, la gorge et les poumons, provoquant une toux et une respiration sifflante.
L'apport anthracène a été associé chez l'homme aux maux de tête, aux nausées, à la perte d'appétit, à une inflammation du tractus gastro-intestinal, à des réactions lentes et à une faiblesse.
Il y a eu des suggestions d'une action contre le cancer de l'anthracène. Cependant, cette présomption n'a pas été corroborée, y compris certains dérivés anthracènes ont été utilisés dans le traitement de certains types de cancer.
Applications
Technologique
-L'anthracène est un semi-conducteur organique, utilisé comme désert dans des photons à haute énergie, des électrons et des particules alpha.
-Il est également utilisé pour le revêtement en plastique, comme le polyviniltoluène. Ceci afin de produire des entourages en plastique, avec des caractéristiques de type eau, pour l'utiliser dans la dosimétrie de la radiothérapie.
Il peut vous servir: pipéridine: structure, synthèse, dérivés, réactions-L'anthracène est couramment utilisé comme traceur de rayonnement UV, appliqué dans des revêtements dans des cartes de circuits imprimées. Cela permet d'inspecter la doublure avec une lumière ultraviolette.
Molécule standard
En 2005, les chimistes de l'Université de Californie à Riverside, ont synthétisé la première molécule standard: 9.10-ditioantone. Ceci est poussé en ligne droite lorsqu'il est chauffé sur une surface de cuivre plate, et peut se déplacer comme s'il avait deux pieds.
Les chercheurs pensaient que la molécule était potentiellement utilisable dans l'informatique moléculaire.
Piézocromaticité
Certains dérivés de l'anthracène ont des propriétés piézochromatiques, c'est-à-dire qu'ils ont la capacité de changer de couleur en fonction de la pression appliquée. Par conséquent, ils peuvent être utilisés comme détecteurs de pression.
L'anthracène est également utilisé dans l'élaboration des écrans de fumée So-appelés.
Écologique
Les hydrocarbures aromatiques politiques (HAP) sont des polluants environnementaux, principalement à partir de l'eau, de sorte que des efforts sont faits pour réduire la présence toxique de ces composés.
L'anthracène est un matériau (HAP) et est utilisé comme modèle, pour étudier l'application de la méthode de pyrolyse de l'eau dans la dégradation des composés PAH.
La pyrolyse d'eau est utilisée dans le traitement de l'eau industrielle. Son action sur l'anthracène a produit la formation de composés d'oxydation: Antrron.
Ces produits sont moins stables que l'anthracène et, par conséquent, ils sont moins persistants dans l'environnement, pouvant être plus facilement éliminés que les composés des HAP.
Autres
-L'anthracène s'oxyde pour créer l'anthroquinone, utilisée dans la synthèse des colorants et des colorants
-L'anthracène est utilisé dans la protection du bois. Il est également utilisé comme insecticide, accident vasculaire cérébral, herbicide et raticide.
-L'antibiotique de l'anthracycline a été utilisé en chimiothérapie, car il inhibe la synthèse de l'ADN et de l'ARN. La molécule d'anthracycline est entrecoupée entre les bases d'ADN / ARN, inhibant la réplication des cellules cancéreuses à croissance rapide.
Les références
- Anthracène. Récupéré de: dans.Wikipédia.org
- Anthracène. Récupéré de: pubchem.NCBI.NLM.NIH.Gouvernement
- « Amphibiens Que sont les caractéristiques, les types, les systèmes, la reproduction
- Trioxyde d'arsenic (AS2O3) »

