Tritio
- 1865
- 2
- Adrien Remy
Qu'est-ce que le tritium?
Il Tritio C'est le nom qui a été accordé à l'un des isotopes de l'élément chimique hydrogène, dont le symbole est généralement t ou 3H, bien qu'il soit également appelé hydrogène-3. Ceci est largement utilisé dans un grand nombre d'applications, en particulier dans le domaine nucléaire.
De plus, dans les années 1930, cet isotope est originaire pour la première fois, sur la base du bombardement avec des particules d'énergie élevées (appelées deutérones) d'un autre isotope du même élément appelé deutérium, grâce aux scientifiques P. Harteck, m. L. Oliphant et E. Rutherford.
Ces chercheurs n'ont pas réussi dans l'isolement du Tritium malgré leurs essais, qui ont montré des résultats concrètes entre les mains de Cornog et Álvarez, découvrant à son tour les qualités radioactives de cette substance.
Sur cette planète, la production de tritium est de nature extrêmement rare, n'étant que dans de si petites proportions que les traces sont considérées par des interactions atmosphériques avec le rayonnement cosmique.
Structure de trio
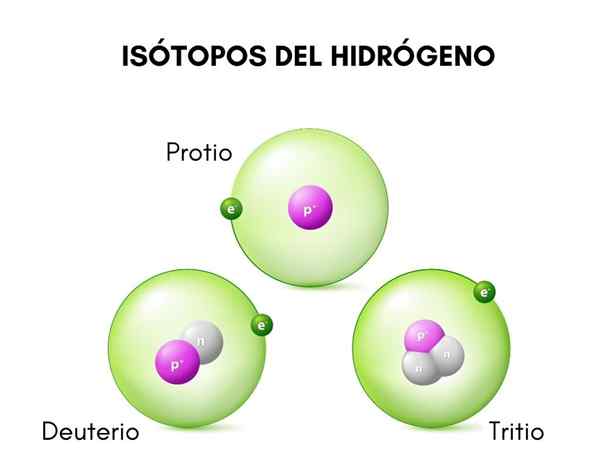
Lorsque vous parlez de la structure du tritium, la première chose qui doit être remarquée est son noyau, le possesseur de deux neutrons et un seul proton, ce qui lui donne une masse trois fois supérieure à celle de l'hydrogène ordinaire.
Cet isotope a des propriétés physiques et chimiques qui la distinguent des autres espèces isotopiques de l'hydrogène, malgré ses similitudes structurelles.
En plus d'avoir un poids ou une masse atomique d'environ 3 g, cette substance radioactivité manifeste, dont les caractéristiques cinétiques montrent une demi-vie d'environ 12,3 ans.

Dans l'image supérieure, les structures des trois isotopes connues de l'hydrogène sont comparés, appelés protio (l'espèce de plus grande abondance), du deutérium et du tritium.
Il peut vous servir: Cruise for Crucible: Caractéristiques, fonctions, utilisez des exemplesLes caractéristiques structurelles du Tritium lui permettent de coexister avec l'hydrogène et le deutérium dans l'eau qui provient de la nature, dont la production est peut-être due à l'interaction entre le rayonnement cosmique et l'azote d'origine atmosphérique.
En ce sens, cette substance est présentée dans l'eau d'origine naturelle dans une proportion de 10-18 par rapport à l'hydrogène ordinaire; c'est-à-dire une très petite abondance qui ne peut être reconnue que comme des traces.
Quelques données sur le tritium
Plusieurs façons de produire Tritio ont été étudiées et utilisées en raison de leur intérêt scientifique élevé dans les propriétés radioactives et de consommation d'énergie qu'il présente.
De cette façon, l'équation suivante montre la réaction générale par laquelle cet isotope se produit, à partir du bombardement des atomes de deutérium avec des deutérones à haute énergie:
D + D → T + H
Il peut également être effectué comme une réaction exothermique ou endothermique par un processus appelé activation à neutrons de certains éléments (comme le lithium ou le bore), et en fonction de l'élément qui est traité.
En plus de ces méthodes, Tritio peut rare à partir de la fission nucléaire, qui se compose de la division du noyau d'un atome considéré comme lourd (dans ce cas, des isotopes d'uranium ou de plutonium) pour obtenir deux noyaux ou plus de taille mineure, produisant d'énormes quantités d'énergie.
Dans ce cas, l'obtention de Tritio est donnée en tant que produit collatéral ou par produit, mais ce n'est pas le but de ce mécanisme.
À l'exception du processus décrit précédemment, tous ces processus de production de ces espèces isotopiques sont effectués dans des réacteurs nucléaires, dans lesquels les conditions de chaque réaction sont contrôlées.
Peut vous servir: verre pyrexPropriétés de Tritio
- Produit une énorme quantité d'énergie lorsqu'elle provient du deutérium.
- Il présente les propriétés de la radioactivité, qui continue de susciter l'intérêt scientifique pour la recherche sur la fusion nucléaire.
- Cet isotope est représenté dans sa forme moléculaire comme t2 soit 3H2, dont le poids moléculaire est d'environ 6 g.
- Semblable à la Protio et au Deuterium, cette substance a du mal à être confiné.
- Lorsque cette espèce est combinée avec de l'oxygène, un oxyde provient (représenté comme t2O) qui est en phase liquide et est communément appelé eau de superpesada.
- Il est capable de ressentir une fusion avec d'autres espèces légères plus facilement que celle montrée par l'hydrogène ordinaire.
- Il présente un danger pour l'environnement s'il est utilisé massivement, en particulier dans les réactions des processus de fusion.
- Il peut former avec de l'oxygène une autre substance connue sous le nom d'eau semi-perpétrée (représentée sous forme d'HTO), qui est également radioactive.
- Il est considéré comme un générateur de particules à faible énergie, connu sous le nom de rayonnement bêta.
- Lorsque des cas de consommation d'eau écrasée ont été présentés, il a été observé que sa demi-vie dans le corps est maintenue entre 2,4 à 18 jours,.
Utilisations / applications
Parmi les applications Tritium figurent les processus liés aux réactions de type nucléaire. Ensuite, une liste est affichée avec ses utilisations les plus importantes:
- Dans le domaine de la radioluminescence, le tritium est utilisé pour produire des instruments qui permettent l'éclairage, en particulier le nocturne, dans différents dispositifs d'utilisation commerciale tels que les montres, les couteaux, les armes à feu, entre autres, à travers l'auto-alimentation.
Il peut vous servir: Cério Oxyde (IV): Structure, propriétés, utilisations- Dans le domaine de la chimie nucléaire, les réactions de ce type sont utilisées comme source d'énergie dans la fabrication d'armes nucléaires et thermonucléaires, en plus d'être utilisées en combinaison avec le deutérium pour les processus de fusion nucléaire sous contrôle.
- Dans le domaine de la chimie analytique, cet isotope peut être utilisé dans le processus de marquage radioactif, où Tritio est placé dans une espèce ou une molécule spécifique et vous pouvez surveiller.
- Dans le cas de l'environnement biologique, le tritium est utilisé comme traceur de transition dans les processus océaniques, ce qui permet d'étudier l'évolution des océans sur Terre dans les sphères physiques, chimiques et même biologiques.
- Entre autres applications, cette espèce a été utilisée pour la fabrication d'une batterie atomique afin de produire de l'électricité.

