Qu'est-ce que le diagramme d'énergie moléculaire et l'exercice
- 3348
- 452
- Eva Henry
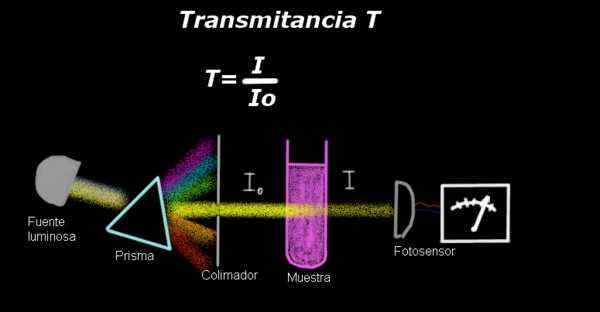
La transmittance L'optique est le quotient entre l'intensité de la lumière émergente et l'intensité de la lumière incidente sur un échantillon de solution translucide qui a été éclairée avec.
Le processus physique du passage de la lumière à travers un échantillon est appelé transmission lumineuse et la transmittance C'est une mesure de la transmission de lumière. La transmittance est une valeur importante pour déterminer la concentration d'un échantillon qui est généralement dissous dans un solvant comme l'eau ou l'alcool, entre autres.
 Figure 1. Assemblage pour la mesure de la transmittance. Source: F. Zapata.
Figure 1. Assemblage pour la mesure de la transmittance. Source: F. Zapata. Un électro-fotomètre mesure un courant proportionnel à l'intensité lumineuse qui affecte sa surface. Pour calculer la transmittance, le signal de l'intensité correspondant au solvant seul est généralement mesuré et ce résultat est enregistré comme Io.
Ensuite, l'échantillon dissous dans le solvant avec les mêmes conditions d'éclairage et le signal mesuré par l'électro-fotomètre est indiqué comme il est indiqué comme Toi, Ensuite, la transmittance est calculée en fonction de la formule suivante:
T = i / isoit
Il convient de noter que la transmittance est une quantité sans dimension, car elle est une mesure de l'intensité lumineuse d'un échantillon par rapport à l'intensité de transmission du solvant.
[TOC]
Qu'est-ce que la transmittance?
Absorption de la lumière dans un milieu
Lorsque la lumière traverse un échantillon, une partie de l'énergie lumineuse est absorbée par les molécules. La transmittance est la mesure macroscopique d'un phénomène qui se produit au niveau moléculaire ou atomique.
La lumière est une onde électromagnétique, l'énergie qu'elle transporte se trouve dans le champ électrique et magnétique de l'onde. Ces champs oscillants interagissent avec les molécules d'une substance.
Il peut vous servir: Rutherford Atomic Modèle: Histoire, expériences, postulatsL'énergie qui transporte l'onde dépend de sa fréquence. La lumière monochromatique n'a qu'une seule fréquence, tandis que la lumière blanche a une plage de fréquences ou un spectre.
Toutes les fréquences d'une onde électromagnétique se déplacent sous vide à la même vitesse de 300000 km / s. Si nous désignons c À la vitesse de la lumière dans le vide, la relation entre la fréquence F et longueur d'onde λ est:
C = λ⋅f
Comme c C'est une constante à chaque fréquence correspond à sa longueur d'onde respective.
Pour mesurer la transmittance d'une substance, les régions du spectre électromagnétique visible (380 nm à 780 nm), la région ultraviolette (180 à 380 nm) et celle de l'infrarouge (780 nm jusqu'à 5600 nm) sont utilisées
La vitesse de propagation de la lumière dans un milieu matériel dépend de la fréquence et est inférieure à c. Cela explique la dispersion dans un prisme avec lequel les fréquences qui composent la lumière blanche peuvent être séparées.
Théorie moléculaire de l'absorption de la lumière
Les atomes et les molécules ont quantifié les niveaux d'énergie. À température ambiante, les molécules sont à leurs niveaux d'énergie les plus bas.
Le photon est la particule quantique associée à l'onde électromagnétique. L'énergie Foton est également quantifiée, c'est-à-dire un photon de fréquence F Il a l'énergie donnée par:
E = h⋅f
où H C'est la constante de Planck dont la valeur est de 6,62 × 10 ^ -34 J⋅s.
La lumière monochromatique est un faisceau de photons d'une fréquence et d'une énergie donnée.
Les molécules absorbent les photons lorsque leur énergie coïncide avec la différence nécessaire pour amener la molécule à un niveau d'énergie plus élevé.
Les transitions énergétiques par absorption de photons dans les molécules peuvent être de plusieurs types:
Peut vous servir: moteur à cage d'écureuil1- transitions électroniques, lorsque les électrons d'orbitales moléculaires passent à l'orbitale de plus grande énergie. Ces transitions se produisent généralement dans la gamme visible et ultraviolette et sont les plus importants.
2- transitions vibratoires, les énergies de liaison moléculaire sont également quantifiées et lorsqu'un photon de la région infrarouge est absorbé, la molécule passe à un état d'énergie vibratoire plus élevé.
3- transitions rotationnelles, lorsque l'absorption d'un photon conduit à la molécule à un état de rotation d'une plus grande énergie.
Diagramme d'énergie moléculaire
Ces transitions sont mieux comprises avec un diagramme d'énergie moléculaire illustré à la figure 2:
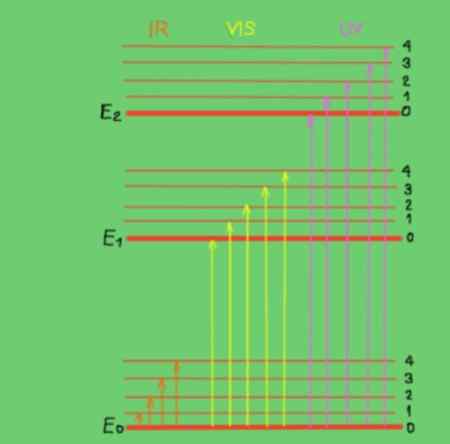 Figure 2. Diagramme d'énergie moléculaire. Source: F. Zapata.
Figure 2. Diagramme d'énergie moléculaire. Source: F. Zapata. Dans le diagramme, les lignes horizontales représentent différents niveaux d'énergie moléculaire. La ligne E0 est un niveau d'énergie fondamental ou inférieur. Les niveaux E1 et E2 sont des niveaux excités de plus grande énergie. Les niveaux E0, E1, E2 correspondent aux états électroniques de la molécule.
Sous-niveaux 1, 2, 3, 4 à chaque niveau électronique correspondent aux différents états vibrationnels correspondant à chaque niveau électronique. Chacun de ces niveaux a les plus belles subdivisions qui ne sont pas montrées qui correspondent aux états de rotation associés à chaque niveau de vibration.
Le diagramme montre des flèches verticales qui représentent l'énergie des photons dans la gamme infrarouge, visible et ultraviolette. Comme on peut le voir, les photons infrarouges n'ont pas assez d'énergie pour promouvoir les transitions électroniques, au lieu de rayonnement visible et ultraviolet oui.
Lorsque les photons incidents d'un faisceau monochromatique coïncident dans l'énergie (ou la fréquence) avec la différence d'énergie entre les états d'énergie moléculaire, alors l'absorption des photons se produit.
Peut vous servir: échelles thermométriquesFacteurs en fonction de la transmittance
Selon ce qui a été dit dans la section précédente, la transmittance dépendra alors de plusieurs facteurs parmi lesquels nous pouvons nommer:
1- La fréquence avec laquelle l'échantillon s'allume.
2- Le type de molécules que vous souhaitez analyser.
3- La concentration de la solution.
4- La longueur du chemin a traversé le faisceau lumineux.
Les données expérimentales indiquent que la transmittance T diminue de façon exponentielle avec la concentration C Et avec la longueur L du chemin optique:
T = 10-A⋅c⋅l
Dans l'expression précédente pour C'est une constante qui dépend de la fréquence et du type de substance.
Exercice résolu
Exercice 1
Un échantillon de motif d'une certaine substance a une concentration de 150 micromoles par litre (μM). Lorsque votre transmittance avec 525 nm est mesurée, une transmittance 0 0 est obtenue.4.
Un autre échantillon de la même substance, mais de concentration inconnue a une transmittance 0.5, lorsqu'il est mesuré à la même fréquence et avec la même épaisseur optique.
Calculer la concentration du deuxième échantillon.
Répondre
La transmittance T se désintègre de façon exponentielle avec la concentration C:
T = 10-B⋅l
Si vous prenez le logarithme de l'égalité précédente, il reste:
journal t = -b⋅c
Le membre divisé en membre l'égalité précédente appliquée à chaque échantillon et effacer la concentration inconnue demeure:
C2 = c1⋅ (log t2 / log t1)
C2 = 150 μm⋅ (log 0.5 / log 0.4) = 150 μm⋅ (-0.3010 / -0.3979) = 113.5 μm
Les références
- Atkins, P. 1999. Chimie physique. Éditions Omega. 460-462.
- Le guide. Transmittance et absorbance. Récupéré de: chimie.Laguia2000.com
- Toxicologie environnementale. Transmittance, absorbance et loi de Lambert. Récupéré de: le référentiel.Innovationumh.est
- Physique de l'aventure. Absorbance et transmittance. Récupéré de: rpfisica.Blogspot.com
- Sistophotométrie. Récupéré de: Chem.Bibliothèque.org
- Toxicologie environnementale. Transmittance, absorbance et loi de Lambert. Récupéré de: le référentiel.Innovationumh.est
- Wikipédia. Transmittance. Récupéré de: Wikipedia.com
- Wikipédia. Spectrophotométrie. Récupéré de: Wikipedia.com
- « Origine mixcóatl, caractéristiques, rituels
- Étape d'indépendance du contexte et du développement du Mexique »

