Transformations de la matière
- 3527
- 584
- Prof Ines Gaillard
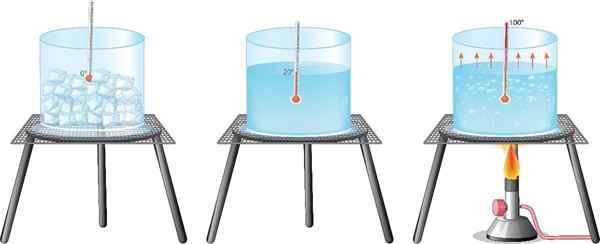
 Les transformations de la matière sont les transformations dont elle souffre sans changer sa composition. Par exemple, l'eau dans sa forme liquide, solide (glace) ou soude (vapeur) reste de l'eau
Les transformations de la matière sont les transformations dont elle souffre sans changer sa composition. Par exemple, l'eau dans sa forme liquide, solide (glace) ou soude (vapeur) reste de l'eau Quelles sont les transformations de la matière?
Les transformations de la matière sont les modifications que cela souffre sans que sa composition ne change. C'est-à-dire que la matière est transformée lorsqu'elle passe par des changements physiques et chimiques.
Des exemples de changements physiques sont la formation de glace lorsque la température descend, la rosée sur les feuilles qui apparaît le matin, la dilatation des objets lorsqu'il est chauffé et l'aimantation d'un corps.
Pour sa part, l'oxydation des vis et des ongles est un changement chimique, car l'oxyde est une substance différente du fer d'origine. Dans tous les cas, des changements d'énergie sont nécessaires afin que ces transformations aient lieu.
La transformation de la glace est un changement d'état dans lequel l'eau se solidifie, mais il y a plus de possibilités. La matière se produit dans la nature et en laboratoire dans divers États, dont le gaz, le liquide et le solide sont les trois les plus courants, du moins dans des conditions terrestres.
Mais, puisque la matière change, les scientifiques ont rencontré plus d'États, de nature quelque peu exotique, sur une base expérimentale et théorique.
On peut affirmer qu'il y a cinq états fondamentaux de la matière:
- Solide
- Liquide
- Gaz
- Plasma
- Condensat de Bose-Einstein
Parmi ceux-ci, les trois premiers sont stables dans les conditions de notre planète, tandis que les deux derniers nécessitent des moyens technologiques pour se produire, bien que dans l'univers ils soient fréquents. Le plasma est, en fait, l'état de matière le plus courant dans le cosmos.
Les états fondamentaux de la matière
Dans les conditions de pression et de température de la Terre, la matière est normalement présentée dans trois états: solide, liquide et gaz, tandis que les états de plasma et de condensat de Bose-Einstein sont obtenus dans différentes conditions, qui peuvent être obtenues en laboratoire.
Peut vous servir: mesures non conventionnellesPour expliquer pourquoi, il est nécessaire de se rappeler que la matière est composée de particules, liées par des forces, à la fois attrayantes et répulsives. Les forces d'attraction, comme son nom l'indique, ont tendance à assembler les particules, tandis que celles répulsives ont l'effet inverse.
Solides, liquides et gaz
Lorsque les forces d'attraction prévalent entre les particules, elles restent proches les unes des autres, ensemble dans des positions plus ou moins fixes, donnant naissance au solides. Les particules peuvent vibrer, mais non abandonner leur position dans le solide, par conséquent, cela maintient une forme et un volume défini.
Dans les Liquides, Les forces d'attraction permettent aux particules de se poursuivre à proximité, mais sont moins intenses que dans les solides en leur offrant la possibilité de se «glisser» d'une certaine manière. Pour cette raison, les liquides adaptent leur forme au conteneur qui les contient, mais maintiennent leur volume fixe.
Enfin, dans le Des gaz, Les forces attractives sont encore plus faibles, principalement des forces de répulsion. Cela fait que les particules restent loin les unes des autres, et avec beaucoup plus de liberté de mouvement. Pour cette raison, les gaz se développent jusqu'à ce que le volume disponible occupe complètement.
Bose-Einstein Condolontes et condensats
En chauffant suffisamment le gaz, les ions et les électrons se séparent dans un processus appelé ionisation, De cette façon plasma dans le laboratoire. L'état du plasma n'est pas facile à voir naturellement près de la terre, mais il peut en être vu dans les lumières du nord et du sud.
Ce beau phénomène naturel se produit lorsque les particules du vent solaire, un plasma plutôt diffus, affectent l'atmosphère terrestre, ionisant.
À l'autre extrémité de l'échelle, le refroidissement, juste au-dessus du zéro absolu, un nouvel état de matière apparaît dans lequel la plupart des particules sont à l'état fondamental, qui est l'énergie la plus basse.
Il peut vous servir: aspect le plus important de la petite science, de la grande science et de la technologieCet état de matière est appelé Condensat de Bose-Einstein, par les physiciens Satyendra Bose et Albert Einstein, qui ont prédit leur existence en 1924.
Plusieurs années plus tard, en 1995, plusieurs scientifiques ont réussi à transporter des gaz très dilués à cet état, une tâche facile, étant donné que les températures de nano-kelvin sont nécessaires au-dessus du zéro absolu.
Les changements d'état dans la question
De nature, il est très courant que la matière passe d'un État à l'autre. Normalement, ces changements physiques sont dus à des variations de pression et de température, dérivées de l'augmentation ou de la diminution de l'énergie des particules.
Lorsque l'énergie thermique est ajoutée à un matériau, l'énergie cinétique de ses particules augmente, réduisant la force d'attraction qui les maintient en cohésion. Si le matériau était à l'état solide, il peut alors se déplacer à l'état liquide, ou même aller directement à l'état gazeux.
Au contraire, en éliminant suffisamment d'énergie thermique, il est possible de faire une transformation gazeuse en liquide, ou qu'elle passe du liquide à solide. En tout cas, la composition de la substance ne change pas.
L'exemple le plus familier pour tous est l'eau: il est bien connu qu'une partie de l'eau liquide est transformée en vapeur lorsqu'elle est bouillie, tandis qu'elle passe pour la refroidir en glace en congélateur.
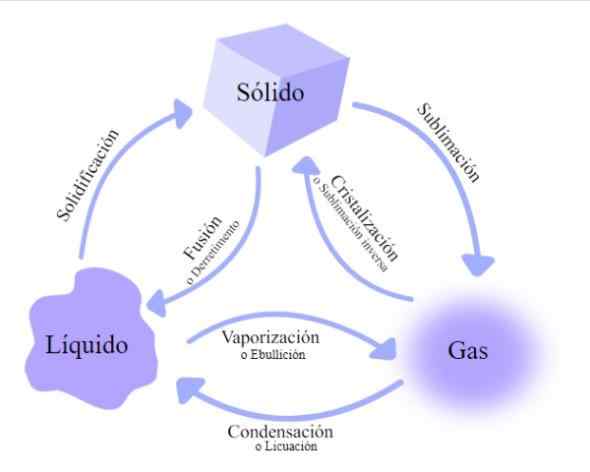 Changements dans l'état de la matière. Source: Wikimedia Commons
Changements dans l'état de la matière. Source: Wikimedia Commons Il y a plusieurs taux de change à travers lesquels la matière passe, classée selon que l'énergie thermique augmente ou diminue:
- Progressive, Ils ont lieu lorsque le matériau absorbe l'énergie thermique.
- Régressif, Ce sont eux qui se produisent lorsque le matériau donne de l'énergie.
Transformations progressives
Parmi les différentes transformations progressives qui se déroulent en la matière en ajoutant de l'énergie, figurent:
La fusion
Un changement qui se produit lorsque le matériau passe de sa phase solide à sa phase liquide. Par exemple, en faisant fondre un bloc de glace ou en chauffant ou en cire dans une casserole.
Vaporisation
Dans ce cas, l'affaire est transformée par l'état liquide à l'état gazeux.
Peut vous servir: méthodologieLa vaporisation se produit de deux manières:
- Ébullition, se déroule lorsque le matériau atteint son température d'ébullition, De cette façon, l'énergie est suffisante pour surmonter les forces intermoléculaires qui gardent les particules à l'état liquide. Chaque substance a une température d'ébullition caractéristique, à une certaine pression.
- Évaporation, Seules les particules superficielles changent l'état, car le matériau n'est pas à la température nécessaire pour entrer à ébullition. L'exemple le plus connu est l'évaporation de l'eau laissée dans un récipient, à température ambiante.
Volatilisation
Appelé trop sublimation, Il a lieu lorsque le matériau se convertit directement à partir du solide de gaz, sans passer par la phase liquide.
Par exemple, la glace sèche est le dioxyde de carbone2 volatilisé à température ambiante. Le naphtalène, qui est utilisé pour protéger les vêtements d'insectes, passe lentement du solide à être un gaz.
Ionisation
C'est le passage d'un gaz plasma.
Transformations régressives
Les transformations sont-elles causées par la diminution de l'énergie thermique des particules. Parmi eux se trouvent:
Solidification
C'est le changement de matière de l'état liquide au solide en refroidissant, comme cela se produit lors de la mise en place d'eau dans le congélateur. Le processus est dû au fait que la substance donne de l'énergie à l'environnement froid, formant de la glace.
Condensation
Il se produit lorsqu'il passe de l'état gazeux à la phase liquide, comme avec la vapeur d'eau dans l'air, lorsque vous entrez en contact avec la surface froide du pare-brise de la voiture.
Liquéfaction
C'est la transformation de la matière lors du passage du gaz au liquide, comme cela se produit, le refroidissement de l'ammoniac ou du dioxyde de carbone à haute pression.
Sublimation inverse
C'est le passage de la matière à l'état gazeux à solide, comme avec l'iode gazeux qui s'affronte contre une surface froide, entraînant la formation de cristaux solides. Il est également connu sous le nom cristallisation.
Désinsionisation
Changement de l'état du plasma à l'état gazeux.
Les références
- Chang, R. (2013). Chimie. 11va. Édition. McGraw Hill Education.
- Giancoli, D. (2006 =. Physique: principes avec applications. 6e. Ed Prentice Hall.
- Matière et ses propriétés. Récupéré de: elbibliote.com.
- OpenTax. Chimie. Récupéré de: OpenStax.org.
- Shipman, J. (2009). Une introduction aux sciences physiques. Douzième édition. Brooks / Cole, Cengage Editions.

