Causes de tension en surface, exemples, applications et expériences

- 3551
- 819
- Mlle Ambre Dumont
La tension superficielle C'est une propriété physique que tous les liquides présentent et se caractérisent par la résistance que leurs surfaces s'opposent à toute augmentation de leur région. C'est la même chose que de dire que cette surface recherchera la zone la moins possible. Ce phénomène entrelace plusieurs concepts chimiques, tels que la cohésion, l'adhésion et les forces intermoléculaires.
La tension de surface est responsable de la formation des courbures de la surface des fluides dans des récipients tubulaires (cylindres gradués, colonnes, tubes à essai, etc.). Ceux-ci peuvent être concaves (incurvées de la vallée) ou convexes (dôme incurvé). De nombreux phénomènes physiques peuvent être expliqués compte tenu des changements subis par la tension de surface d'un liquide.
 Les formes sphériques adoptées par les gouttes d'eau sur les feuilles sont en partie dues à leur tension de surface. Source: Photo prise par l'utilisateur Flickr Tanakawho [CC par (https: // CreativeCommons.Org / licences / par / 2.0)]
Les formes sphériques adoptées par les gouttes d'eau sur les feuilles sont en partie dues à leur tension de surface. Source: Photo prise par l'utilisateur Flickr Tanakawho [CC par (https: // CreativeCommons.Org / licences / par / 2.0)] L'un de ces phénomènes est la tendance que les molécules de liquides ont à agglomérer sous forme de gouttes, lorsqu'ils reposent sur des surfaces qui les repoussent. Par exemple, les gouttes d'eau que nous voyons au-dessus des feuilles ne peuvent pas la mouiller en raison de sa colline, surface hydrophobe.
Cependant, il arrive un moment où la gravité exerce son rôle et la goutte est renversée comme une colonne d'eau. Un phénomène similaire se produit dans les gouttes sphériques du mercure lorsqu'un thermomètre est renversé.
D'un autre côté, la tension des eaux de surface est la plus importante de toutes, car elle contribue et organise l'état des corps microscopiques dans des milieux aqueux, tels que les cellules et leurs membranes lipidiques. De plus, cette tension est responsable de l'évaporation de l'eau lentement, et certains corps les plus denses qui peuvent flotter à sa surface.
[TOC]
Causes de tension de surface
L'explication du phénomène de tension de surface est au niveau moléculaire. Les molécules d'un liquide interagissent les uns avec les autres, de sorte qu'ils sont cohésifs dans leurs mouvements erratiques. Une molécule interagit avec ses voisins à côté et ceux qui sont au-dessus ou en dessous.
Cependant, cela ne se produit pas de la même manière avec les molécules de la surface du liquide, qui sont en contact avec l'air (ou tout autre gaz), ou avec un solide. Les molécules de surface ne peuvent pas cohésives avec celles de l'environnement extérieur.
En conséquence, ils ne connaissent aucune force qui les attire; Seulement en bas, de ses voisins du milieu liquide. Pour contrer ce déséquilibre, les molécules de surface sont "pressées", car ce n'est qu'alors qu'ils parviennent à surmonter la force qui les pousse vers le bas.
Peut vous servir: silicate de sodium (NA2SIO3): structure, propriétés, utilisations, risquesUne surface est ensuite créée où les molécules sont dans une élimination plus tendue. Si une particule veut pénétrer le liquide, elle doit d'abord traverser cette barrière moléculaire proportionnelle à la tension superficielle dudit liquide. Il en va de même pour une particule qui veut s'échapper vers l'environnement externe des profondeurs du liquide.
Par conséquent, sa surface se comporte comme s'il s'agissait d'un film élastique qui montre une résistance à la déformation.
Unités
La tension de surface est généralement représentée avec le symbole γ et est exprimée en unités N / M, force par longueur. Cependant, la plupart du temps, votre unité est dyn / cm. L'un peut devenir l'autre grâce au prochain facteur de conversion:
1 dyn / cm = 0,001 n / m
Tension des eaux de surface
L'eau est l'ouest et la plus surprenante de tous les liquides. Sa tension en surface, ainsi que plusieurs de ses propriétés, ont une valeur inhabituellement élevée: 72 dyn / cm à température ambiante. Cette valeur peut augmenter à 75,64 dyn / cm, à une température de 0 ºC; ou diminuer à 58,85 ºC, à une température de 100 ºC.
Ces observations ont du sens s'il est considéré que la barrière moléculaire est encore plus tendue à des températures proches du point de congélation, ou "desserrer" un peu plus autour du point d'ébullition.
L'eau a une grande tension de surface après ses ponts d'hydrogène. Si ceux-ci sont notoires dans le liquide, ils sont encore plus à la surface. Les molécules d'eau sont fortement liées en formant des interactions dipolo-dipolo du type H2Oh oh.
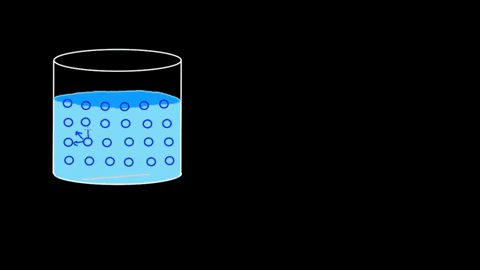 Les molécules d'eau s'attirent; Ils sont liés par des ponts d'hydrogène
Les molécules d'eau s'attirent; Ils sont liés par des ponts d'hydrogène L'efficacité de ses interactions est telle que la barrière moléculaire aqueuse peut même soutenir certains corps avant de couler. Dans les sections des applications et des expériences, ce point sera repris.
Autres exemples
Tous les liquides ont des tensions de surface, à un degré inférieur ou supérieur à celle de l'eau, soit si ce sont des substances ou des solutions pures. Quelle est la force et la tendance des barrières moléculaires de leur superficiel, elle dépendra directement de ses interactions intermoléculaires, en plus des facteurs structurels et énergétiques.
Gaz condensé
Par exemple, les molécules de gaz à l'état liquide n'interagissent que par les uns avec les autres par le biais de forces dispersives à Londres. Cela convient du fait que leurs tensions superficielles ont de faibles valeurs:
-Hélium liquide, 0,37 dyn / cm A -273 ºC
Il peut vous servir: chlorure d'ammonium (NH4CL)-Azote liquide, 8,85 dyn / cm A -196 ºC
-Oxygène liquide, 13,2 dyn / cm A -182 ºC
La tension superficielle de l'oxygène liquide est supérieure à celle de l'hélium car ses molécules ont une plus grande masse.
Liquides apolaires
À partir des liquides apolaires et organiques, ils devraient avoir des tensions de surface plus élevées que celles de ces gaz condensés. Parmi certains d'entre eux, nous avons ce qui suit:
-Dietileter, 17 dyn / cm à 20 ºC
-n-Hexano, 18,40 dyn / cm à 20 ºC
-n-Octane, 21,80 dyn / cm à 20 ºC
-Toluène, 27,73 dyn / cm à 25 ºC
Une tendance similaire est observée pour ces liquides: la tension de surface est augmentée à mesure que ses masses moléculaires augmentent. Cependant, le n-L'octane devrait, selon cela, avoir la plus grande tension de surface et non le toluène. Ici, les structures moléculaires et les géométries entrent en jeu.
Les molécules du toluène, du plan et des anillares ont des interactions plus efficaces que celles de la n-octane. Par conséquent, la surface du toluène est "tendue" que la surface du n-octane.
Liquides polaires
Être plus fort dipol-dipol. Mais ce n'est pas toujours le cas. Parmi quelques exemples que nous avons:
-Acide acétique, 27,60 dyn / cm à 20 ºC
-Acétone, 23,70 dyn / cm à 20 ºC
-Sang, 55,89 dyn / cm à 22 ° C
-Éthanol, 22,27 dyn / cm à 20 ºC
-Glycérol, 63 dyn / cm à 20 ºC
-Chlorure de sodium fondu, 163 dyn / cm à 650 ºC
-Solution NaCl 6 m, 82,55 dyn / cm à 20 ºC
Le chlorure de sodium fondu devrait avoir une énorme tension de surface: c'est un liquide visqueux et ionique.
D'un autre côté, le mercure est l'un des liquides avec la tension de surface la plus élevée: 487 dyn / cm. En elle, sa surface est composée d'atomes de mercure fortement cohésifs, bien plus que les molécules d'eau.
Applications
 Certains insectes utilisent la tension en surface de l'eau pour marcher dessus. Source: Pixabay.
Certains insectes utilisent la tension en surface de l'eau pour marcher dessus. Source: Pixabay. La tension superficielle n'a à elle seule des applications. Cependant, cela ne signifie pas qu'il n'est pas impliqué dans plusieurs phénomènes quotidiens, que s'il n'y en avait pas, ils n'arriveraient pas.
Par exemple, les moustiques et autres insectes peuvent marcher dans l'eau. C'est parce que leurs jambes hydrophobes repoussent l'eau, en même temps que leur petite masse leur permet.

La tension superficielle rencontre également un rôle dans le mouillage des fluides. Plus sa tension superficielle est grande, moins sa tendance à couler à travers les pores ou les poussins d'un matériau. En plus de cela, ce sont peu de liquides utiles pour nettoyer les surfaces.
Peut vous servir: réaction de neutralisationDétergents
C'est ici où les détergents agissent, réduisant la tension de surface de l'eau et l'aidant à couvrir de plus grandes surfaces; Tout en améliorant votre action de dépassement. En diminuant sa tension superficielle, il peut accueillir les molécules d'air, avec lesquelles des bulles se forment.
Émulsions
D'un autre côté, de faibles tensions sont liées à la stabilisation des émulsions, très importante dans la formulation de différents produits.
Expériences simples
 Clip métallique flottant en raison de la tension des eaux de surface. Source: Alvesgaspar [cc by-s (https: // CreativeCommons.Org / licences / by-sa / 3.0)]
Clip métallique flottant en raison de la tension des eaux de surface. Source: Alvesgaspar [cc by-s (https: // CreativeCommons.Org / licences / by-sa / 3.0)] Enfin, certaines expériences qui peuvent être effectuées dans n'importe quel espace domestique seront citées.
Clip d'expérience
Dans un verre à l'eau froide, un clip métallique est placé à sa surface. Comme on le voit dans l'image supérieure, le clip restera à flot grâce à la tension de surface de l'eau. Mais si un peu de lave lave est ajoutée au verre, la tension de surface diminuera considérablement et le clip va soudainement couler.

Bateau en papier
Si nous avons un navire en papier ou une palette en bois, et si vous lavez le petit ou le détergent, il est ajouté dans la tête d'un écouvillonnage, alors un phénomène intéressant se produira: il y aura une répulsion qui les étalera vers les bords du verre. Le navire en papier et la palette en bois s'éloigneront de l'évanouissement enduit de détergent.

Une autre expérience similaire et plus graphique consiste à répéter la même opération, mais dans un seau d'eau pulvérisée de poivre noir. Les particules de poivre noir s'éloigneront et la surface ira du poivre pour être cristallin, avec les bords sur les bords.
Les références
- Whitten, Davis, Peck & Stanley. (2008). Chimie. (8e Ed.). Cengage Learning.
- Wikipédia. (2020). Tension superficielle. Récupéré de: dans.Wikipédia.org
- USGS. (s.F.). Tension et eau en surface. Récupéré de: USGS.Gouvernement
- Jones, Andrew Zimmerman. (12 février 2020). Tension de surface - Définition et expériences. Récupéré de: Thoughtco.com
- Susanna Lauren. (15 novembre 2017). Pourquoi la tension de surface est-elle importante? Biolin scientifique. Récupéré de: blog.Biolinscientifique.com
- Science parentale recrue. (7 novembre 2019). Qu'est-ce que la tension de surface | Expérience scientifique cool. Récupéré de: leparlent recru.com
- Jessica Mock. (2020). Expérience de tension en surface. Étude. Récupéré de: étudier.com
- Le gamin devrait voir ça. (2020). Sept expériences de tension en surface - Physics Girl. Récupéré de: thekidshelseethis.com
- « Les 13 inventions les plus remarquables de l'Égypte
- Caractéristiques, symptômes et causes de l'atrophie cérébrale »

