Table quantique
- 5085
- 554
- Prof Ines Gaillard
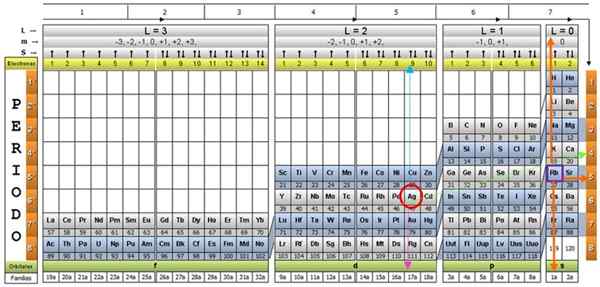
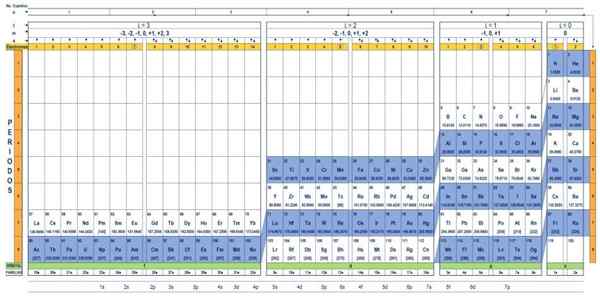 La table quantique des éléments. Source: Unam.
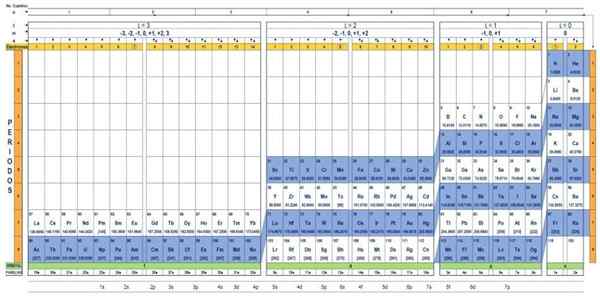
La table quantique des éléments. Source: Unam. Quelle est la table quantique?
La Table quantique C'est un moyen d'organiser les éléments chimiques, conçus pour déterminer facilement l'ensemble des nombres quantiques qui caractérisent chacun d'eux.
Les scientifiques ont découvert que, dans la nature de tous les éléments, il existe certains modèles. Parmi ces modèles figurent des nombres quantiques, quatre nombres simples qui décrivent la configuration électronique de chaque élément.
Les nombres quantiques proviennent naturellement du modèle mécanique mécanique de l'atome et sont désignés par les lettres: n, ℓ, mℓ et s. Ils décrivent l'état énergétique des électrons dans l'atome de chaque élément chimique.
Grâce au tableau périodique traditionnel et à quelques outils supplémentaires, il est possible d'avoir la configuration électronique de l'atome de n'importe quel élément. L'avantage de la table quantique est que les éléments sont organisés de manière à ce que leurs nombres quantiques soient immédiatement visibles, sans avoir besoin de faire de nombreux calculs séparément.
Caractéristiques de la table quantique
Il y a plusieurs conceptions de tables quantiques. Le modèle illustré dans la figure ci-dessus contient:
- Un en-tête avec quatre rangées, avec les valeurs des quatre nombres quantiques, n, ℓ, m et s, plus une cinquième rangée en jaune, ce qui correspond au nombre d'électrons dans l'orbitale la plus externe.
- Le corps de la table, qui se compose d'une grille qui contient le symbole de l'élément chimique, en commençant par l'hydrogène, dans l'avant-dernière colonne de la droite, suivie de l'hélium, etc. Le nombre ci-dessous représente la quantité d'électrons atomes dans un état fondamental.
- En bas, dans la rangée verte, il y a quatre classes pour organiser les éléments: les orbitales S, P, D et F (de gauche à droite).
- Enfin, sous la rangée orbitale se trouve la famille. Chaque colonne est une famille, numérotée de 1 à 32. Par exemple, les 1er et 2e familles appartiennent à la classe S, les familles du 3 à 8A appartiennent à la classe P, etc.
Quelle est la table quantique pour?
La table quantique sert à trouver l'ensemble des nombres quantiques qui caractérise un électron de l'atome. Normalement, ces électrons seront ceux de la couche la plus externe, car ce sont ceux qui définissent le comportement chimique de l'élément.
Comment est la table quantique?
La table quantique permet de trouver facilement les nombres quantiques des électrons dans la couche la plus externe de l'atome.
Exemple 1
Pour illustrer la procédure, l'élément en aluminium est pris comme exemple, dont le symbole est au. La première étape consiste à la localiser dans la table quantique, la marquant avec un Cercle rouge:
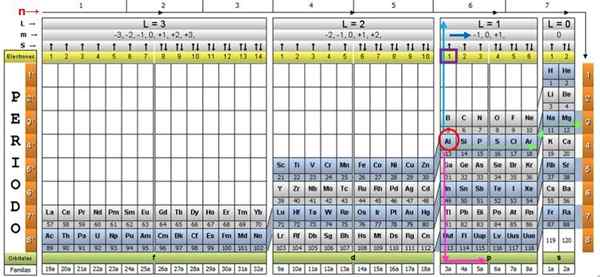
Étape 1: trouver n
Après avoir localisé l'élément dans le tableau, vous devez vous déplacer dans la même ligne et la même couleur, à droite, jusqu'à ce que vous atteigniez la colonne Orange, en suivant la route de la flèche verte montrée dans l'image.
La flèche pointe vers la boîte marquée avec le numéro 3, qui est le principal numéro quantique n:
n = 3
Étape 2: trouver ℓ
Pour déterminer le nombre quantique secondaire, la flèche verticale bleue est suivie, ce qui indique:
ℓ = 1.
Étape 3: trouver m
L'électron en aluminium externe se trouve dans la famille PuBilling P, comme on peut le lire dans la rangée verte, à laquelle la flèche rose pointe.
De plus, la quantité d'électrons dans la dernière couche est lue dans la rangée jaune de l'en-tête. Dans le cas de l'aluminium, il y a 1 électron (mis en évidence sur le carré violet), qui est la référence. En combinant les résultats ci-dessus, la configuration de la dernière couche est:
Peut vous servir: cellule galvanique: pièces, comment fonctionne, applications, exemples3p1
Il est connu qu'une couche P prend en charge un maximum de 6 électrons. Et le nombre m prend certaines des valeurs entières - ℓ, (- ℓ + 1),… 0,… (+ ℓ −1), + ℓ.
Comme dans ce cas ℓ = 1, alors m peut être −1, 0, 1.
Ces nombres apparaissent dans la rangée de l'en-tête correspondant à m (voir dans l'image l'image Flèche horizontale bleu). Le tableau suivant sert de guide pour savoir quelle est la valeur du choix, selon l'affaire:
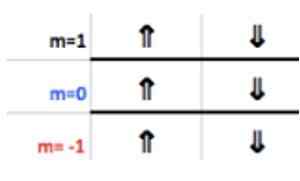
Puisque la dernière couche d'aluminium a 1 électron, le nombre quantique magnétique correspond
M = 1.
Étape 4: Trouver s
Le nombre de spin s n'a que deux valeurs: + ½ ou - ½. Dans la boîte supérieure, si la flèche indique, elle est choisie s = + ½ et si elle pointe vers le bas, alors s = - ½. Dans le cas de l'aluminium, l'électron 1 pointe donc:
S = + ½.
En bref, le nombre quantique de l'électron de la couche la plus externe d'aluminium au son:
n = 3; ℓ = 1; M = 1, s = + ½
Exemple 2 (cas exceptionnels)
Silver AG, et environ vingt éléments de plus, sont des cas exceptionnels, donc il faut prendre soin de vous utiliser la table quantique avec eux.
Si la procédure précédente est répétée, AG serait obtenu comme dernier sous-niveau sur le 4D9.
En effet, la configuration prévue de La Plata, selon la règle de Madelung, est:
12 2s2 2 P6 3s2 3p6 4s2 3Ddix 4p6 5s2 4d9
Cependant, dans la pratique, AG ne suit pas exactement cette configuration, ni aucun autre éléments dont la dernière couche prévue est 4D9, comme le cuivre et l'or, entre autres (consultez Internet pour obtenir une liste complète d'éléments qui ne suivent pas la règle de Madelung).
Peut vous servir: molélitéLa véritable configuration d'Ag est:
12 2s2 2 P6 3s2 3p6 4s2 3Ddix 4p6 5s1 4ddix
Dans lequel un électron de la couche 5s2 a sauté à la couche 4D9 Pour le terminer. De cette façon, la stabilité de l'atome augmente. Par conséquent, le dernier sous-niveau est vraiment:
5s1
Et ses nombres quantiques seraient ceux correspondant à l'élément RB, illustré dans une boîte violette, avec des flèches orange pointant vers les nombres restants:
n = 5; ℓ = 0; M = 0; S = + ½
 Examiner le tableau périodique, en effet, on voit que l'AG est dans la période 5, une caractéristique déterminée par le principal numéro quantique n.
Examiner le tableau périodique, en effet, on voit que l'AG est dans la période 5, une caractéristique déterminée par le principal numéro quantique n.
Différences avec le tableau périodique
Les deux tables sont deux façons d'organiser les éléments chimiques en fonction des caractéristiques de leurs atomes:
-Dans le tableau périodique, les éléments trouvés dans la même colonne ont des propriétés chimiques similaires. Par exemple, il commence par la colonne des métaux alcalins à gauche et se termine celui des gaz nobles vers la droite. Tandis que dans les rangs se trouvent les éléments avec le même niveau d'énergie supérieur.
-La table quantique a une disposition étagée, conçue selon les règles de remplissage. Par conséquent, vous devez suivre les étapes pour obtenir le numéro quantique principal, sauf dans le cas d'exceptions telles que l'argent, dans l'exemple de la section précédente. Les familles d'éléments de ce tableau sont liées à l'orbitale supérieur, dans S, P, D ou F.
Les références
- Chang, R. 2013. Chimie. 11va. Édition. McGraw Hill Education.
- Configuration électronique. Configuration électronique et numéros quantiques. Récupéré de: configuionectronica.com.
- Manuel de chimie. Récupéré de: DCB.ingénierie.Unam.mx.
- Chimie officielle. Comment être facile des nombres quantiques faciles. Récupéré de: Officiel de chimie.com
- Tripler. Exceptions à la règle de Madelung dans la configuration électronique des éléments chimiques. Récupéré de: triplenlace.com.

