Structure de sulfate de sodium (NA2SO4), propriétés, utilisations, obtention

- 2392
- 543
- Louna Baron
Il sulfate de sodium C'est un sel inorganique dont la formule chimique est na2Swin4. Il se compose d'un solide blanc, présent sous trois formes: anhydre, heptohydraté (de peu d'existence) et de décroissance (qui est connu sous le nom de sel de Glaubert); Ce dernier est la forme la plus abondante de sulfate de sodium.
Dispayroyed de sulfate de sodium, Na2Swin4· 10h2Ou, il a été découvert en 1625 par Glaubert dans l'eau d'une source, qui l'a nommée saltabilis (sel miraculeux) en raison de ses propriétés médicinales.
 Verre d'horloge avec un échantillon de sulfate de sodium. Source: Walkerma via Wikipedia.
Verre d'horloge avec un échantillon de sulfate de sodium. Source: Walkerma via Wikipedia. Le sulfate de sodium possède de nombreuses applications dans l'industrie du textile et du papier, ainsi que dans la fabrication de verre. Ses utilisations sont étendues avec des applications thermiques, qui incluent l'alimentation environnementale de chaleur et le refroidissement des ordinateurs portables.
Le sulfate de sodium est un composé de faible toxicité et de ses actions nuisibles, elles sont fondamentalement mécaniques et non chimiques. Pour des raisons cristallographiques, ce sel, comme son homologue Poetassium, k2Swin4, présente le cadre et les structures polymorphes.
[TOC]
Structure
Sel anhydre
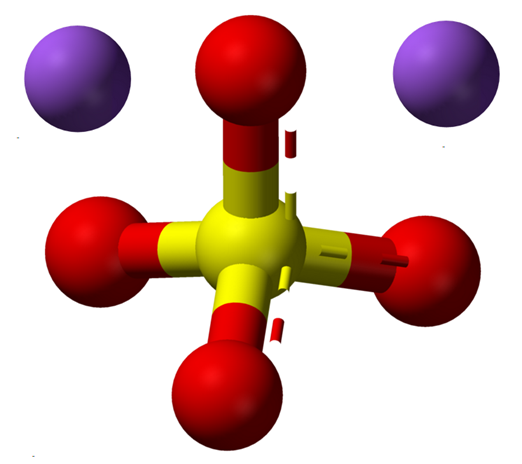 Ions de sulfate de sodium anhydre. Source: Claudio Pistilli [CC BY-SA 4.0 (https: // CreativeCommons.Org / licences / by-sa / 4.0)]
Ions de sulfate de sodium anhydre. Source: Claudio Pistilli [CC BY-SA 4.0 (https: // CreativeCommons.Org / licences / by-sa / 4.0)] La formule NA2Swin4 Indique une fois les ions na dans les cristaux de sel+ Et ainsi42- Ils sont dans une relation 1: 2; c'est-à-dire pour tous les deux cations na+ il y a un anion alors42- interagir avec eux par attraction électrostatique (image supérieure).
Bien sûr, cela s'applique au NA2Swin4 anhydre, sans molécules d'eau coordonnées avec du sodium à l'intérieur des cristaux.
 Sulfate de sodium
Sulfate de sodium En dépit d'être une apparence simple, sa description structurellement est complexe. Puis un2Swin4 Il présente le polymorphisme, ayant jusqu'à cinq phases cristallines: I, II, III, IV et V, dont les températures de transition sont respectivement de 180, 200, 228, 235 et 883 ºC,.
Bien qu'il n'y ait pas de références qui le certifient, le NA2Swin4I ce doit être celui qui a une structure cristalline hexagonale, plus dense par rapport à la na ortorrombique2Swin4Iii, dans les cristaux duquel le na+ Forme de tétraède (Nao4) et les octaèdros (Nao6) coordination; c'est-à-dire qu'il peut être entouré de quatre ou six anions alors42-.
Sel de décomposition
Pendant ce temps, la structure cristalline monoclinique de son hydrate le plus important, na2Swin4· 10h2Ou, c'est plus simple. Il y a pratiquement les molécules d'eau qui interagissent ou se coordonnent avec le NA+ Dans les octaèdres na (h2SOIT)6+, Avec le so42- contribuant à peine une stabilité suffisante au verre pour exister en phase solide.
Il peut vous servir: Première révolution de la chimieCependant, son point de fusion (32,38 ºC) est bien inférieur à celui du sel anhydre (884 ºC) montre comment les molécules d'eau et leurs ponts d'hydrogène affaiblissent les interactions ioniques, plus fortes, en NA2Swin4.
Propriétés
Des noms
-Sulfate de sodium (IUPAC)
-Sel de glauber (déshydrate)
-Sala Miraculous (DecayRoper)
-Disodique sulfate.
Masse molaire
142.04 g / mol (anh¡dro)
322,20 g / mol (décydrate)
Apparence physique
Blanc Hygroscopic cristallin solide
Odeur
Toilettes
Saveur
Amer et salin
Densité
2 664 g / cm3 (anhydre)
1 464 g / cm3 (Dahydrate)
Notez comment les molécules d'eau à l'intérieur des cristaux les font se dilater et, par conséquent, diminuent leur densité.
Point de fusion
884 ºC (anhydre)
32,38 ºC (décydrate)
Point d'ébullition
1.429 ºC (anhydre)
Solubilité dans l'eau
4,76 g / 100 ml (0 ºC)
13,9 g / 100 ml (20 ºC)
42,7 g / 100 ml (100 ºC)
Toutes les valeurs de solubilité correspondent à un sel anhydre, qui est assez soluble dans l'eau à toutes les températures.
La solubilité augmente brusquement entre 0 ºC et 38,34 ºC, observant que dans cette gamme de températures, la solubilité augmente plus de 10 fois. Cependant, à partir de 32,38 ºC, la solubilité est indépendante de la température.
Il arrive qu'à température 32,8 ºC, le sulfate de sodium pour la décomposition se dissout dans sa propre eau cristalline. Par conséquent, un équilibre entre le sel de décroissance, le sel d'anhydrate et la solution saturée de sulfate de sodium.
Tant que la condition de trois phases est maintenue, la température restera constante, ce qui permet à la température des thermomètres à calibrer.
D'un autre côté, les solubilités de sel d'heptahydrate sont:
19,5 g / 100 ml (0 ºC)
44,0 g / 100 ml (20 ºC)
Notez qu'à 20 ° C, le sel d'heptahydrate est trois fois plus soluble qu'anhydre.
Indice de réfraction
1 468 (anhydre)
1 394 (décydrate)
La stabilité
Stable dans des conditions de stockage recommandées. Incompatible avec de forts acides et bases, en aluminium et en magnésium.
Décomposition
Lorsqu'il est chauffé en décomposition, il émet une fumée toxique d'oxyde de soufre et d'oxyde de sodium.
pH
Une solution aqueuse de 5% a un pH de 7.
Réactivité
Le sulfate de sodium se dissocie en solution aqueuse en 2+ Et ainsi42-, qui permet à l'ion sulfate d'être combiné avec le BA2+ Pour précipiter le sulfate de baryum. Il aide pratiquement à déplacer les ions baryum d'échantillons d'eau.
Peut vous servir: transaminationLe sulfate de sodium devient du sulfure de sodium par réaction à des températures élevées avec du charbon:
N / A2Swin4 + 2 c => na2S +2 CO2
Le sel de Glaubert, Naso4.10h2O réagit avec du carbonate de potassium pour produire du carbonate de sodium.
Applications
Industrie du papier
Le sulfate de sodium est utilisé dans la fabrication de pâte en papier. Il est utilisé dans l'élaboration du papier kraft, qui ne contient pas de lignine ou se soumet au processus de blanchiment, raison qui lui donne une grande résistance. De plus, il est utilisé dans la fabrication en carton.
Détergents
Il est utilisé comme matériau de remplissage de détergent synthétique à utiliser à la maison, ajoutant au détergent pour réduire la tension de surface.
Verre
Il est utilisé dans la fabrication de verre pour réduire ou éliminer la présence de petites bulles d'air dans le verre fondu. De plus, élimine la formation de scories pendant le processus de raffinage en verre fondu.
Industrie du textile
Le sulfate de sodium est utilisé comme mordant, car il facilite l'interaction des colorants avec les fibres de tissu. Le sulfate de sodium détahydraté est utilisé dans le test de colorant.
De plus, le sulfate de sodium est utilisé comme agent d'impression de diluant et de colorant auxiliaire; comme les colorants directs, les colorants de soufre et d'autres agents qui favorisent la coloration au coton. Il est également utilisé comme agent qui retarde les colorants directs de la soie.
Médecine
Le sulfate de sodium decahrid est utilisé comme un laxatif, car il est peu absorbé par l'intestin, et reste donc à la lumière de cette augmentation du volume. Cela stimule l'augmentation des contractions péristaltiques qui induisent l'expulsion du contenu intestinal.
Le sulfate de sodium est un antidote pour contrôler l'empoisonnement avec le baryum et les sels de plomb. Le sel de Glaubert est efficace pour l'élimination de certains médicaments excessivement ingérés; Par exemple, le paracétamol (acétoaminophène).
De plus, il est utilisé pour fournir des électrolytes pauvres en présence dans des solutions isoosmotiques.
Agent desséchant
Le sulfate de sodium car il s'agit d'un réactif inerte, est utilisé pour l'élimination de l'eau des solutions de composés organiques.
Matière première
Le sulfate de sodium est utilisé comme matière première pour la production de nombreuses substances, notamment: sulfure de sodium, carbonate de sodium et sulfate d'ammonium.
Peut vous servir: chromatographie en phase gazeuseObtention
Le sulfate de sodium est obtenu par extraction minière et réactions chimiques.
Extraction minière
Il y a trois minerai ou minéraux qui sont exploités avec des performances commerciales: Thenardita (NA2Swin4), Mirabilita (na2Swin4· 10h2O) et le glaubarita (na2Swin4·Cas4).
En Espagne, les dépôts de Thenardita et Mirabilita sont exploités par l'exploitation souterraine des galeries et des piliers. Pendant ce temps, la glauberita est obtenue à l'air libre, par de grands radeaux placés sur le réservoir minéral.
Le terrain est préparé avec un dynamitage à faible intensité pour produire une porosité qui permet la lixiviation de sulfate de sodium. La phase de production se produit avec une irrigation de gicleurs avec de l'eau douce de la glauberita, dont la lixiviation se propage de manière descente.
La saumure de sulfate de sodium est collectée, le résidu de sulfate de calcium étant rempli.
Production chimique
Le sulfate de sodium est obtenu lors de la production d'acide chlorhydrique à travers deux processus: le processus de Mannheim et le processus hardgrenave.
Processus de Mannheim
Il se fait dans de grands fours en acier et avec une plate-forme de réaction en acier de 6 m. La réaction se produit entre le chlorure de sodium et l'acide sulfurique:
2 NaCl + H2Swin4 => 2 HCL + NA2Swin4
Procédé de HardReave
Il s'agit de la réaction du chlorure de sodium, de l'oxyde de soufre, de l'oxygène et de l'eau:
4 NaCl + 2 SO2 + SOIT2 + 2 h2O => 4 HCL + NA2Swin4
Autres
Le sulfate de sodium se produit dans la réaction de neutralisation entre l'hydroxyde de sodium et l'acide sulfurique:
2 NaOH + H2Swin4 => Na2Swin4 + H2SOIT
Le sulfate de sodium est un sous-produit de la production de nombreux composés. Il est extrait des déchets liquides déchargés pendant la production de la viscose et du cellophane. Également dans la production de dichromate de sodium, de phénols, d'acide borique et de carbamate de lithium.
Des risques
Le sulfate de sodium est considéré comme un composé de faible toxicité. Cependant, cela peut produire des dommages à la personne qui l'utilise inappropriée.
Par exemple, vous pouvez provoquer une irritation des yeux, des rougeurs et une douleur. Dans la peau, cela peut provoquer une irritation et une allergie chez certaines personnes. Son ingestion peut provoquer une irritation du tube digestif avec des nausées, des vomissements et de la diarrhée. Et enfin, son inhalation produit une irritation dans les voies respiratoires.
Les références
- Fhiver & Atkins. (2008). Chimie inorganique. (Quatrième édition). Mc Graw Hill.
- Wikipédia. (2019). Sulfate de sodium. Récupéré de: dans.Wikipédia.org
- Centre national d'information sur la biotechnologie. (2019). Sulfate de sodium. Base de données PubChem. CID = 24436. Récupéré de: pubchem.NCBI.NLM.NIH.Gouvernement
- B. N. Mehrotra. (1978). La structure cristalline de Na2Swin4III. Récupéré de: RRUFF-2.géo.Arizona.Édu
- Glauberita-thenardita (sulfate de sodium). [PDF]. Récupéré de: Igme.est
- « Structure d'oxyde de zinc (ZnO), propriétés, utilisations, risques
- Caractéristiques du bleu lactophénol, composition, préparation, utilisations »

