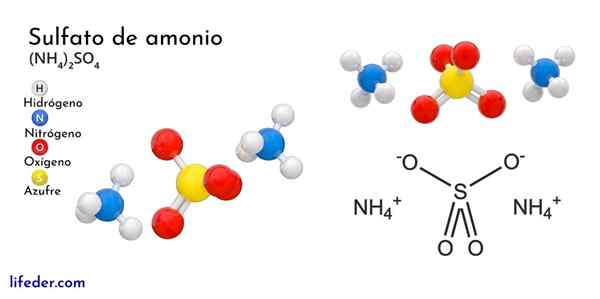
Sulfate d'ammonium
- 2408
- 193
- Anaïs Julien
Nous expliquons ce qu'est le sulfate d'ammonium, sa structure chimique, ses propriétés physiques et chimiques et les utilisations
Qu'est-ce que le sulfate d'ammonium?
Il sulfate d'ammonium C'est un sel inorganique ternaire et ammoniac d'acide sulfurique. Sa formule chimique est (NH4)2Swin4. Par conséquent, les proportions stoechiométriques disent que pour chaque anion sulfate, il y a deux cations ammonium interagissant avec lui. Cela permet la neutralité du sel ((+1) ∙ 2 + (-2)).
Sa nomenclature est due au fait d'être un sel dérivé de H2Swin4, Modification du suffixe "Uric" pour "ATO". Ainsi, les deux protons initiaux sont remplacés par NH4+, produit de la réaction avec l'ammoniac (NH3). Ainsi, l'équation chimique de sa synthèse est: 2 NH3 + H2Swin4 => (NH4)2Swin4
Le sulfate d'ammonium est également préparé par réaction de carbonate d'ammonium avec du sulfate de calcium: (NH4)2CO3 + Cas4 => (NH4)2Swin4 + Voleur3, précipiter le carbonate de calicot, qui est séparé du liquide restant.
Le sulfate d'ammonium est un stockage d'azote et de soufre, tous deux indispensables en chimie du sol et en engrais.
Structure chimique du sulfate d'ammonium

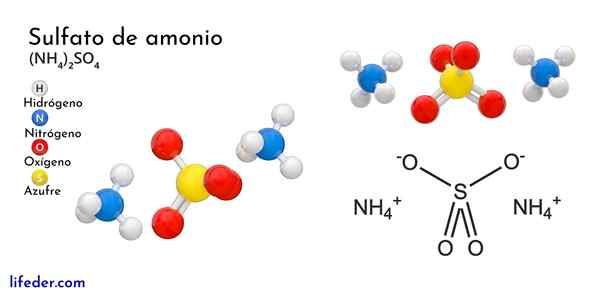
L'image supérieure illustre les géométries moléculaires des ions NH4+ Et ainsi42-. Les sphères rouges correspondent aux atomes d'oxygène, aux atomes blancs à hydrogène, à l'atome bleu à l'azote et à l'atome jaune à soufre.
Les deux ions peuvent être considérés comme deux tétraèdres, ayant ainsi trois unités qui interagissent pour former un arrangement cristallin ortorrombique. L'anion sulfate est ainsi42- Et il est capable de donner ou d'accepter quatre ponts d'hydrogène, ainsi que le cation NH4+.
Propriétés du sulfate d'ammonium
Poids moléculaire
132 134 g / mol.
Il peut vous servir: relation entre la chimie et la technologie avec l'être humain, la santé et l'environnementAspect physique
Blanc. Cristaux ortorrhrombiques blancs ou bruns, selon les niveaux d'impureté.
Odeur
Toilettes.
Point de fusion
280 ºC. Ce point de fusion, sous d'autres composés ioniques, est parce qu'il s'agit d'un sel avec des cations monovalents (+1) et avec des ions de déguisement dans ses tailles, ce qui fait que le solide a une énergie réticulaire basse cristalline.
Solubilité
76,4 g / 100 g d'eau à 25 ° C. Cette affinité pour l'eau est due à la grande capacité de leurs molécules à résoudre les ions ammonium. D'un autre côté, il est insoluble dans l'acétone et l'alcool; c'est-à-dire dans des solvants moins polaires que l'eau.
Densité
1,77 g / cm3 à 25 ºC.
La pression de vapeur
1 871 kpa à 20 ºC.
point de rupture
26 ºC.
pH
5.0 - 6.0 (25 ºC. solution 1 m). Le pH légèrement acide est dû à l'hydrolyse NH4+ Dans l'eau, produisant H3SOIT+ à faible concentrations.
La stabilité
Stable dans des conditions environnementales adéquates. En contact avec de forts oxydants, il peut mettre le feu.
Décomposition
Il commence à se décomposer à 150 ºC, libérant des vapeurs d'oxyde de soufre toxiques, de l'oxyde d'azote et de l'ammonium.
Corrosion
N'attaque pas le fer ou l'aluminium.
Utilisations du sulfate d'ammonium
Dans l'agriculture
- Le sulfate d'ammonium est utilisé comme engrais dans les sols alcalins. Le sel d'ammonium a 21% d'azote et 24% de soufre dans sa composition. Cependant, il existe des composés qui fournissent une quantité d'azote supérieure à celle du sulfate d'ammonium; L'avantage de ce dernier est sa forte concentration de soufre.
- Le soufre est essentiel dans la synthèse des protéines, car plusieurs acides aminés - comme la cystine, la méthionine et la cystéine - ont du soufre. Pour ces raisons, le sulfate d'ammonium continue d'être l'un des engrais les plus importants.
- Il est utilisé dans le blé, le maïs, le riz, le coton, les pommes de terre, le chanvre et les arbres fruitiers.
- Le pH des sols alcalins vers le bas pour leur contribution au processus de nitrification réalisé par les microbes. L'ammonium est utilisé (NH4+) pour produire du nitrate (non3-) et libérer H+: 2NH4+ + 4e2 => 2No3- + 2h2O + 4H+. L'augmentation de la concentration d'hydrogène diminue le pH des sols alcalins et permet une utilisation plus.
- En plus de son utilisation comme engrais, le sulfate d'ammonium agit comme un adjuvant d'insecticides, d'herbicides et de fongicides solubles, qui sont pulvérisés sur les cultures.
- Le sulfate est capable d'enlèvement d'ions présents dans le sol et l'eau d'irrigation qui sont nécessaires à la vie de certains agents pathogènes. Parmi les ions que le sulfate d'ammonium capture est le CA2+, Le mg2+, foi2+ et la foi3+. Cette action améliore l'effet microbicide des agents susmentionnés.
En tant que réactif analytique
Le sulfate d'ammonium agit comme un agent précipitant dans l'analyse électrochimique, au milieu de la culture microbiologique et dans la préparation des sels d'ammonium.
Dans les précipitations et l'isolation des protéines
Le sulfate d'ammonium est utilisé dans l'isolation et la purification des protéines, en particulier le plasma. Pour le plasma, une quantité de sulfate d'ammonium est ajoutée pour le porter à une certaine concentration; Ainsi, la précipitation d'un groupe de protéines est causée.
Le précipité par centrifugation est collecté et le surnageant s'ajoute une quantité supplémentaire de sulfate d'ammonium et, à une nouvelle concentration, la précipitation d'un autre groupe de protéines est produite.
La répétition du processus précédent permet d'obtenir différentes fractions de protéines plasmatiques.
Avant que les nouvelles technologies de biologie moléculaire n'apparaissent, cette procédure a permis l'isolation des protéines plasmatiques d'une grande importance en médecine, par exemple: immunoglobulines, facteurs de coagulation, etc.
Dans l'industrie
Le sulfate d'ammonium agit en retardant le début du feu dans l'industrie textile. Il est utilisé comme additif dans l'industrie de l'électroenchapado. Il est également utilisé dans la production de peroxyde d'hydrogène, de chlorure d'ammonium, etc.
Autres utilisations
- Le sulfate d'ammonium est utilisé comme agent réglementaire de pression osmotique et comme agent précipitant des sels.
- Sous forme de sulfate d'ammonium Lauril, il diminue la tension superficielle de l'eau, permettant ainsi la séparation des polluants par une augmentation de la dureté de l'eau.
- Est un agent anticorrosif.
- Il est utilisé comme additif alimentaire qui régule l'acidité dans la pâte à farine et le pain.
- « Mission et concept de vision personnelle, comment les faire, exemples
- Salts ultérieurs quelles sont, nomenclature, propriétés, exemples »