Caractéristiques, structure et fonctions ribose
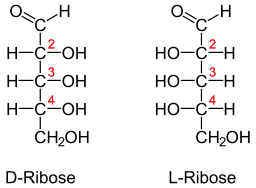
- 4535
- 1172
- Noa Da silva
La Ribosa C'est un sucre à cinq carbone qui est présent dans les ribonucléosides, les ribonucléotides et ses dérivés. Vous pouvez trouver d'autres noms tels que β-d-librounosa, d-libose et l-libose.
Les nucléotides sont les "blocs" constitutifs du squelette d'acide ribonucléique (ARN). Chaque nucléotide est composé d'une base qui peut être de l'adénine, de la guanine, de la cytosine ou de l'uracile, un groupe de phosphate et un sucre, le ribose.
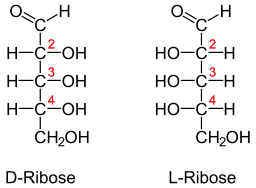 Projection de Fisher pour D et L-libose (Source: Neurotokeker [Domaine public] via Wikimedia Commons)
Projection de Fisher pour D et L-libose (Source: Neurotokeker [Domaine public] via Wikimedia Commons) Ce type de sucre est particulièrement abondant dans les tissus musculaires, où il est associé aux ribonucléotides, en particulier avec l'adénosine ou le tryphosphate d'ATP, qui est essentiel pour le fonctionnement musculaire.
Le D-Rribose a été découvert en 1891 par Emil Fischer, et depuis lors, une grande attention a été accordée à ses caractéristiques physicochimiques et à son rôle dans le métabolisme cellulaire, c'est-à-dire dans le cadre du squelette de l'acide ribonucléique, de l'ATP et de plusieurs de plusieurs coenzymes.
Au début, cela n'a été obtenu qu'à partir de l'hydrolyse de l'ARN des levures, jusqu'à ce que, dans les années 1950, il a réussi à synthétiser à partir du D-glucose en quantités plus ou moins accessibles, permettant l'industrialisation de sa production.
[TOC]
Caractéristiques
Le ribose est un aldopentosa couramment extrait comme un composé chimique pur sous la forme de d-libose. C'est une substance organique soluble dans l'eau, blanche et cristalline. Étant glucides, le ribose a des caractéristiques polaires et hydrophiles.
Le ribose est conforme à la règle commune des glucides: il a le même nombre d'atomes de carbone et d'oxygène, et deux fois cette quantité dans les atomes d'hydrogène.
À travers les atomes de carbone dans les positions 3 ou 5, ce sucre peut rejoindre un groupe de phosphate, et s'il rejoint l'une des bases azotées de l'ARN, un nucléotide se forme.
La façon la plus courante de trouver le ribose dans la nature est comme le d-libose et le 2-dexy-d-libose, ce sont des composants des nucléotides et des acides nucléiques. Le D-libose fait partie de l'acide ribonucléique (ARN) et du 2-disaxi-D-dibose de l'acide désoxyribonucléique (ADN).
Peut vous servir: protéine K: caractéristiques, activité enzymatique, applications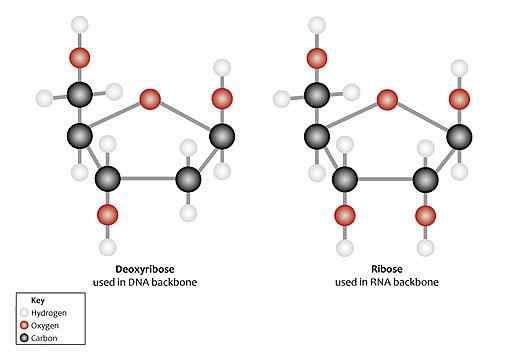 Différences structurelles entre le ribose et le désoxyribose (Source: Genomics Education Program [CC par 2.0 (https: // CreativeCommons.Org / licences / par / 2.0)] via Wikimedia Commons)
Différences structurelles entre le ribose et le désoxyribose (Source: Genomics Education Program [CC par 2.0 (https: // CreativeCommons.Org / licences / par / 2.0)] via Wikimedia Commons) Dans les nucléotides, les deux types de pentose se trouvent sous la forme β-fluanous (anneau pentagonal fermé).
En solution, le ribose libre est en équilibre entre l'aldéhyde (chaîne ouverte) et la forme cyclique β-furanonne. Cependant, l'ARN ne contient que la forme cyclique β-d-dribofuranosa. La forme biologiquement active est généralement le d-libose.
Structure
La ribosa est un sucre dérivé du glucose qui appartient au groupe Aldopentosa. Sa formule moléculaire est C5H10O5 et a un poids moléculaire de 150.13 g / mol. Puisqu'il s'agit d'un sucre monosaccharide, son hydrolyse sépare la molécule dans ses groupes fonctionnels.
Il a, comme l'indique sa formule, cinq atomes de carbone qui peuvent être trouvés cycliquement dans le cadre de cinq ou six anneaux de membres. Ce sucre a un groupe aldéhyde dans l'atome de carbone 1 et un groupe hydroxyle (-OH) dans les atomes de carbone de la position 2 à la position 5 de l'anneau Pontosa.
La molécule ribose peut être représentée dans la projection de Fisher de deux manières: d-libose ou l-libose, étant la forme l le stéréoisomère et l'énantiomère de la forme d et vice versa.
La classification de la forme D ou L dépend de l'orientation des groupes hydroxyles du premier atome de carbone après le groupe aldéhyde. Si ce groupe est orienté vers le côté droit, la molécule au nom de Fisher correspond au d-riby.
La projection de Haworth du ribose peut être représentée dans deux structures supplémentaires en fonction de l'orientation du groupe hydroxyle dans l'atome de carbone qui est anomérique. En position β, l'hydroxyle est orienté vers la partie supérieure de la molécule, tandis que la position α guide l'hydroxyle vers le bas.
Il peut vous servir: flore et faune de Santa Fe: espèces représentatives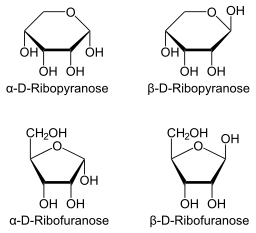 Projection de Haworth pour la ribopyranosa et la ribofuranosa (source: Neurotokeker [domaine public] via Wikimedia Commons)
Projection de Haworth pour la ribopyranosa et la ribofuranosa (source: Neurotokeker [domaine public] via Wikimedia Commons) Ainsi, selon la projection de Haworth, quatre façons possibles peuvent être prises: β-d-libose, α-d-libose, β-l-libose ou α-l-libose.
Lorsque les groupes de phosphate sont joints au ribose, ils sont généralement appelés α, β et ƴ. L'hydrolyse des nucléosides tryphosphate fournit une énergie chimique pour augmenter une grande variété de réactions cellulaires.
Les fonctions
Il a été proposé que le produit phosphate ribose de la décomposition des ribonucléotides, est l'un des principaux précurseurs du furano et des thiophénols, qui sont responsables de l'odeur caractéristique de la viande.
Dans les cellules
La plasticité chimique du ribose entraîne l'implication de la molécule dans la grande majorité des processus biochimiques à l'intérieur des cellules, certains tels que la traduction de l'ADN, la synthèse des acides aminés et des nucléotides, etc.
Le ribose agit constamment comme un véhicule chimique à l'intérieur de la cellule, puisque les nucléotides peuvent en présenter un, deux groupes de phosphate unis de manière covalente les unes avec les autres par des liaisons anhydre. Ceux-ci sont connus sous le nom de mono-, di- et triphosphate, respectivement.
Le lien entre le ribose et le phosphate est du type d'ester, l'hydrolyse de ce lien libère environ 14 kJ / mol dans des conditions standard, tandis que celle de chacune des liaisons anhydride libère environ 30 kJ / mol.
Dans les ribosomes, par exemple, le groupe 2'-hydroxyle du ribose peut former une liaison hydrogène avec les différents acides aminés, union qui permet la synthèse des protéines de l'ARNt dans tous les organismes vivants connus.
Le poison de la plupart des serpents contient de la phosphodiestérase qui hydrolyse les nucléotides de l'extrémité 3 qui ont un hydroxyle libre, brisant les syndicats entre l'hydroxyle 3 'du ribose ou du dexyribosa.
Il peut vous servir: Aérobie glycolyse: ce qui est, les réactions, les intermédiaires glycolytiquesEn médecine
Dans des contextes médicinaux, il est utilisé pour améliorer les performances et la capacité d'exercice en augmentant l'énergie musculaire. Le syndrome de fatigue chronique est également traité avec ce saccharide, ainsi que la fibromyalgie et certaines maladies de l'artère coronaire.
En termes préventifs, il est utilisé pour éviter la fatigue musculaire, les crampes, la douleur et la rigidité après l'exercice chez les patients atteints de trouble héréditaire de la carence en myoadénylate désaminase ou une carence en AMP de l'AMP désaminase.
Les références
- Alberts, B., Johnson, un., Lewis, J., Morgan, D., Raff, m., Roberts, k., & Walter, P. (2015). Biologie de la cellule moléculaire (6e Ed.). New York: Garland Science.
- Angyal, s. (1969). La composition et la conformation des sucres. Angewandte Chemie - Édition internationale, 8(3), 157-166.
- Foloppe, n., & Mackerell, un. D. (1998). Propriétés conformationnelles des fragments désoxyribose et ribose des acides nucléiques: une étude mécanique quantique, 5647(98), 6669-6678.
- Garrett, R., & Grisham, C. (2010). Biochimie (4e ed.). Boston, États-Unis: Brooks / Cole. Cengage Learning.
- Guttman, B. (2001). Nucléotides et nucléosides. Presse universitaire, 1360-1361.
- Mathews, C., Van Holde, K., & Ahern, k. (2000). Biochimie (3e érigé.). San Francisco, Californie: Pearson.
- Mottram, D. S. (1998). Formation de saveurs dans les produits de viande et de viande: une revue. chimie alimentaire, 62(4), 415-424.
- Nechamkin, h. (1958). Dérivations ethmologiques de sous-intérêt de la terminologie chimique. Terminologie chimique, 1-12.
- Nelson, D. L., & Cox, M. M. (2009). Principes de lehninger de la biochimie. Éditions Omega (5e Ed.). https: // doi.org / 10.1007 / S13398-014-0173-7.2
- Shapiro, R. (1988). Synthèse prébiotique du ribose: une analyse critique. Origines de la vie et évolution de la biosphère, 18, 71-85.
- L'index Merck en ligne. (2018). Récupéré de www.RSC.org / merck-index / monographie / m9598 / dribose?Q = Unautant
- WARIS, S., Pischetsrianer, m., & Salemuddin, m. (2010). Dommages à l'ADN par ribose: inhibition à des concentrations ribose élevées. Journal indien de biochimie et de biophysique, 47, 148-156.
- Webmd. (2018). Récupéré le 11 avril 2019 de www.Webmd.com / vitamines / ai / ingrédientmono-827 / ribose
- Wulf, p., & Vandamme, et. (1997). Synthèse microbienne de D-libose: processus de déréglementation et de fermentation métabolique. Progrès en microbiologie appliquée, 4, 167-214.
- Xu, Z., Sha, et., Liu, C., Li, s., Liang, J., Zhou, J., & Xu, H. (2016). L -Ribose isomérase et Mannose -6 -6-phosphate isomérase: Propriétés et applications pour la production de L -rabose. Microbiologie appliquée et biotechnologie, 1-9.

