Point triple
- 4636
- 300
- Paul Dumas
Quel est le triple point?
Il Point triple C'est un terme dans le domaine de la thermodynamique qui fait référence à la température et à la pression dans lesquelles il y a simultanément trois phases d'une substance dans un état d'équilibre thermodynamique. Ce point existe pour toutes les substances, bien que les conditions dans lesquelles ils sont atteints varient considérablement entre chacun.
Un triple point peut également impliquer plus d'une phase du même type pour une substance spécifique; c'est-à-dire que deux phases solides, liquides ou gaziers différentes sont observées. L'hélium, en particulier son isotope de Helio-4, est un bon exemple de triple point impliquant deux phases de fluide individuelles: le fluide normal et superflu.
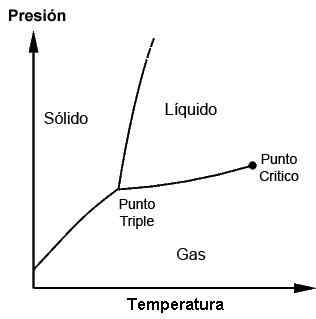
 Diagramme de phase montrant le point triple et le point critique
Diagramme de phase montrant le point triple et le point critique À quoi sert-il et quand le triple point est utilisé?
Le triple point d'eau est utilisé pour définir le Kelvin, l'unité de base de température thermodynamique dans le système des unités internationales (SI). Cette valeur est définie par définition au lieu de mesurer.
Les triples points de chaque substance peuvent être observés avec l'utilisation de diagrammes de phase, qui sont des graphiques tracés qui permettent de démontrer les conditions limitantes des phases solides, liquides et gazeuses (et autres, dans des cas spéciaux) d'une substance pendant qu'elles exercent des changements dans Température, pression et / ou solubilité.
Une substance peut être trouvée dans son point de fusion dans lequel le solide rencontre le liquide; Il peut également être trouvé à son point d'ébullition dans lequel le liquide rencontre le gaz. Cependant, c'est au triple point où les trois phases sont obtenues. Ces diagrammes seront différents pour chaque substance, comme on le verra plus tard.
Peut vous servir: Gravité de l'API: échelle et classification du brutLe point triple peut être utilisé efficacement dans l'étalonnage des thermomètres, en utilisant des cellules à point triple.
Ce sont des échantillons de substances dans des conditions isolées (dans les "cellules" de verre) qui sont à leur triple point avec des conditions de température et de pression connues, et ainsi faciliter l'étude de la précision des mesures du thermomètre.
L'étude de ce concept dans l'exploration de la planète Mars a également été utilisée, dans laquelle le niveau de la mer a été tenté pendant les missions qui ont été effectuées dans les années 1970.
Triple eau
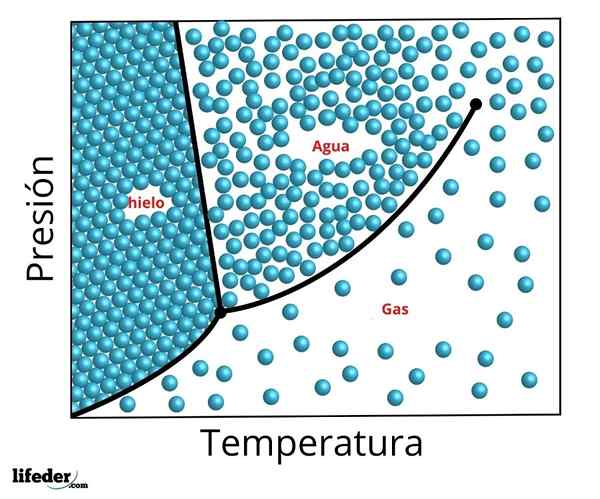 Diagramme de phase du triple point de l'eau. Le triple point est le point inférieur et le critique le point supérieur
Diagramme de phase du triple point de l'eau. Le triple point est le point inférieur et le critique le point supérieur Les conditions précises de pression et de température à laquelle l'eau coexiste dans ses trois phases en équilibre - l'eau liquide, la glace et la vapeur - se produisent à une température de 273,16 K (0,01 ºC) et une pression partielle de vapeur de vapeur 611 656 pass (0,00603659 atm ).
À ce stade, il est possible de convertir la substance en l'une des trois phases avec un minimum de changements dans sa température ou sa pression. Même lorsque la pression totale du système pourrait être située au-dessus de celle requise pour le point triple, si la pression partielle de la vapeur est à 611 656 PA, le système atteindra le point triple de la même manière.
Il est possible d'observer dans la figure précédente la représentation du triple point (ou Point triple, en anglais) d'une substance dont le diagramme est similaire à celui de l'eau, selon la température et la pression nécessaires pour atteindre cette valeur.
Dans le cas de l'eau, ce point correspond à la pression minimale à laquelle l'eau liquide peut exister. Aux pressions mineures à ce triple point (par exemple, dans un vide) et lorsqu'un chauffage à pression constante est utilisé, la glace solide se convertira directement en vapeur d'eau sans passer par liquide; Ceci est un processus appelé sublimation.
Il peut vous servir: Théorie du Big Bang: caractéristiques, étapes, preuves, problèmesAu-delà de cette pression minimale (PTp), la glace se fondera d'abord pour former de l'eau liquide, et seulement là, elle s'évaporera ou bouillonnera pour former de la vapeur.
Pour de nombreuses substances, la valeur de température à son triple point est la température minimale à laquelle la phase liquide peut exister, mais cela ne se produit pas dans le cas de l'eau. Pour l'eau, cela ne se produit pas, car le point de fusion de la glace diminue en fonction de la pression, comme indiqué avec la ligne en pointillé vert de la figure précédente.
Dans les phases à haute pression, l'eau a un diagramme de phase assez complexe, qui montre quinze phases de glace connues (à différentes températures et pressions), en plus de dix points triples différents qui sont affichés dans la figure suivante:
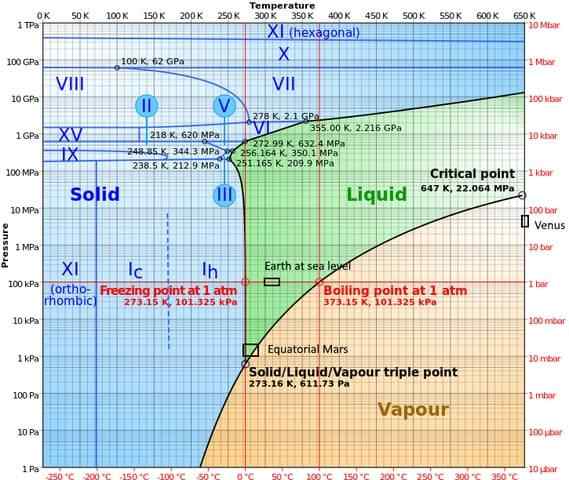
On peut noter que, dans des conditions de haute pression, la glace peut exister en équilibre avec le liquide; Le diagramme montre que les points de fusion augmentent avec la pression. À basse température constante et une pression croissante, la vapeur peut être transformée directement en glace, sans passer par la phase liquide.
Les différentes conditions qui se produisent sur les planètes où le point triple (terre en mer et dans la zone équatoriale de Mars) est également représentée dans ce diagramme).
Le diagramme indique clairement que le triple point varie en fonction de l'emplacement pour des raisons de pression et de température atmosphérique, et pas seulement par intervention de l'expérimentateur.
Triple point de cyclohexane
Le cyclohexan est un cyclocano qui a la formule moléculaire de C6H12. Cette substance a la particularité d'avoir des conditions à triple point qui peuvent être facilement reproduites, comme dans le cas de l'eau, car ce point est situé à une température de 279,47 K et une pression de 5 388 kpa.
Il peut vous servir: charges vivantes: concept, caractéristiques, exemplesDans ces conditions, le composé Hirar, se solidifiant et fusionnant avec un minimum de changements de température et de pression.
Point triple benzène
Dans un cas similaire au cyclohexan, benzène (composé organique avec formule chimique C6H6) a facilement des conditions de triple point reproductibles dans un laboratoire.
Ses valeurs sont de 278,5 K et 4,83 kPa, donc l'expérimentation avec ce niveau débutant est également courante.
Les références
- Wikipédia. (s.F.). Wikipédia. Obtenu à partir de.Wikipédia.org
- Britannica, E. (1998). Encyclopédie Britannica. Obtenu de Britannica.com
- Puissance, n. (s.F.). Power Nuclear. Obtenu à partir de puissance nucléaire.filet
- Wagner, W., Saul, un., & Prub, à. (1992). Équations internationales pour la pression le long de la fusion et le long de la courbe de sublimation de l'eau ordinaire. Bochum.
- Penoncello, s. g., Jacobsen, R. T., & Goodwin, un. R. (Année mille neuf cents quatre-vingts-quinze). À la formulation de propriété thermodynamique pour le cyclohexane.
- « Structure de sulfure d'aluminium (Al2S3), propriétés, utilisations
- La Colombie typique la plus populaire »

