Valeurs de z potentiels, degrés de coagulation, détermination, utilisations
- 2017
- 502
- Eva Henry
Il Potentiel z o Le potentiel électrocinétique est une propriété de particules en suspension colloïdales qui indiquent la taille des amplitudes de leurs charges électriques par rapport à l'environnement de dispersion. Il est représenté par la lettre grecque ζ et a des unités V ou MV.
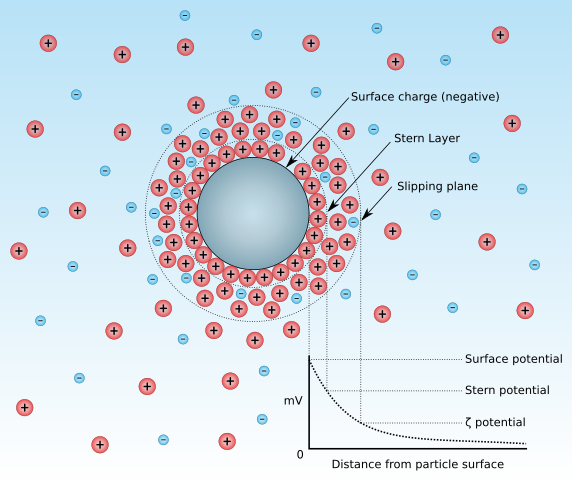
Les particules colloïdales sont généralement une charge négative associée à leur nature. Lorsque ceux-ci sont dispersés dans n'importe quel milieu, ils attirent des particules de charges positives, qui finissent par former une couche d'épaisseur des ions: la couche sévère (image inférieure).
 Source: modifié et converti en SVG par Mjones1984. Travail original de Larryisgood. / Cc by-sa (https: // creveVecommons.Org / licences / by-sa / 3.0)
Source: modifié et converti en SVG par Mjones1984. Travail original de Larryisgood. / Cc by-sa (https: // creveVecommons.Org / licences / by-sa / 3.0) À propos de cette couche fixe (Couche sévère), Selon les dimensions de la particule colloïdale, qu'elles soient solides, liquides ou soda, d'autres ions voisins seront ajoutés. La plupart d'entre eux resteront positifs, car ils subissent la grande charge négative de la particule colloïdale; Cependant, les particules négatives apparaîtront également, donnant naissance à une double couche électrique.
Au-delà de la double couche d'électricité, le milieu diffus et dispersant aura, indifférent à la charge de la particule colloïdale. Ainsi, le potentiel Z reflète à quel point cette particule est chargée devant l'environnement qui l'entoure, prenant comme référence au plan (Avion de glissement, ci-dessus) qui sépare la double couche électrique avec le reste de la solution.
[TOC]
Valeurs
Intervalles
Le potentiel z peut acquérir certaines valeurs, positives ou négatives, selon le signe de la charge que les particules colloïdales transportent. Beaucoup d'entre eux montrent des valeurs ζ dans un intervalle de -60 mV à 60 mV.
Si ζ est en dessous ou au-dessus de cette plage de valeurs, la stabilité des particules colloïdales sera excellente, ce qui signifie qu'ils resteront dispersés sans ajouter.
Pendant ce temps, les particules qui ont une valeur de ζ entre -10 mV et 10 mV seront sujettes à l'agglomérat; Tant qu'ils ne sont pas couverts par des films de molécules ancrées de manière covalente à leurs surfaces. On dit alors que l'état colloïdal est des "ruptures".
Il peut vous servir: 4 périodes de chimie: de la préhistoire jusqu'à aujourd'huiVariations
Ces valeurs doivent être rapportées avec les indications de pH et le solvant dans lequel ils ont été déterminés. Par exemple, ζ variera considérablement avec l'ajout d'un acide, car il fournit des ions H+ qui se faufilent dans la double couche qui entoure les particules. Il en résulte une augmentation positive de ζ.
Lorsque ζ a une valeur de 0, nous parlons du point isoélectrique de la solution. C'est donc la région où les particules tenteront beaucoup plus d'agglomérat. L'ajout de sels montre le même effet: les ions agrégés diminueront ou comprimeront la double couche, ayant en conséquence l'agglomération.
Degrés de coagulation
Le potentiel z est responsable des particules colloïdales de charges égales se repoussant mutuellement. On dit alors que le degré de coagulation est vide, car il n'y a aucune possibilité d'interagir.
À mesure que ces charges neutralisent, les particules commenceront à interagir à travers les forces des murs de van der, jusqu'à ce que la coagulation ait lieu.
Détermination
L'électrophorèse est une méthode utilisée pour estimer la valeur du potentiel z d'une particule en suspension.
Lorsqu'un champ électrique est appliqué, les particules chargées électriquement se déplaceront vers l'électrode qui a une charge contraire à la leur. La mobilité électrophorétique est directement liée à la vitesse de la particule en électrophorèse et inversement au gradient de tension.
Ainsi, le potentiel zêta est soumis à une mobilité électrophorétique, qui à son tour dépend de la viscosité de la solution, de la différence de tension appliquée entre les électrodes et de la constante diélectrique de la solution.
Ce déplacement est analysé par l'incidence d'un faisceau laser, dont le rayonnement est dispersé par des particules mobiles et provoque des variations de sa fréquence. Ces changements dans la fréquence du laser sont liés à la mobilité électrophorétique, et enfin, avec le potentiel z.
Peut vous servir: Aliquot (chimie)Plus la mobilité électrophorétique est grande, plus le potentiel z des particules en question est grand.
Applications
Détermination des changements superficiels
Les mesures de ζ permettent de déterminer s'il y a eu des changements superficiels dans les particules colloïdales. Comprendre par ces changements dans les interactions entre deux ou plusieurs agrégats.
Par exemple, si les particules A et B se mélangent et que ζ changent pour les deux, cela signifie qu'ils interagissent; Et donc, que leurs surfaces font l'expérience des changements en termes de charges.
Filtre des supports
La plupart des colloïdes, des particules, des bactéries et des pyrogènes sont chargés négativement. Un milieu filtre peut être modifié pour donner naissance à un potentiel Z positif.
Les éléments de filtrage avec Z Z positif ont l'avantage que les petits organismes et chargés négativement, avec des radios inférieurs à celles des microns.
L'eau déminéralisée a une échelle de pH entre 5 et 8. Par conséquent, la plupart des particules dissoutes contiennent une charge négative. Cela permet son élimination de l'eau par interaction avec le filtre de charge positif.
Traitement de l'eau
Les rivières présentent des fluctuations en peu de temps dans la qualité de l'eau qu'elles transportent. Cela détermine qu'il est nécessaire.
Il a été déterminé qu'avec une valeur de potentiel zêta entre -2,28 et + 1,2 mV dans de l'eau coagulée, de faibles turbidité et des valeurs de couleur y sont obtenues.
Il est donc possible d'obtenir un comportement optimal des processus de coagulation et / ou de floculation de l'eau, en prenant des déterminations dans l'eau coagulée du potentiel zêta comme indicateur de la déstabilisation des colloïdes et d'autres particules.
Il peut vous servir: calcogens ou amphumosLa valeur potentielle zêta a une corrélation positive avec la dose de coagulant appliquée dans la purification de l'eau.
Préparation des peintures
La dispersion des pigments de peinture est une exigence nécessaire pour obtenir un produit de bonne qualité. L'agglomération des pigments produit la formation de grains, ce qui réduit la qualité de la peinture, car ils entravent son application.
De plus, la luminosité et la texture de la peinture dépendent de la façon dont les particules qui le forment sont dispersées. La mesure potentielle de Zeta sert à contrôler la composition de la peinture, permettant aux additifs optimaux d'additifs nécessaires à une dispersion correcte de pigments.
Fluidisation d'une suspension
Carregenano est un polyhélectrolyte doté d'une charge négative qui est utilisée comme agent de fluidificateur. Les polyélectrolytes sont adsorbés à la surface des particules insolubles et inverse la floculation, dès que la valeur potentielle Z acquiert une valeur critique.
Ce système a été utilisé dans la suspension de l'hydroxyde d'aluminium antiacide. La réduction du potentiel z est corrélée avec la viscosité de la suspension.
Les références
- Betancur, C. B., Jimenez, D. M. et Linares, B. g. (2012). Potentiel Z en tant que critères d'optimisation de dosage coagulant dans la plante de traitement de l'eau potable. Dyna 79 (175): 166-172.
- Zeta-mètre. (s.F.). Potentiel Zeta: un cours complet en 5 minutes. [PDF]. Récupéré de: DEPA.Finesse.Unam.mx
- Glasstone. (1970). Traité de physicochimie. Aguilar s. POUR. des éditions, Juan Bravo, 38 ans, Madrid (Espagne).
- Walter J. Moore. (1962). Chimie physique. (Quatrième édition). Longmans.
- Nanocomposix. (2020). Mesures potentielles Zeta. Récupéré de: Nanocomposix.com
- Wikipédia. (2020). potentiel Zeta. Récupéré de: dans.Wikipédia.org
- Elsevier B.V. (2020). potentiel Zeta. Récupéré de: ScienceDirect.com
- Lentech. (2020). potentiel Zeta. Récupéré de: lentech.est
- « Les régions culturelles de l'Amérique et leurs caractéristiques
- Les 6 activités économiques de guerrier les plus remarquables »

