Niveau chimique
- 4277
- 867
- Lucas Schneider
Quel est le niveau chimique?
Le niveau chimique est l'étape la plus simple et la plus élémentaire dans laquelle la question est organisée, et comprend ce que nous comprenons par des éléments chimiques, des atomes, des molécules, etc. Parce que c'est le niveau de matière le plus élémentaire, c'est le même pour tous les coins du cosmos, en appliquant à la fois sur Terre et dans d'autres planètes et galaxies.
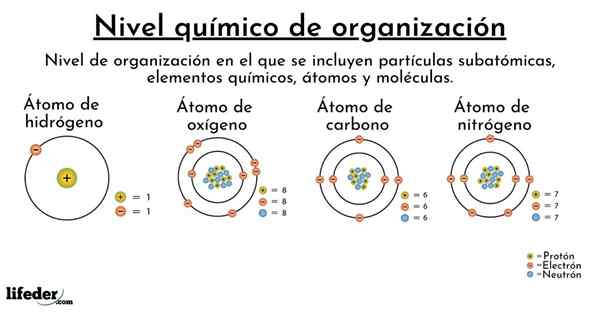
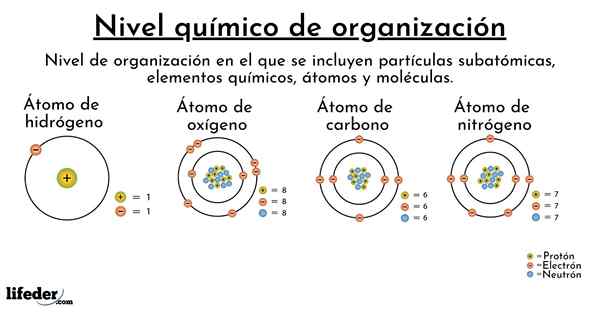
Les atomes d'hydrogène que nous avons dans le corps, par exemple, sont identiques (en ce qui concerne le noyau) à ceux trouvés dans les étoiles, comme le soleil. De même, nos atomes de carbone ne diffèrent pas de ceux qui font partie des hydrocarbures d'huile, car nous vivons ne modifie pas les noyaux ou les caractéristiques électroniques (valences) desdits atomes.
Parler du niveau chimique fait référence et voyage le tableau périodique, connaissant ses 118 éléments, les atomes de ces éléments, ses syndicats ou interactions pour provoquer des petites ou grandes molécules, puis ses agglomérations et ses connexions au niveau biologique.
Tous les êtres vivants ont en principe le même niveau chimique, qui est basé sur le carbone et l'atome d'eau, avec des variations petites mais essentielles qui définissent le phénomène de la vie; ici sur terre, et aussi hors de lui.
Caractéristiques de niveau chimique
Le niveau d'organisation chimique a plusieurs caractéristiques:
C'est invariable
Le niveau chimique est caractérisé par l'invariable, car il dépend des noyaux atomiques, qui sont responsables de la définition de l'identité d'un élément chimique.
Chaque élément a un atome avec son propre noyau personnel ou distinctif; plus petit et léger (comme l'hydrogène), et d'autres plus lourds et plus instables (comme le plomb ou l'uranium).
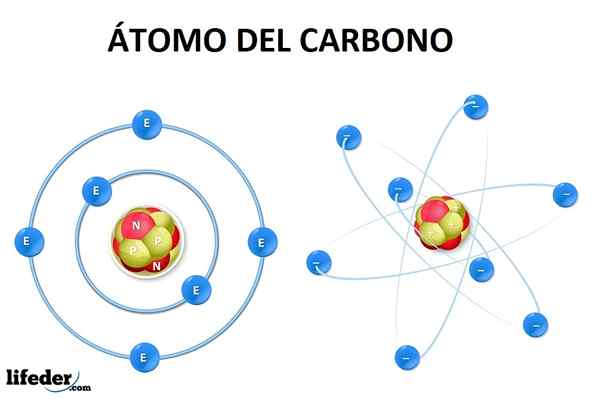
Peut vous servir: liaison covalente non polaire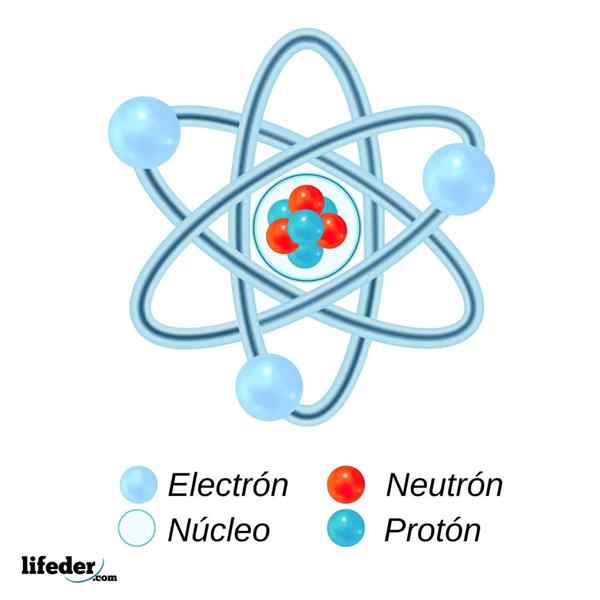 Illustration d'un atome avec ses électrons, noyau, neutrons et protons
Illustration d'un atome avec ses électrons, noyau, neutrons et protons Les noyaux atomiques, et donc les atomes des éléments sont les mêmes dans toutes les parties de l'univers. Qu'est-ce que le changement est la façon dont ils combinent ou s'unissent pour former des molécules. Et même ainsi, les molécules, bien que très variables, sont également les mêmes dans n'importe quel endroit où elles sont considérées.
Par exemple, les molécules d'eau de notre corps, h2Ou, ce sont exactement les mêmes qui ont été récemment découverts sur la lune, ou les mêmes qui sont détachés que la vapeur d'eau dans la queue des comètes.
C'est très petit
Le niveau chimique peut se manifester à différentes échelles, mais sa nature sera la même, car elle est invariable.
Revenons à l'eau. Une goutte d'eau pure, chimiquement parlant, est identique à une cascade, une rivière, un océan ou une planète entière formée par cette même eau (si nous ignorons les sels dissous, les micro-organismes ou la faune marine).
Le niveau chimique de l'eau est réduit à sa molécule H simple2Ou, qui est extraordinairement petit: il a un diamètre de 0.27 nanomètres (ce sont 0.00000000027 mètres).
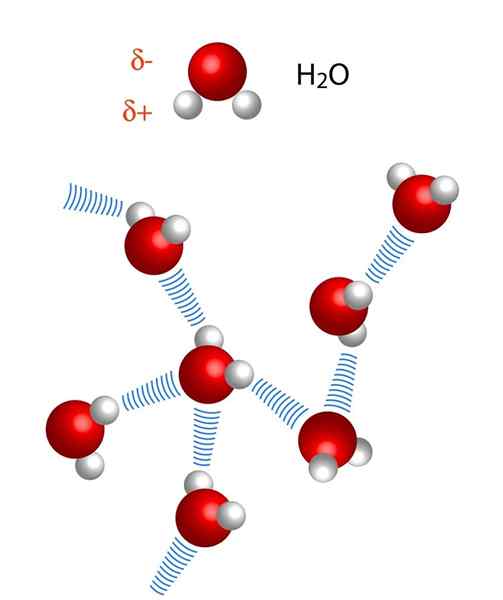 Molécule d'eau
Molécule d'eau Par conséquent, depuis les composants du niveau chimique (atomes, molécules, neutrons, etc.) Ils sont incroyablement petits, cela est toujours décrit à de très petites échelles et avec des unités telles que des nanomètres (NM) ou des picomètres (PM).
C'est déterminé
Le niveau chimique est invariable, petit et, définissant également. C'est-à-dire que le niveau chimique est responsable de la définition des propriétés physiques et chimiques des substances que nous connaissons aujourd'hui. Ce n'est pas la même chose, par exemple, une pièce de cuivre (Cu) composée d'atomes de cuivre, qu'un cristal de quartz, composé de réseaux de silice ordonnés (SIO2).
Cependant, en ce qui concerne la vie, la situation devient complexe, étant nécessaire des approches plus appropriées au niveau biologique (comme l'ADN et ses gènes).
Il peut vous servir: hydroxyde de lithium (LIOH)Est partout
 Du point de vue chimique, les étoiles, ainsi que les arbres, les insectes et les êtres humains, partagent une similitude étroite
Du point de vue chimique, les étoiles, ainsi que les arbres, les insectes et les êtres humains, partagent une similitude étroite Et enfin, le niveau chimique, comme prévu, est partout: toute manifestation de la matière est due à la masse de ses atomes.
Biologique
Le niveau chimique soutient la vie et les cellules à travers des atomes qui interagissent exceptionnellement et stables. Nous parlons d'atomes de carbone, qui sont liés pour former des chaînes ou des unités C-C difficile à briser. Nous avons également des molécules très stables telles que l'eau, qui compose 60% de notre corps.

De nombreux éléments de la table périodique se trouvent dans les êtres vivants, mais tout le monde ne joue pas un rôle essentiel pour son opération.
Par exemple, chez les êtres vivants, l'azote (N) est présent dans les protéines et les enzymes, ainsi que dans le calcium (CA) et le magnésium (mg) dans les os et les tissus, ou le potassium (k) dans les neurones, le phosphore (P) dans les molécules ATP et fer (foi) dans l'hémoglobine comme facilitateur du transport de l'oxygène à travers le sang.
Exemples du niveau chimique d'organisation
Clarifié quel est le niveau chimique et ses caractéristiques, ses «étapes internes» ou sous-niveaux seront mentionnés, et quelques exemples de chacun.
Subatomique
Dans le sous-niveau subatomique, nous avons des particules plus petites que le même atome. Parmi eux, nous avons les protons (positifs), les neutrons (neutres) et les électrons (négatifs). Les protons et les neutrons intègrent le noyau atomique, tandis que les électrons orbitent à de grandes vitesses autour du noyau.
Atomique
Dans le sous-niveau atomique, nous avons les atomes, et donc les 118 éléments du tableau périodique. Ainsi, par exemple, un atome avec un seul proton et un électron correspond à celui de l'élément hydrogène (H). Nous avons également des atomes d'hélium (HE), du lithium (LI), du béryllium (BE), du bore (B), du carbone (C), de l'azote, de l'oxygène (O), du fluor (F), du néon (NEON (NE), du sodium ( na), etc.
Peut vous servir: Oxyde d'étain (II): structure, propriétés, nomenclature, utilisationsMoléculaire
Les molécules se combinent ou se joignent à des liaisons covalentes dans lesquelles les électrons de leurs couches les plus externes (ceux de Valence) participent (ceux de Valence).
De cette façon, des molécules telles que l'hydrogène surgissent, H2, oxygène, ou2 (O = o), ou celui de l'azote, n2 (N≡n). Il existe des millions de molécules, qui étudient différentes branches de chimie (comme inorganiques et organiques).
Macromoléculaire
L'un des derniers sièges du niveau chimique est le sous-niveau macromoléculaire. Ici, nous avons les plus grandes molécules, dont beaucoup sont dans des êtres vivants; c'est-à-dire que certains peuvent être appelés biomolécules. Parmi eux nous avons:
- Polysaccharides, comme le glycogène.
- Protéines, comme l'insuline.
- Acides nucléiques, comme l'ARN.
- Lipides, tels que les phospholipides et les glucolipides.
Les macromolécules sont agglomérat pour former des supramolécules, qui à leur tour construisent les différents compartiments qui composent les cellules (organites).
Dès lors, nous touchons les portes du niveau biologique, qui est basé sur le niveau chimique: ils ne sont pas divorcés, mais entrelacés, plus que vous ne pouvez croire.
Les références
- Whitten, Davis, Peck & Stanley. (2008). Chimie. (8e Ed.). Cengage Learning.
- Académie Khan. (2021). Matière, éléments et atomes. Récupéré de: Khanacademy.org
- María Estela Raffino. (16 juillet 2020). Niveaux d'organisation du sujet. Récupéré de: concept.de
- Ana Zita. (2021). Niveaux d'organisation du sujet. Récupéré de: Todamaateria.com
- Joshua Halpern. (5 septembre 2020). Classification de la matière. CHIMISTER BOOLISTexts. Récupéré de: Chem.Bibliothèque.org