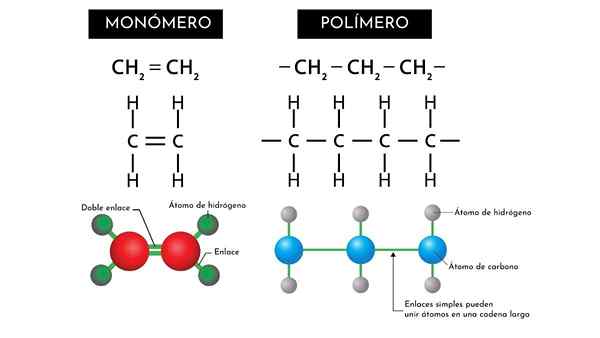
Monomère
- 4301
- 901
- Mlle Ambre Dumont
 Le monomère est une molécule de masse moléculaire liée à d'autres monomères par des liaisons chimiques
Le monomère est une molécule de masse moléculaire liée à d'autres monomères par des liaisons chimiques Que sont les monomères?
Les monomère Ce sont des molécules petites ou simples qui constituent l'unité structurelle de base ou essentielle de molécules plus grandes ou complexes appelées polymères. Le monomère est un mot d'origine grecque qui signifie chignon, un et Simple, partie.
Alors qu'un monomère rejoint un autre, un dimère se forme. En rejoignant cela tour à tour avec un autre monomère, il forme un trimère, etc., pour former de courtes chaînes appelées oligomères, ou chaînes plus longues, qui sont les polymères si appelés.
Les monomères se lient ou polymérisent en formant des liaisons chimiques en partageant des paires d'électrons; c'est-à-dire qu'ils se joignent par des liens covalents.
Cette union des monomères est connue sous le nom de polymérisation. Les monomères du même type ou différent peuvent être joints, et le nombre de liaisons covalentes qu'ils peuvent établir avec une autre molécule détermineront la structure du polymère qui se forment (chaînes linéaires, inclinées ou structures à trois dimensions).
Il existe une grande variété de monomères, parmi lesquels sont ceux d'origine naturelle. Ceux-ci appartiennent et conçoivent les molécules organiques appelées biomolécules, présentes dans la structure des êtres vivants.
Par exemple, les acides aminés qui forment des protéines; Les unités monosaccharides en glucides et mononucléotides qui forment des acides nucléiques. Il existe également des monomères synthétiques, qui permettent d'élaborer une innombrable variété de produits polymères inertes, tels que des peintures ou des plastiques.
Caractéristiques des monomères
Les monomères se lient par les liaisons covalentes
Les atomes qui participent à la formation d'un monomère restent unis par des liens solides et stables tels que le lien covalent. De même, les monomères polymérisent ou se lient à d'autres molécules monomères à travers ces liens, en donnant la force et la stabilité aux polymères.
Ces liaisons covalentes entre les monomères peuvent être formées par des réactions chimiques qui dépendront des atomes qui composent le monomère, la présence de doubles liaisons et d'autres caractéristiques qui présentent la structure du monomère.
Le processus de polymérisation peut être donné par l'une des trois réactions suivantes: par condensation, addition ou radicaux libres. Chacun d'eux implique ses propres mécanismes et mode de croissance.
Fonctionnalité monomère et structure de polymère
Un monomère peut être rejoint avec au moins deux autres molécules monomères. Cette propriété ou cette caractéristique est ce que l'on appelle la fonctionnalité des monomères, et c'est ce qui leur permet d'être les unités structurelles des macromolécules.
Il peut vous servir: nitrite de potassium (KNO2): structure, propriétés et utilisationsLes monomères peuvent être bifonctionnels ou polyifonctionnels, selon les sites actifs ou réactifs du monomère; c'est-à-dire des atomes de la molécule qui peuvent participer à la formation de liaisons covalentes avec les atomes d'autres molécules ou monomères.
Cette caractéristique est également importante, car elle est étroitement liée à la structure des polymères qui se conforment, comme détaillé ci-dessous.
Bifonctionnalité: polymère linéaire
Les monomères sont bifonctionnels lorsqu'ils n'ont que deux sites syndicaux avec d'autres monomères; C'est-à-dire que le monomère ne peut former que deux liaisons covalentes avec d'autres monomères et former uniquement des polymères linéaires.
Parmi les polymères linéaires, l'éthylen glycol et les acides aminés peuvent être mentionnés comme exemple.
Monomères polyifonctionnels - polymères à trois dimensions
Il y a des monomères qui peuvent être joints à plus de deux monomères et constituent les unités structurelles de plus grande fonctionnalité.
Ils sont appelés polyifonctionnels et sont ceux produits par des macromolécules polymères ramifiées, réseau ou trois dimensions; Comme le polyéthylène, par exemple.
Squelette ou structure centrale
Avec double liaison entre le carbone et le carbone
Il y a des monomères qui présentent dans leur structure un squelette central formé d'au moins deux atomes de carbone unis par une double liaison (c = c).
À son tour, cette chaîne ou structure centrale présente des atomes unis latéralement qui peuvent changer en formant un monomère différent (R2C = cr2).
Si l'une des chaînes R est modifiée ou remplacée, un monomère différent est obtenu. De plus, lorsque ces nouveaux monomères rejoindront un polymère différent.
Il peut être mentionné comme un exemple de ce groupe de monomères le propylène (H2C = ch3H), tétrafluoroéthylène (f2C = cf2) et le chlorure de vinyle (H2C = CCLH).
Deux groupes fonctionnels dans la structure
Bien qu'il y ait des monomères qui ont un seul groupe fonctionnel, il existe un large groupe de monomères qui ont deux groupes fonctionnels dans leur structure.
Les acides aminés en sont un bon exemple. Ils ont un groupe fonctionnel amino (-nh2) et le groupe fonctionnel de l'acide carboxylique (-COOH) unis à un atome de carbone central.
Cette caractéristique d'être un monomère diffonctionnel lui donne également la capacité de former de longues chaînes de polymères, comme la présence de doubles liens.
Groupes fonctionnels
En général, les propriétés présentées par les polymères sont données par les atomes qui forment les chaînes latérales des monomères. Ces chaînes constituent les groupes fonctionnels de composés organiques.
Peut vous servir: loi de plusieurs proportionsIl existe des familles de composés organiques dont les caractéristiques sont données par des groupes fonctionnels ou des chaînes latérales. À titre d'exemple, le groupe fonctionnel d'acide carboxylique R-COOH, le groupe amino R-NH2, L'alcool R-OH, entre autres qui participent à des réactions de polymérisation.
Union des monomères égaux ou de types différents
Union de monomères égaux
Les monomères peuvent former différentes classes de polymères. Ils peuvent rejoindre des monomères égaux ou le même type et générer les homopolymères si appelés.
À titre d'exemple, vous pouvez mentionner l'étirement, un monomère qui forme le polystyrène. L'amidon et la cellulose sont également des exemples d'homopolymères formés par de longues chaînes ramifiées du monomère de glucose.
Union de différents monomères
L'union de différents monomères forment les copolymères. Les unités sont répétées en nombre, un ordre ou une séquence différents à travers la structure des chaînes polymères (a-b-b-b-a-a-b-a-a-……).
À titre d'exemple de copolymères, le nylon peut être mentionné, un polymère formé par des unités répétitives de deux monomères différents. Ce sont de l'acide dicarboxylique et une molécule de diamine, qui se lie par condensation dans des proportions équimolaires (égales).
Différents monomères peuvent également être rejoints dans une proportion inégale, comme le cas de la formation d'un polyéthylène spécialisé qui a comme structure de base le monomère à 1 octone plus le monomère d'éthylène.
Types de monomères
Il existe de nombreuses caractéristiques qui permettent d'établir plusieurs types de monomères, parmi lesquels leur origine, leur fonctionnalité, leur structure, le type de polymère qu'ils forment, comment ils polymérisent et leurs liaisons covalentes se démarquent.
Monomères naturels
- Il existe des monomères d'origine naturelle comme l'isoprène, qui est obtenu à partir de la sève ou du latex des plantes, et qui est également la structure monomère du caoutchouc naturel.
- Certains acides aminés produits par les insectes forment du fibroine ou une protéine de soie. Ce sont également des acides aminés qui forment le polymère de kératine, qui est la protéine de laine produite par des animaux tels que des moutons.
- Parmi les monomères naturels figurent les unités structurelles de base des biomolécules. Le monosaccharide de glucose, par exemple, rejoint d'autres molécules de glucose pour former différents types de glucides tels que l'amidon, le glycogène, la cellulose, entre autres.
- Les acides aminés, en revanche, peuvent former une large gamme de polymères appelés protéines. En effet, il existe vingt types d'acides aminés, qui peuvent être liés dans n'importe quel ordre arbitraire; Et par conséquent, ils finissent par former l'une ou l'autre protéine avec leurs propres caractéristiques structurelles.
- Les mononucléotides, qui forment les macromolécules appelées acides nucléiques ADN et ARN respectivement, sont également des monomères très importants dans cette catégorie.
Monomères synthétiques
- Parmi les monomères artificiels ou synthétiques (qui sont nombreux), certains peuvent être mentionnés avec lesquels différentes variétés de plastiques sont élaborées, comme le chlorure de vinyle, qui forme le chlorure ou le polyvinil PVC; et le gaz d'éthylène (H2C = ch2), et son polymère en polyéthylène. Il est bien connu qu'avec ces matériaux, vous pouvez construire une grande variété de conteneurs, de bouteilles, d'objets domestiques, de jouets, de matériaux de construction, entre autres.
- Le monomère tétrafluoroéthylène (F2C = cf2) forme le polymère appelé et commercialement connu sous le nom de téflon.
- La molécule de caprolactam dérivée du toluène est essentielle pour la synthèse en nylon, entre autres.
- Il existe plusieurs groupes de monomères acryliques qui sont classés en fonction de la composition et de la fonction. Parmi ceux-ci figurent l'acrylamide et le métacrylamide, l'acrylate, l'acrylique avec du fluor, entre autres.
Monomères apolaires et polaires
Cette classification est effectuée en fonction de la différence d'électronégativité des atomes qui forment le monomère. Lorsqu'il y a une différence notable, des monomères polaires se forment; Par exemple, les acides aminés polaires tels que la treonine et l'asparagine.
Lorsque la différence d'électronégativité est nulle, les monomères sont apolaires. Il existe des acides aminés non polaires tels que le tryptophane, l'alanine, la valine, entre autres; et aussi des monomères apolaires comme l'acétate de vinyle.
Monomères cycliques ou linéaires
Selon la forme ou l'organisation des atomes dans la structure des monomères, ceux-ci peuvent être classés comme des monomères cycliques, tels que la proline ou l'oxyde d'éthylène; et linéaire ou aliphatique, comme l'acide aminé valine ou l'éthylène glycol, entre autres.
Exemples de monomères
En plus de ceux déjà mentionnés, il existe les exemples supplémentaires suivants de monomères:
- Formaldéhyde
- Furfural
- Cardanol
- Galactose
- Extensible
- Alcool polyvinylique
- Isoprène
- Les acides gras
- Époxydes
- Et bien qu'ils n'aient pas été mentionnés, il y a des monomères dont les structures ne sont pas gazeuses, mais sulfurisées, phosphorées ou ont des atomes de silicium.
Les références
- Carey F. (2006). Chimie organique. (6e. élégant.). Mexique: Mc Graw Hill.
- Les éditeurs de l'Encyclopedia Britannica (2015). Monomère: composé chimique. Tiré de: Britannica.com
- Mathews, Holde et Ahern (2002). Biochimie (3e. élégant.). Madrid: Pearson
- Polymères et monomères. Récupéré de: matériauxworldmodules.org
- Wikipedia (2018). Monomère. Pris de: dans.Wikipédia.org

