Caractéristiques de la lysine, structure, fonctions, biosynthèse
- 2784
- 743
- Raphaël Meyer
La lysine (Lys, K) ou la acide ε-diaminoproïque, C'est l'un des 22 acides aminés qui font.
Il a été découvert par Drechsel en 1889 comme produit d'hydrolyse (décomposition) de casinogène. Des années plus tard, Fischer, Siegfried et Hedin ont déterminé qu'il faisait également partie de protéines telles que la gélatine, l'albumine d'oeuf, la conglutine, la fibrine et d'autres protéines.
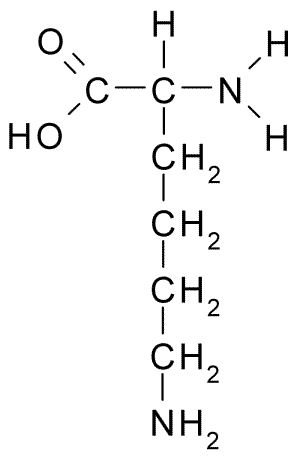
 Structure chimique de la lysine en acide aminé (source: borb, via Wikimedia Commons)
Structure chimique de la lysine en acide aminé (source: borb, via Wikimedia Commons) Son événement a ensuite été démontré dans les semis de graines en germination et dans la plupart des protéines végétales examinées, ce qui a déterminé leur abondance en tant qu'élément constituant général de toutes les protéines cellulaires.
Il est considéré comme l'un des principaux acides aminés "limitants" dans les régimes riches en céréales et, pour cette raison, on pense que la qualité de la teneur en protéines consommée par les différentes populations sous-développées du monde est affectée.
Certaines études ont déterminé que la consommation de lysine favorise la production et la libération d'insuline et les hormones glucagon, qui ont des effets importants sur le métabolisme énergétique du corps.
[TOC]
Caractéristiques
La lysine est un acide α-amino chargé positivement.53, qui implique que, le pH physiologique, votre groupe amino substituant est complètement ionisé, conférant une charge nette positive à l'acide aminé.
Son occurrence dans les protéines de différents types d'organismes vivants est proche de 6% et que divers auteurs considèrent que la lysine est essentielle pour la bonne croissance et la réparation des tissus.
Les cellules ont beaucoup de dérivés de lysine, qui remplissent une grande diversité de fonctions physiologiques. Dans ce sont l'hydroxilisine, la méthyl-lysine et autres.
Il s'agit d'un acide aminé cétogène, qui implique que son métabolisme produit des squelettes carbonatés de substrats intermédiaires pour des voies de formation de molécules telles que l'acétyl-CoA, avec la formation ultérieure de corps cétone dans le foie.
Contrairement à d'autres acides aminés essentiels, ce n'est pas un acide aminé glycogène. En d'autres termes, sa dégradation ne se termine pas par la production d'intermédiaires de routes qui produisent du glucose.
Structure
La lysine est classée dans le groupe d'acides aminés de base, dont les chaînes latérales ont des groupes ionisables avec des charges positives.
Sa chaîne latérale ou le groupe R R a un deuxième groupe amino primaire attaché à l'atome de carbone en position ε de sa chaîne aliphatique, d'où son nom «ε-aminocaproïco».
Il a un atome de carbone α, auquel un atome d'hydrogène, un groupe amino, un groupe carboxyle et la chaîne latérale r, caractérisée par la formule moléculaire (-ch2-ch2-ch2-ch2-nh3 +) sont jointes.
Puisque la chaîne latérale a trois groupes de méthylène, et bien que la molécule de lysine ait un groupe amino avec une charge positive au pH physiologique, ce groupe R a un fort caractère hydrophobe, il est donc souvent «enfoui» dans les structures protéiques, ne laissant que le ε- groupe amino.
Le groupe amino de la chaîne latérale de la lysine est très réactif et participe généralement aux centres actifs de nombreuses protéines à activité enzymatique.
Les fonctions
La lysine, étant un acide aminé essentiel, remplit de multiples fonctions telles que le micronutriment, en particulier chez l'homme et d'autres animaux, mais il est également métabolite dans différents organismes tels que les bactéries, les levures, les plantes et les algues.
Les caractéristiques de sa chaîne latérale, en particulier celles du groupe ε-amino attachées à la chaîne d'hydrocarbures qui est capable de former des ponts d'hydrogène, lui donnent des propriétés spéciales qui la font participer à des réactions catalytiques dans divers types d'enzymes.
Il peut vous servir: flore et faune de zacatecas: espèces plus représentativesIl est très important pour la croissance normale et le remodelage des muscles. De plus, il s'agit d'une molécule précurseur pour la carnitine, un composé synthétisé dans le foie, le cerveau et les reins responsables du transport des acides gras vers les mitochondries pour la production d'énergie.
Cet acide aminé est également nécessaire pour la synthèse et la formation de collagène, une protéine importante du système de tissu conjonctif dans le corps humain, donc elle contribue au maintien de la structure de la peau et des os.
Il a des fonctions expérimentalement reconnues dans:
- La protection des intestins contre les stimuli stressants, la contamination par des agents pathogènes bactériens et viraux, etc.
- Diminuer les symptômes d'anxiété chronique
- Favoriser la croissance des nourrissons qui se développent sous des régimes de faible qualité
Biosynthèse
Les êtres humains et autres mammifères ne peuvent pas synthétiser la lysine acide aminé In vivo Et c'est pour cette raison qu'ils doivent l'obtenir à partir de protéines animales et végétales ingérées avec de la nourriture.
Dans le monde naturel, deux routes différentes ont évolué pour la biosynthèse de la lysine: une qui utilise des bactéries, des plantes et des champignons "inférieurs» et un autre utilisé par Euglénides et "supérieurs".
Biosynthèse de la lysine chez les plantes, les champignons inférieurs et les bactéries
Dans ces organismes, la lysine est obtenue à partir de l'acide diaminéopimélique par une voie à 7 étapes qui commence par le pyruvate et l'aspartate éthique semi-éthique. Pour les bactéries, par exemple, cette voie implique la production de lysine à des fins de (1) synthèse des protéines, (2) synthèse de diaminopimellate et de synthèse de (3) lysine qui sera utilisée dans la paroi cellulaire de la pepidoglin.
L'aspartate, dans les organismes qui présentent cette voie non seulement à l'origine de Lisina, mais dérive également dans la production de métification et de treonine.
L'itinéraire Diverge en semi-carré ASP.
Biosynthèse de la lysine dans les champignons supérieurs et Euglénidos
Synthèse de lysine de Novo Dans les champignons supérieurs et les micro-organismes d'Euglénide, il se produit par l'intermédiaire L-α-aminoadipato, qui est transformé de nombreuses fois de différentes manières à celles qui se déroulent dans les bactéries et les plantes.
L'itinéraire se compose de 8 étapes enzymatiques, qui impliquent 7 intermédiaires libres. La première moitié de l'itinéraire se déroule dans les mitochondries et atteint la synthèse de l'α-aminoadipato. La conversion de l'α-aminoadipato dans la L-lisin se produit plus tard dans le cytosol.
- La première étape de l'itinéraire se compose de la condensation des molécules α-cétoglutarate et acétyl-CoA par l'homochitrate enzymatique synthase, qui donne l'acide homocitrique.
- L'acide homocitrique est déshydraté dans l'acide Cis-homoaconitique, qui est ensuite converti en acide homoisocitrique par une enzyme homoaconitasa.
- L'acide homoisocitrique est oxydé par l'homoisocytrate déshydrogénase, qui atteint la formation d'oxyglutarate transitoire, qui perd une molécule de dioxyde de carbone (CO2) et se termine sous forme d'acide α-catoadipique.
- Ce dernier composé est transaminé par un processus dépendant du glutamate grâce à l'action de l'enzyme aminotransférase aminoadipate, qui produit de l'acide L-α-aminoaadipie.
- La chaîne latérale de l'acide L-α-aminoadipique est réduite pour former du L-α-aminoadipic-Δ-semi-assess.
- Sacoopine réductase puis catalyz. Par la suite, l'imino est réduit et la sacoopine est obtenue.
- Enfin, la liaison en carbone-nitrogen dans la partie glutamate de la sacaopine est "coupée" par l'enzyme de la sacraopine déshydrogénase, se rendant comme produits finaux L-lisin et α-zétoglutarate acide.
Alternatives à la lysine
Les tests expérimentaux et l'analyse effectués avec des rats dans une période de croissance ont permis d'élucider que le ε-N-L'acétyl-lysine peut remplacer la lysine pour soutenir la croissance des jeunes et cela grâce à la présence d'une enzyme: ε-lisin acilase.
Il peut vous servir: zone affotique: caractéristiques, flore, fauneCette enzyme catalyse l'hydrolyse du ε-N-acétyl-lysine pour produire de la lysine et fait si rapidement et en quantités abondantes.
Dégradation
In all mammal species, the first step in lysine degradation is catalyzed by the lysine-2-oxoglutarate enzyme reductase, capable of converting lysine and α-oxoglutarate into sacalopine, an amino acidic derivative present in animal physiological fluids and whose existence in them was demonstrated À la fin des années 60.
La sacroopine est de retour à α-aminoadipato δ-semialdehid et au glutamate par l'action de l'enzyme de la sacaropine déshydrogénase. Une autre enzyme est également capable d'utiliser la sacaropina comme substrat pour hydrolyz.
La sacaropine, l'un des principaux intermédiaires métaboliques de la dégradation de la lysine, a un taux de remplacement, dans des conditions physiologiques, extrêmement élevés, de sorte qu'il ne s'accumule pas dans les fluides ou les tissus, qui ont été démontrés par les activités élevées trouvées du développeur déshydrogénase.
Cependant, la quantité et l'activité des enzymes impliquées dans le métabolisme de la lysine dépend, dans une large mesure, sur divers aspects génétiques de chaque espèce particulière, car il existe des variations intrinsèques et des mécanismes de contrôle ou de régulation spécifiques.
"Sacaropinurie"
Il existe une condition pathologique liée à la perte abondante d'acides aminés tels que la lysine, la citruline et l'histidine à travers l'urine et c'est ce qu'on appelle la "Saropinurie". La sacaropine est un dérivé d'acides aminés du métabolisme de la lysine qui est excrété avec les trois acides aminés mentionnés dans l'urine de patients "saropinuriques".
La sacaropine a été initialement découverte dans la levure de bière et est un précurseur de la lysine dans ces micro-organismes. Dans d'autres organismes eucaryotes, ce composé est produit lors de la dégradation de la lysine dans les mitochondries des hépatocytes
Aliments riches en lysine
La lysine est obtenue de la nourriture consommée avec le régime alimentaire et un être humain adulte moyen a besoin d'au moins 0.8 g de ce jour. Il se trouve dans de nombreuses protéines d'origine animale, en particulier dans les viandes rouges telles que la vache, l'agneau et le poulet.
Il se trouve dans des poissons comme le thon et le saumon et dans les fruits de la mer comme les huîtres, les crevettes et les moules. Il est également présent dans les protéines constituantes des produits laitiers et de leurs dérivés.
Dans les aliments végétaux se trouvent dans les pommes de terre, dans les poivrons et dans les poireaux. Il est également dans les avocats, les pêches et les poires. Dans les légumineuses telles que les haricots d'arriñonados, les pois chiches et le soja; dans les graines de citrouille, dans les noix de la macadamia et dans les anacardos (Merey, Marañón, etc.).
Avantages de votre apport
Cet acide aminé est inclus dans de nombreux médicaments de formulation nutraceutique, c'est-à-dire isolés de composés naturels, en particulier des plantes.
Il est utilisé comme anticonvulsif et son efficacité a également été démontrée dans l'inhibition de la réplication du Virus herpes simplex Type 1 (HSV-1), qui se manifeste généralement en moments de stress, lorsque le système immunitaire est déprimé ou "affaibli" comme des ampoules ou de l'herpès sur les lèvres.
L'efficacité des suppléments de L-lisine pour le traitement de l'herpès des lèvres est due au fait que cette "concurrence" ou "bloque" l'arginine, une autre acide aminé protéique, qui est nécessaire pour la multiplication du HSV-1.
Il a été déterminé que la lysine a également des effets anti-intoolitiques, car il aide à bloquer les récepteurs qui sont impliqués dans les réponses à différents stimuli stressants, en plus de participer à la diminution des niveaux de cortisol, "hormone de stress".
Certaines études ont indiqué qu'elle peut être utile pour l'inhibition des tumeurs cancérigènes, pour la santé des yeux, pour le contrôle de la pression artérielle, entre autres.
Peut vous servir: Médias de culture: histoire, fonction, types, préparationDans les animaux
Une stratégie commune pour traiter les infections du virus de l'herpès I dans les félines est la supplémentation en lysine. Cependant, certaines publications scientifiques établissent que cet acide aminé n'a pas, chez les félines, pas de propriété antivirale, mais agit plutôt en diminuant la concentration d'arginine.
Dans la santé des nourrissons
L'apport expérimental de L-Lisina, ajouté dans le lait nourrisson pendant la période d'allaitement, s'est avéré bénéfique pour le gain de la masse corporelle et l'induction de l'appétit chez les enfants pendant les premières étapes du développement postnatal.
Cependant, l'excès de L-lisine peut provoquer des excrétions urinaires exagérées des acides aminés, à la fois neutres et de base des caractéristiques, ce qui entraîne un déséquilibre corporel.
L'excès de supplémentation en L-lisine peut se terminer par la répression de la croissance et d'autres effets histologiques évidents dans les organes importants, probablement en raison de la perte d'acides aminés avec l'urine.
Dans la même étude, il a également été mis en évidence que la supplémentation en lysine améliore les propriétés nutritionnelles des protéines végétales ingérées.
D'autres études similaires menées chez des adultes et des enfants des deux sexes du Ghana, de la Syrie et du Bangladesh ont fait ressortir les propriétés bénéfiques de l'apport de lysine pour réduire la diarrhée chez les enfants et certaines conditions respiratoires mortelles chez les hommes adultes chez les hommes.
Troubles de la carence en lysine
La lysine est, comme tous les acides aminés essentiels et non essentiels, nécessaires à la synthèse correcte des protéines cellulaires qui contribuent à la formation de systèmes organiques corporels.
Des carences marquées en lysine dans l'alimentation, car il s'agit d'un acide aminé essentiel qui n'est pas produit par le corps, peut entraîner le développement de peintures anxieuses médiées par la sérotonine, en plus de la diarrhée, également liée aux récepteurs de la sérotonine.
Les références
- Bol, s., & Bunnik, et. M. (2015). La supplication de la lysin n'est pas efficace pour la prévention ou le traitement de l'infection féline de l'herpèsvirus 1 chez les chats: une revue systématique. BMC Research vétérinaire, onze(1).
- Carson, N., Scally, B., Neill, D., & Carré, je. (1968). Saccharopinurie: une nouvelle erreur innée du métabolisme de la lysine. Nature, 218, 679.
- Colina R, J., Díaz E, M., Manzanilla m, l., Araque m, h., Martínez G, G., Rossini V, M., & Jerez-Timaure, n. (2015). Évaluation des niveaux de lysine digestibles dans les régimes alimentaires à haute densité d'énergie pour finir les porcs. MVZ Córdoba Magazine, vingt(2), 4522.
- Fellows, B. F. C. Toi., & Lewis, M. H. R. (1973). Métabolisme de la lysine chez les mammifères. Journal biochimique, 136, 329-334.
- Fornazier, R. F., Azevedo, R. POUR., Ferreira, R. R., & Varisi, V. POUR. (2003). Catabolisme de la lysine: flux, rôle métabolique et régulation. Journal brésilien de physiologie végétale, quinze(1), 9-18.
- Ghosh, s., Smriga, m., Vuvor, f., Suri, D., Mohammed, h., Armah, s. M., & Scrimshaw, n. S. (2010). Effet de la supplication de la lysine sur la santé et la morbidité chez les sujets appartenant à de mauvais ménages périurbains à Accra, au Ghana,. American Journal of Clinical Nutrition, 92(4), 928-939.
- Hutton, C. POUR., Pérugini, m. POUR., & Gerrard, J. POUR. (2007). Inhibition de la biosynthèse de la lysine: une stratégie antibiotique en évolution. Biosystèmes moléculaires, 3(7), 458-465.
- KALOGEROPOUL, D., Lafave, L., Schweim, k., Gannon, m. C., & Nuttall, f. Q. (2009). L'ingestion de lysine atténue considérablement la réponse du glucose au glucose ingéré sans changement dans la réponse à l'insuline. American Journal of Clinical Nutrition, 90(2), 314-320.
- Nagai, h., & Takeshita, s. (1961). Effet nutritionnel de la supplémentation en L-lysine sur la croissance des nourrissons et des enfants. Pédiatrie japonaise, 4(8), 40-46.
- O'Brien, S. (2018). Healthline. Récupéré le 4 septembre 2019 de www.Healthline.com / nutrition / lysine-benefits
- Zabriskie, t. M., & Jackson, m. D. (2000). Biosynthèse et métabolisme de la lysine chez les champignons. Rapports de produits naturels, 17(1), 85-97.
- « Les 25 pirates les plus célèbres de l'histoire
- Mécanismes de défense de Freud et de psychanalyse (exemples) »

