Principe et droit de formule de Raault, exemples, exercices
- 3082
- 37
- Noa Da silva
La Loi de Rauolt C'est celui qui est utilisé pour expliquer la descente ou la réduction de la pression de la vapeur, présente sur une solution, en raison de la dissolution d'un soluté non volatile, comme un sel ou un composé organique.
Cette loi est également utilisée pour analyser et décrire la composition de solvants volatils dans la phase gazeuse, situé dans l'espace sur une solution qui en présente un mélange. La loi porte son nom en l'honneur de son créateur, François-Marie Rauolt (1830-1901).
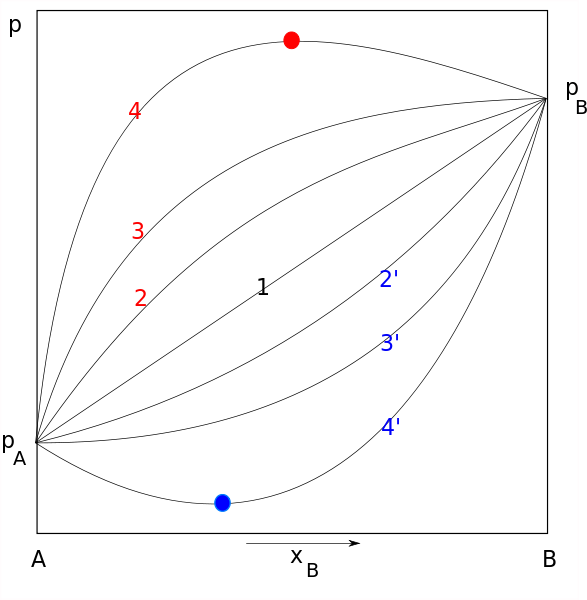
 Diagrammes de la loi de Raault. La ligne 1 représente le comportement idéal, tandis que le rouge et le bleu correspondent à des écarts positifs et négatifs, respectivement. Source: Joanna Kośmider / Domaine public
Diagrammes de la loi de Raault. La ligne 1 représente le comportement idéal, tandis que le rouge et le bleu correspondent à des écarts positifs et négatifs, respectivement. Source: Joanna Kośmider / Domaine public La loi de Rauolt s'applique aux solutions idéales conformes à certaines caractéristiques, y compris celles suivantes: les forces intermoléculaires entre les molécules égales (forces cohésives) doivent être égales aux forces intermoléculaires entre des molécules différentes ou différentes (forces adhésives).
De nombreuses solutions ne sont pas idéales, ce qui explique les écarts de la loi de Rauolt observés dans certains mélanges de solvants volatils. Par exemple, le mélange de chloroforme (ch3Cl) et acétone (choisissez3Coch3), présente un écart négatif par rapport à la loi de Raoul.
 François-Marie Raault
François-Marie Raault La pression de vapeur dans la phase gazeuse dans de tels cas est inférieure à celle prévue par la loi, explicable par la formation de ponts d'hydrogène entre les composants du mélange.
[TOC]
Principe et formule
La loi de Rauolt indique que la pression partielle de la vapeur exercée par un composant volatil ou un solvant du mélange de gaz, au-dessus de la solution, est lié à la pression de vapeur exercée par le composant ou le solvant volatile pur, et leurs fractions molaires respectives.
Peut vous servir: népelométrieL'équation suivante résume ce qui précède:
PSV = PSVº · xSV
Où pSV C'est la pression partielle du solvant volatil dans le mélange de soude, PSVº la pression du solvant volatile pur et xSV la fraction molaire dans la solution du solvant volatil.
Mélange de solvants volatils
Si vous avez un mélange de deux solvants volatils (A et B) dans la solution, vous pouvez calculer la pression de vapeur qu'ils proviennent de la phase gazeuse, au-dessus de la solution. Ce sera une somme des pressions partielles exercées par les gaz A et B:
PPOUR = XPOUR · PPOURº
PB = XB · PBº
Donc, en ajoutant les pressions de A et B, nous obtenons la pression P totale:
P = xPOUR · PPOURº + xB · PBº
Où p est la pression de vapeur du mélange de soude sur le dessus de la solution, xPOUR et xB les fractions molaires des solvants volatils a et b dans le mélange, et pPOURº et pBº Les pressions de vapeur des solvants volatils purs A et B.
Diminution de la pression dans la phase gazeuse en raison de la présence d'un soluté non volatile
La pression partielle d'un solvant volatil dans la phase gazeuse est donnée par l'expression:
P = PPOURº · xPOUR
En présence d'un soluté B dans la solution, la fraction molaire de B est exprimée comme suit:
XB = 1 -xPOUR
Ensuite, grâce à un traitement mathématique simple, l'expression est atteinte:
Δp = pPOURº · xB (1)
Où Δp est la diminution de la pression partielle du solvant dans la phase gazeuse.
L'expression mathématique (1) indique la diminution de la pression de vapeur d'un solvant en raison de la présence d'un soluté B non volatile. La diminution de la pression de vapeur de solvant a été expliquée en raison de l'emplacement des molécules de soluté B sur la surface de la solution.
Il peut vous servir: groupe carbonyle: caractéristiques, propriétés, nomenclature, réactivitéLa présence de molécules de soluté B produirait une diminution de la concentration de molécules de solvant A à la surface de la solution, limitant son évaporation; Et expliquant ainsi la diminution de la pression de vapeur dans la phase gazeuse.
Exemples
La loi de Raault sert à calculer la pression de vapeur d'une composante volatile d'une solution, comme l'éthanol, le benzène, le toluène, l'éthane, le propane, etc., dans l'espace sur la solution.
Il peut être utilisé pour calculer la pression de vapeur générée dans l'espace sur une solution, en raison du mélange de fluides volatils, de benzène et de toluène, d'éthane et de propane, d'acétone et d'éthanol, etc.
De plus, avec cette loi, vous pouvez déterminer quelle sera la diminution de la pression de vapeur si, par exemple, il dissoudrait le saccharose dans l'eau, étant un soluté non volatile.
Exercices résolus
Exercice 1
Calculez la pression de vapeur d'une solution préparée en dissolvant 60 g de chlorure de sodium (NaCl) dans 400 g d'eau (H2SOIT). Pression de vapeur d'eau (pH2Oº) Un 37 ºC est de 47,1 mmHg. Poids moléculaire h2O = 18 g / mol et poids moléculaire NaCl = 58,5 g / mol.
Nous calculons d'abord les moles d'eau et de chlorure de sodium afin de déterminer leurs fractions molaires:
Moles de h2O = grammes de h2O / PM H2SOIT
= 400 g / (18 g / mol)
= 22,22 moles
Moles de NaCl = G de NaCl / PM NaCl
= 60 g / (58,5 g / mol)
= 1,03 moles
NaCl est un composé électrolytique qui se dissocie en Na+ + CL-. Par conséquent, 1,03 moles de NaCl se dissocient dans 1,03 moles de Na+ et 1,03 moles de Cl-.
Il peut vous servir: réaction de MaillardNous avons l'expression:
PV = XH2O · PH2Oº
Nous n'avons donc pas la fraction molaire de l'eau:
XH2O = Moles de h2O / (moles de h2O + moles de na+ + Moles de Cl-)
= 22,2 moles / 22,22 moles +1,03 moles +1,03 moles
= 0,896
Et nous calculons PV:
PV = 47,1 mmHg · 0.896
PV = 42,20 mmHg
Étant la diminution de la pression de vapeur en raison de la présence de chlorure de sodium:
ΔPV = 47,1 mmHg - 42,20 mmHg
= 4,9 mmHg
Exercice 2
À une température de -100 ºC l'éthane (choisissez3Ch3) et le propane (Cho3Ch2Ch3) Ce sont des liquides. À cette température, la pression de vapeur de l'éthane pur (PEtanoº) est de 394 mmHg, tandis que la pression de vapeur du propane pur (Ppropaneº) est de 22 mmHg. Quelle sera la pression de vapeur sur une solution qui contient des quantités équimolaires des deux composés?
L'approche du problème indique que la solution contient des quantités équimolaires des composés. Cela implique que la fraction molaire du composé et des composés propane est nécessairement égale à 0,5.
Encore une fois, la solution vient par l'expression:
PV = PEtano + Ppropane
Nous calculons les pressions partielles de l'éthane et du propane:
PEtano = PEtanoº · xEtano
= 394 mmHg · 0,5
= 197 mmHg
Ppropane = Ppropaneº · xpropane
= 22 mmHg · 0,5
= 11 mmHg
Et donc nous calculons enfin PV:
PV = PEtano + Ppropane
= 197 mmHg +11 mmHg
= 208 mmHg
Les références
- Whitten, Davis, Peck & Stanley. (2008). Chimie. (8e Ed.). Cengage Learning
- Wikipédia. (2020). La loi de Rault. Récupéré de: dans.Wikipédia.org
- Helmestine, Anne Marie, Ph.D. (11 février 2020). Définition de la loi de Rault en chimie. Récupéré de: Thoughtco.com
- Encyclopædia Britannica. (2020). La loi de Rault. Récupéré de: Britannica.com
- Clark J., Ly i., & Khan s. (18 mai 2020). La loi de Rault. CHIMISTER BOOLISTexts. Récupéré de: Chem.Bibliothèque.org
- « Quantité de moment angulaire, conservation, exemples, exercices
- Concept d'objets opaques, caractéristiques et exemples »

