Structure d'hormones de croissance (somatotropine), fonctions
- 1256
- 169
- Louna Baron
La Somatotropine (STH) U Hormone de croissance (GH) est une protéine relativement petite produite au niveau d'adénohypophyse et impliqué dans les processus de développement, la croissance longitudinale de l'organisme et le contrôle de plusieurs processus métaboliques.
C'est une hormone non glaro. Les hormones glandotropas de l'hypophyse.
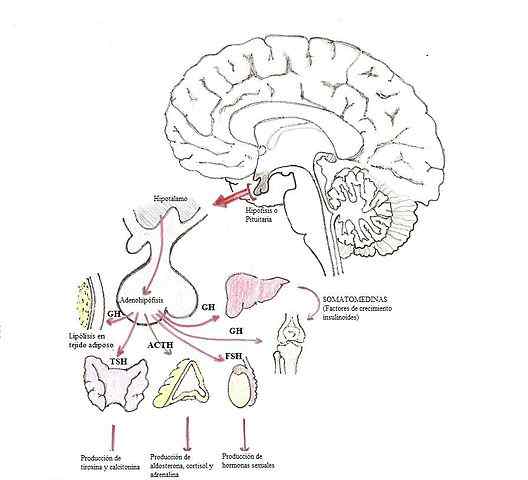
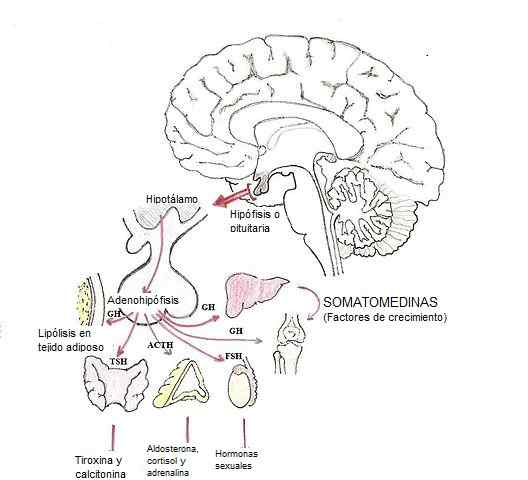 Modification des hormones dans l'hypophyse (Source: Dubaele / Domaine public, via Wikimedia Commons)
Modification des hormones dans l'hypophyse (Source: Dubaele / Domaine public, via Wikimedia Commons) Les hormones des glandotropas sont, par exemple, de l'adrénocortopine (ACTH), des gonadotrophines (FSH et LH) et de l'hormone stimulante thyroïdienne (TSH).
Les hormones non-Glandropas, en revanche, et parmi lesquelles sont incluses par la prolactine et la croissance.
[TOC]
Structure
L'hormone de croissance est une protéine relativement petite qui se produit dans plusieurs isoformes. L'isoforme principale est composée d'environ 191 acides aminés, a un poids moléculaire de 22 kDa et provient d'un peptide précurseur plus long (pré-GH) de 28 kDa, qui est également sécrété mais qui manque de fonctions physiologiques.
Dans sa structure, la somatotropine semble être homologue en prolactine et en somatomamamototropine chorionique (CS), a produit ce dernier dans le placenta. Telle est la similitude, qui est considérée que les trois forment une famille hormonale.
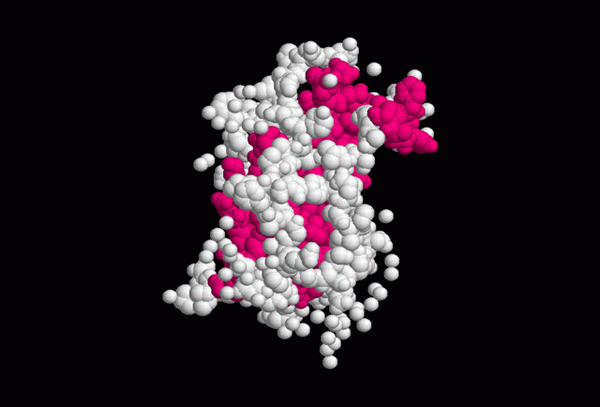 Structure approximative de l'hormone de croissance (Source: роан бекер, via Wikimedia Commons)
Structure approximative de l'hormone de croissance (Source: роан бекер, via Wikimedia Commons) La structure secondaire de la somatotropine montre 4 hélices alpha stabilisées avec deux ponts disulfure, dont la configuration est nécessaire pour l'interaction de l'hormone avec son récepteur.
Un fait par rapport à la structure, et digne d'être mis en évidence, représente le fait que malgré le fait que les hormones de croissance de différentes espèces ont des similitudes remarquables avec l'humain, seuls les seconds et celui des primates, exercent des effets significatifs chez l'homme.
Les fonctions
Les fonctions de somatotropine sont généralement décrites comme celles associées au développement et à la croissance de l'organisme. Également ceux associés au métabolisme, qui comprennent des modifications du métabolisme lipidique et du glucose favorisé par l'hormone.
Les fonctions de croissance, cependant, peuvent également être considérées comme métaboliques, car elles impliquent des fonctions anaboliques associées à la synthèse des protéines, qui n'exclut pas d'autres fonctions sans association directe avec le métabolisme tel que la prolifération cellulaire.
Certaines des fonctions ou actions déployées par la somatotropine sont exercées par cette hormone directement sur ses tissus blancs, mais beaucoup d'entre eux sont exécutés par d'autres substances dont la synthèse et la libération sont stimulées par l'hormone de croissance.
Synthèse IGF
La première ligne d'action de somatotropine est précisément la synthèse de ces substances appelées facteurs de croissance similaires à l'insuline (IGF), dont les types 1 et 2 ont été identifiés. Ils sont désignés comme IGF1 (les plus importants) et IGF2, selon son acronyme en anglais.
Ces facteurs ont été initialement connus et sont toujours désignés, comme des médiateurs de la somatotropine ou des somatomedins C (IGF1) et A (IGF2) ou également comme une activité similaire à l'insuline non suppressionnable (NSILA) (NSILA). Ils sont synthétisés par de nombreux types de cellules, mais se produisent principalement dans le foie.
Les actions du STH et de l'IGF1 sont très diverses. Certains font de l'exercice de chacune de ces substances indépendamment, parfois en conjonction et en synergisme et d'autres fois, ils agissent de manière antagonale.
Peut vous servir: électrophorèse: fondation, technique, à quoi sert, des exemplesInduction de croissance
C'est l'une des actions les plus importantes promues par la somatotropine, mais exécutée en collaboration avec l'IGF1. Bien que les deux induisent la croissance de nombreux tissus corporels, leur effet le plus important est exercé sur la croissance du squelette.
Ce résultat final est produit par plusieurs effets induits par l'hormone et l'IGF1. Ils comprennent l'augmentation du dépôt de protéines par les cellules chondrocytaires et ostéogéniques, le taux de reproduction le plus élevé de ces cellules et la conversion des chondrocytes en cellules ostéogéniques; Tout cela conduit au nouveau dépôt d'os.
Pendant la croissance et le développement de l'organisme, et avant la fermeture des épiphyses osseuses, un nouveau cartilage est déposé dans les épiphyses suivis par sa conversion en un nouvel os, qui allonge la diaphyse et les épiphyses sont séparées.
La consommation progressive de cartilage épiphysaire l'épuise et l'os ne peut continuer de croître. À la fin de l'adolescence, la diaphyse et les épiphyses et la croissance de la longueur des os longs sont ralenties à chaque extrémité et s'arrête enfin.
Un deuxième mécanisme peut expliquer l'augmentation de l'épaisseur osseuse. Les ostéoblastes du périosteium déposent de nouveaux os sur l'ancien, et les ostéoclastes éliminent l'ancien os. Si le taux de dépôt dépasse l'élimination, l'épaisseur augmente.
Comme l'hormone de croissance exerce une stimulation intense sur les ostéoblastes, sous son effet, l'épaisseur des os peut continuer à augmenter, bien que sa longueur ne soit plus modifiée en raison de la fermeture des épiphyses.
Promotion du dépôt de protéines dans les tissus
Cet effet peut être obtenu par différents mécanismes: l'augmentation du transport des acides aminés à travers les membranes cellulaires, l'augmentation de la traduction de l'ARN au niveau des ribosomes, l'augmentation de la transcription de l'ADN en ARN dans le noyau et une réduction des protéines et des acides aminés catabolisme.
Autres actions métaboliques
Dans les tissus gras, l'hormone de croissance favorise la lipolyse et la libération d'acides gras au torrent circulatoire, ce qui augmente sa concentration dans les fluides corporels. En même temps, il favorise dans tous les tissus, la conversion des acides gras dans l'acétyl coenzyme A et son utilisation comme source d'énergie.
La stimulation de l'utilisation des graisses, ainsi que l'accumulation de protéines dues à leur effet anabolique, entraînent une augmentation du tissu maigre.
L'augmentation de la mobilisation des graisses peut être si élevée que le foie produit de grandes quantités d'acide acétoacétique qui conduisent à la cétose et un foie gras peut être généré.
En ce qui concerne le métabolisme des glucides, les effets de la somatotropine comprennent la diminution de la collecte du glucose dans les tissus musculaires et musculaires, une production accrue du foie du glucose et une augmentation de la sécrétion d'insuline.
Tous ces effets sont appelés diabétogènes et la sécrétion d'hormones de croissance élevée peut reproduire des altérations métaboliques qui accompagnent le diabète de type II de type II dépendant du non-insuline.
Autres fonctions
Les actions anaboliques et mitogènes de la GH et de l'IGF1 se manifestent également dans la croissance et la fonction du cœur, du foie, de la rate, de la thyroïde, du thymus et de la langue. L'hormone peut contribuer à l'épaississement de la peau, à la stimulation des glandes transpiratrices et à la croissance des cheveux.
Dans les reins, le taux de filtration glomérulaire et la synthèse du calcitriol augmentent, ce qui favorise non seulement la croissance, mais aussi la minéralisation osseuse. Il favorise également l'érythropoïèse et la synthèse du fibrinogène et la réponse immunitaire par la stimulation des lymphocytes T et des macrophages.
Peut vous servir: tissu épithélial: caractéristiques, description, fonctions, typesRécepteurs pour la somatotropine
Les actions de la somatotropine, y compris la promotion de la synthèse de facteurs de croissance similaires à l'insuline, sont médiées par leur union avec des récepteurs spécifiques exprimés dans les membranes des cellules blanches.
Il existe deux formes de ces récepteurs, dont le second est une variante courte (tronquée) du premier; Forme tronquée qui inhibe la fonction du récepteur long, et que si elle était surexprimée, elle produirait une insensibilité aux tissus à l'hormone.
Le récepteur long est composé de 638 acides aminés et possède un domaine extracellulaire de 250, un domaine alpha transmembraal d'environ 38 et un domaine intracellulaire de 350 acides aminés. Chaque molécule de somatotropine finit par rejoindre deux molécules de récepteur et produire ce qu'on appelle la dimérisation du récepteur.
Cette dimérisation active une protéine JAK2 kinase située sur les extrémités intracellulaires de chaque monomère du récepteur et ces kinases actifs phosphorylent d'autres substrats tels que la STAT5 et le récepteur de la somatotropine lui-même.
Les molécules phosphorylées STAT5 souffrent également d'une dimérisation qui les rend très précises des régulateurs de l'expression des gènes et de la synthèse des protéines.
Production
La somatotropine est synthétisée au niveau des cellules de somatotropas d'adénohypophyse. Ces cellules sont teintes intensément avec des substances acides afin qu'elles soient également appelées acidophiles. Ils sont ensemble le groupe cellulaire le plus abondant de la glande car ils représentent 50% du total de 5 types différents.
Il existe un complexe génétique de 5 gènes dans le bras long du chromosome 17 humain qui code pour les différentes isoformes de l'hormone de croissance et la somatomamototropine chorionique humaine (HCS).
L'un d'eux est le HGH-N normal, qui code la forme la plus abondante d'hormone de croissance humaine qui est la susmention de 22 kDa et représente 75% de l'hormone totale de croissance circulante.
Son ARN messager est soumis à "Couper et épisser" pour produire une forme plus petite d'hormone, de 20 kDa, qui manque de déchets d'acides aminés de 32 à 46 et représente 10%.
Un deuxième gène (HGH-V) est exprimé principalement dans le placenta et code une forme variante de HGH dont seules des quantités significatives apparaissent dans la circulation pendant la grossesse. Les 3 autres gènes codent les isoformes de la somatomamototropine humaine.
Libérer
La synthèse et la sécrétion ou la libération d'hormone de croissance sont régulées par des facteurs stimulants et inhibiteurs de ces fonctions.
Influences stimulantes
Parmi les principales influences humoristiques, la synthèse stimulante et la sécrétion de somatotrophine figurent les peptides de Ghrh (hormones de libération d'hormone de croissance) et la ghréline.
L'hormone libératrice de l'hormone de croissance (GHRH) est un peptide hypothalamique qui existe respectivement dans deux variantes de 40 et 44 acides aminés. Il conduit dans des cellules de somatotropas à la synthèse de l'AMPC et à l'activation du facteur de transcription Pit1 spécifique pour l'hormone de croissance.
La ghréline est une hormone endogène de la croissance de l'hormone de croissance. C'est un peptide d'environ 28 acides aminés synthétisés au niveau de l'hypothalamus et de l'estomac. Il agit synergique avec la GHRH dont la libération favorise, tout en inhibant la somatostatine. Agit à travers des récepteurs qui activent la phospholipase C.
Certains paramètres métaboliques tels que l'hypoglycémie, les faibles niveaux d'acides gras libres dans le sang et les concentrations élevées d'acides aminés sont des stimuli importants pour la sécrétion d'hormones de croissance.
Peut vous servir: les 12 étapes du développement humain et ses caractéristiquesD'autres facteurs stimulants qui comptent sont le stress aigu, la surcharge corporelle, la douleur, les stéroïdes sexuels (puberté), la dopamine, la stimulation des récepteurs α2, l'acétylcholine, la galanine, la sérotonine et la β-endorphine.
Influences inhibiteurs
Parmi ceux-ci figurent la somatostatine ou l'inhibiteur hormonal de la libération d'hormones de croissance (GHRIH) et la rétroaction négative.
La somatostatine est un peptide hypothalamique de 14 acides aminés qui inhibe la sécrétion, mais pas la synthèse, de l'hormone de croissance. Une longue variante, 28 acides aminés, est synthétisée dans le tractus gastro-intestinal. Les deux variantes se lient au même récepteur et inhibent la synthèse cyclique de l'ampli.
Quant à la rétroaction négative, la GH libérée, grâce à une action auto-sociale, inhibe sa propre libération. L'IGF1 inhibe l'hypothalamus à l'hormone de croissance de l'hormone de croissance et stimule la somatostatine, tout en inhibe la synthèse de GH dans l'hypophyse.
Certains paramètres métaboliques tels que l'hyperglycémie, les taux plasmatiques élevés d'acides gras libres et les faibles niveaux d'acides aminés sont des inhibiteurs de sécrétion de somatotropine.
Les inhibiteurs sont également un stress chronique, un stress chronique, une adiposité, une progestérone, des hormones thyroïdiennes, des déficits ou des excès de cortisol et une stimulation des récepteurs adrénergiques β2 β2.
Dose
L'utilisation thérapeutique de l'hormone de croissance biosynthétisée est indiquée pour le traitement des souffrances dans lesquelles une carence en sécrétion a été révélée, dans le nanisme pituitaire et chez les enfants de taille faible par le syndrome de Turner.
L'administration est faite sous la forme d'une solution injectable reconstruite à partir d'une route qui contient un lyophilisé avec 40 U.Toi. de l'hormone biosynthétique, et à laquelle les 2 ml de compagnons de solution de chlorure de sodium à 0,9% sont ajoutés.
Dans une carence en hormones de croissance chez les enfants, il est recommandé entre 0,07 et 0,1 U.Toi./ kg de poids corporel par jour. Dans le syndrome de Turner 0,14 U.Toi./ kg de poids corporel par jour. Pour une carence en hormones de croissance chez les adultes: 0,018 à 0,036 u.Toi./ kg de poids corporel par jour.
Effets
L'administration thérapeutique de l'hormone de croissance peut être accompagnée de certains effets collatéraux défavorables tels que l'hypersensibilité manifeste à travers l'urticaire généralisé, l'hypoglycémie à jeun, l'inflammation au site d'injection et les maux de tête passager.
Le développement d'une certaine hypertension intracrânienne bénigne a été décrit, plus fréquent chez les enfants et moins chez les adultes.
En ce qui concerne le métabolisme des glucides, le développement du diabète sucré a été signalé chez les patients qui ont reçu un traitement avec l'hormone de croissance.
En ce qui concerne le système musculaire squelettique, il existe des preuves de myosite inflammatoire avec la myalgie et la faiblesse musculaire, produites non pas par l'hormone, mais peut-être par le métacresol utilisé comme conservateur dans la formule.
Des cas de gynécomastie, d'anémie et de pancréatite aiguë ont été signalés.
Les références
- Ganong WF: L'hypophyse, 25e Ed. New York, McGraw-Hill Education, 2016.
- Guyton AC, Hall JE: Hormones hypophysaires et leur contrôle par l'hypothalamus, dans Manuel de physiologie médicale, 13e éd, AC Guyton, JE Hall (éd.). Philadelphie, Elsevier Inc., 2016.
- Lang F, Verrey F: Hormone, dans Physiologie des Menschen Pathophysiologie, 31 ed, RF Schmidt et al (eds). Heidelberg, Springer Medizin Verlag, 2010
- Voigt K: Système Endokrines, dans Physiologie, 6e éd; R Klinke et al (eds). Stuttgart, Georg Thieme Verlag, 2010.
- Widmaier EP, Raph H et Strang KT: Le système endocrinien. L'Hypothalamus et la glande hypophysaire, dans la physiologie humaine de Vander: les mécanismes de la fonction corporelle, 13e éd; EP Windmaier et al (eds). New York, McGraw-Hill, 2014.
- « Concept d'allitération, caractéristiques et exemples
- Caractéristiques de communication de groupe, éléments, exemples »

