Caractéristiques de l'histidine, structure, fonctions, nourriture
- 2052
- 246
- Jade Duval
La Histidine (His, h) C'est un acide aminé qui est utilisé pour la synthèse des protéines. Il s'agit d'une molécule hydrophile, il est donc généralement orienté vers l'extérieur des structures protéiques lorsqu'elles sont dans un milieu liquide.
Il est considéré comme un acide aminé essentiel pour les enfants en croissance car ils ne le produisent pas. Chez l'adulte, il y a une petite production d'histidine, mais elle est insuffisante pour fournir les besoins quotidiens, il est donc considéré comme un acide aminé semi-essentiel.
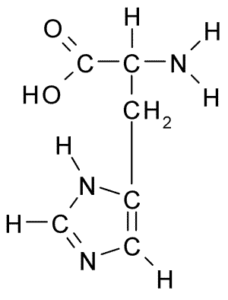 Structure chimique de l'acide aminé histidine (Source: Borb, via Wikimedia Commons)
Structure chimique de l'acide aminé histidine (Source: Borb, via Wikimedia Commons) Para los animales y el hombre, la histidina es un aminoácido esencial o al menos semi esencial, sin embargo, las plantas, los hongos y los microorganismos producen eficientemente la histidina que necesitan y son parte de las fuentes dietéticas de histidina, además de las proteínas les animaux.
L'histidine remplit des fonctions physiologiques très importantes dans l'être humain telles que: celles de faire partie des centres actifs de nombreuses enzymes, de participation à la croissance, du système immunitaire et de la formation de la myéline dans les fibres nerveuses, entre autres.
La biosynthèse de l'histidine est un processus complexe qui se déroule principalement dans le foie et nécessite 9 à 11 étapes enzymatiques. Sa dégradation se produit dans le foie et la peau et passe par la formation de glutamate, puis suivant différents chemins.
De nombreux aliments sont riches en histidine, comme les protéines animales telles que la viande et les produits laitiers, ainsi que les protéines végétales. Ceux-ci fournissent une grande partie des exigences quotidiennes d'histidine dont notre corps a besoin pour fonctionner correctement.
Le déficit ou l'excès d'histidine causé par des problèmes hérités métaboliques ou de transport, ou une insuffisance alimentaire dans l'apport, sont liés à certains problèmes importants qui affectent la santé chez les enfants et les adultes. La consommation suffisante d'histidine vous permet de maintenir une vie saine et saine dans la plupart des cas.
[TOC]
Caractéristiques
Une caractéristique de mise en évidence de l'histidine est qu'elle peut être convertie en histamine, une substance qui participe activement à de nombreuses réactions allergiques et inflammatoires.
Dans les poissons exposés à l'environnement sans réfrigération suffisante, les bactéries peuvent convertir l'histidine en histamine et c'est pourquoi, lorsqu'elles sont ingérées, elles provoquent une intoxication alimentaire.
Une autre caractéristique de cet acide aminé est qu'il est l'un des rares, parmi les 22 existants, qui dans la gamme de pH physiologique (environ 7.4) Il est ionisé et, par conséquent, peut participer activement au site catalytique de nombreuses enzymes.
Dans la molécule d'hémoglobine, l'histidine proximale est l'un des ligands du groupe Hemo. En d'autres termes, cet acide aminé participe à la fonction de transport d'oxygène de l'hémoglobine et est indispensable pour la synthèse de cette protéine, ainsi que pour la myoglobine, qui est également connue sous le nom de «l'hémoglobine musculaire».
Structure
L'histidine est un acide aminé Hydrophile polaire basique, Classé dans des acides aminés essentiels, car il ne peut pas être synthétisé par les animaux. Cependant, et comme mentionné précédemment, il est synthétisé par les bactéries, les champignons et les plantes.
Chez les enfants en croissance, l'histidine est absolument nécessaire; L'adulte peut le synthétiser, mais il n'est pas clair si cela couvre les besoins quotidiens de l'histidine, il doit donc être ingéré avec le régime.
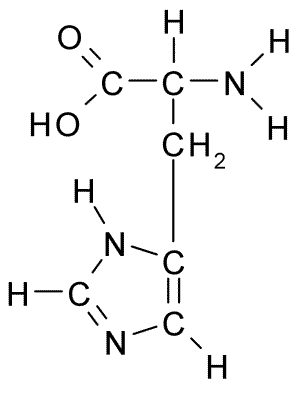
Comme tous les acides aminés, l'histidine a un carbone α auquel un groupe amino, un groupe carboxyle, un atome d'hydrogène et une chaîne latérale sont joints.
Peut vous servir: coxiella burnetiiLa chaîne latérale de cet acide aminé est formée par un cycle d'imidazole qui, au pH physiologique, les protons et acquiert une charge positive et est appelé "Imidazolio " abrégé comme IMH+.
Avec la lysine et l'arginine, l'histidine forme le groupe d'acides aminés de base. Des trois, l'histidine est la moins basique et son anneau imididoólica peut être non protégé à un pH près de 6.
Étant donné que le pH physiologique histidine peut échanger des protons, cela participe généralement à une catalyse enzymatique qui implique le transfert de protons. De plus, comme il s'agit d'un acide aminé polaire, il se trouve généralement sur la surface externe des protéines, où elle peut hydrater dans un milieu aqueux.
Les fonctions
Dans le cadre du site enzymatique actif
L'histidine est nécessaire pour la synthèse de nombreuses protéines, en particulier les enzymes dont les centres actifs ont cet acide aminé. Il fait partie du centre actif des aldlasases de mammifères, où il fonctionne comme donneur de protons.
Il est situé dans le centre actif de la carboxipeptidase A, une enzyme pancréatique qui a un site actif formé par Zn et Histidine. Dans l'enzyme glycolithique mutasa phosphoglycérate, il y a deux déchets d'histidine dans son centre actif qui agissent comme des accepteurs ou des donneurs de groupes phosphoryle.
Il se trouve également dans le site actif des enzymes telles que la glycéraldéhyde 3-phosphate déshydrogénase, la lactate déshydrogénase, la papaïne, la chimotripsine, le RNASA A et l'ammoniac liasa histidine (histidase). De plus, c'est un inhibiteur de l'enzyme glutamine synthétase.
Autres fonctions
Cet acide aminé est d'une grande importance pour l'organisme, car son décarnar histidine décarboxylase.
L'histidine est produite par les neurones du système nerveux central avec des fonctions neuromodulatrices.
Il est nécessaire pour la formation de gousses de myéline de fibres nerveuses, donc elle rencontre un rôle important dans la transmission des impulsions électriques.
Avec l'hormone de croissance et d'autres acides aminés, l'histidine contribue aux mécanismes de réparation des tissus, principalement dans le système cardiovasculaire.
Certaines fonctions supplémentaires incluent:
- Contribue à la détoxification de certains métaux lourds car il agit comme le chélation.
- Protège contre les dommages causés par le rayonnement.
- Participer à la formation de globules rouges et blancs.
- Il est nécessaire pour la formation d'hémoglobine.
- Il aide à lutter contre certains effets négatifs de la polyarthrite rhumatoïde tels que l'inflammation et le manque de mobilité.
- C'est un acide aminé important pour la régénération capillaire, la croissance et la fonction sexuelle.
Carnosine, ansérine et homocosine, sont des diphéptides formés à partir de l'histidine. Les deux premiers se trouvent dans les muscles et ont des fonctions importantes telles que les tamponners et en tant qu'activateurs de la myosine atasa.
L'homocosine est produite dans le cerveau en quantité 100 fois plus élevée que le muscle squelettique charnu.
Biosynthèse
L'histidine obtient son squelette gazéifié du ribose à 5 phosphate. Dans les bactéries ET. Coli, Cet acide aminé se produit à partir dudit composé au moyen de 11 étapes enzymatiques:
- La première étape de la synthèse consiste en le transfert d'un phosphorribosyl de l'ATP au carbone 1 du ribose 5-phosphate, générant du 5-phosphorribosyl-1-pyrophosphate (PRPP) (PRPP). L'enzyme phosphorribosyl-pyrophosphate synthétase (PRPP synthétase) catalyse cette réaction.
- Ensuite, le transfert du groupe de pyrophosphate de carbone 1 au N-1 de l'ATP se produit, et le N1- se produit (5'-phosphorribosyl) -ATP. L'enzyme qui catalyse cette réaction est la phosphoruseltransférase ATP.
- Par l'action de la phosphorribosyl-top-pyrophosphate hydroxylase, la liaison α, β-pyophosphate de l'ATP est hydroxilase et la N1- est formée (5'-phosphorribosyl) -AMP.
- L'enzyme hydroxylase phosphorribosyl-MAP ouvre le cycle purine entre le N-1 et le C-6 et le ribonucléotide est formé N1- (5'-phosphorribosil formimino) -5-amininimidazole-4-carboxamide-1-lribonucléotide.
- Ensuite, l'anneau Ribofuranosa qui provient du PRPP est ouvert et est isomérisé à un ketosa, formant le N1- (5'-phosphorribosyl formimine) -5-amininimidazole-4-carboxamide-1-lribonucléotide par un effet d'une enzyme isomérase.
- L'enzyme aminotransférase transfère le groupe au milieu de la glutamine, qui devient glutamate, et rompt la liaison formimine, il est donc libéré du 5-aminoimimidazole-carboxamide-1-lribonucléotide et le phosphate d'imidazole-glycérol est généré.
- Une molécule d'eau du phosphate d'imidazole-glycérol est éliminée au moyen de l'imidazole-glycérol phosphate déshydratase et forme l'imidazole-acétol phosphate.
- Le phosphate d'imidazole-acétol est transféré un groupe amino par le phosphate de l'histidinol transaminase et le phosphate histidinol est formé.
- Le groupe d'ester phosphorique de phosphate d'histidinol pour former l'histidinol est hydrolysé. Histidinol phosphate fospatase catalyse cette réaction.
- Plus tard, l'histidinol est oxydé par l'histidinol déshydrogénase et est histidinal.
- La même histidinol déshydrogénase oxyde à l'histidinal et la rend histidine.
La première enzyme de la voie biosynthétique d'histidine est inhibée par le produit de la route, c'est-à-dire que l'histidine participe à l'inhibition allestrique de l'ATP phosphorribosyltransférase, qui représente le principal mécanisme de régulation de l'itinéraire.
Dégradation
L'histidine, la proline, le glutamate, l'arginine et la glutamine sont des acides aminés qui finissent par former α-zotogluer. Quatre d'entre eux deviennent d'abord le glutamate, qui en raison de la transamination donne lieu à l'α-cétoglutorat.
L'histidine, par l'histidinase, perd le groupe α-amino pour devenir urocanato. Ensuite, l'urocanase hydrate les positions 1 et 4 de l'urocanato, formant le 4-midazolone-5-propionate. Par la suite, le groupe imino du 4-midazolone-5-propionato se produit, formant le N-Formiminoglutamato.
La dernière réaction implique le transfert du formyle du N-Formiminoglutamate en tétrahydropholate, qui fonctionne avec le transfert forminéte du glutamate enzymatique. Les produits finaux de cette réaction sont le glutamate et le tétrahydropholate N5-Formimino.
Α-cétoglutarate est formé par transamination du glutamate. Α-cétoglutarate est un intermédiaire du cycle de Krebs et peut également entrer dans la route gluconéogène pour la formation du glucose.
Le groupe Amino Glutamato entre dans le cycle de production de l'urée pour être éliminé par l'urine. Toutes ces réactions se produisent dans le foie et une partie d'entre elles sur la peau.
Aliments riches en histidine
Les besoins quotidiens de l'histidine sont d'environ 10 à 11 mg par kg de poids corporel, par jour. Chez les enfants en croissance, l'histidine est un acide aminé essentiel qui doit être fourni avec le régime.
Chez d'autres animaux, l'histidine est également un acide aminé essentiel et ceux qui sont élevés dans les écuries devraient recevoir l'histidine pour maintenir leurs niveaux d'hémoglobine normaux.
Parmi les aliments riches en histidine figurent:
- Bœuf, agneau, porc, poulet et dinde. Il se trouve également dans les poissons comme le thon (même en conserve), le saumon, la truite, le pargo et la lubina, ainsi que dans certains fruits de mer.
Peut vous servir: Huile Culture: à quoi sert, Foundation, Procédure, Résultats- Le lait et ses dérivés, en particulier dans les fromages mûrs tels que le parmesan, le gruyère, le fromage suisse, le Gouda, entre autres. Chez les indigènes, dans le sérum, dans le yaourt et dans la crème sure.
- Soja et noix comme les noix et les graines. Dans le tournesol, la citrouille, la pastèque, le sésame, les amandes, la pistache, le beurre d'arachide et le chia.
- Œufs et haricots ou haricots blancs.
- Des grains entiers tels que le quinoa, le blé, le riz intégral, etc.
Avantages de votre apport
Il existe un certain nombre de conditions pathologiques dans lesquelles l'histidine peut être utile comme adjuvant pour le traitement.
Parmi ces pathologies, nous pouvons nommer la polyarthrite rhumatoïde, l'hypertension artérielle (depuis qu'un effet hypotensif de l'histidine a été décrit), dans les infections, la frise et le sexe et l'audition, les ulcères et les anémies.
Dans la peau, la dégradation de l'histidine consommée produit de l'acide uroanique, qui est capable de protéger la peau car elle absorbe les rayons ultraviolets.
La consommation excessive par des individus en bonne santé ne produit pas de modifications majeures, car elle est rapidement dégradée. Cependant, l'utilisation de compléments alimentaires histidine chez les patients présentant des problèmes de foie et / ou rénaux graves doit être restreint.
Troubles de la carence
Le déficit d'histidine est lié à des altérations de la réponse immunitaire due.
Des problèmes osseux, la surdité et les anémies associées au déficit d'histidine ont également été signalées.
La maladie de Hartnup est une condition héréditaire qui affecte le transport de l'histidine et du tryptophane à travers la muqueuse de l'intestin mince et des reins, ce qui provoque un déficit des deux acides aminés.
Les manifestations cliniques les plus pertinentes sont l'apparition de lésions schegous et rouges dans la peau après l'exposition au soleil, divers degrés d'altération des mouvements et certains symptômes de maladies psychiatriques.
L'histidémie est une maladie récessive autosomique caractérisée par le déficit de l'enzyme histidase, ce qui provoque une augmentation des concentrations d'histidine dans le sang et l'urine.
En conséquence, ces patients ne peuvent pas dégrader l'histidine en acide urocale dans le foie et la peau. Cette maladie s'accompagne d'un retard mental modéré, de défauts de la parole et de la mémoire auditive sans surdité.
La restriction de l'apport en histidine en tant que traitement n'a pas été efficace pour générer une amélioration clinique et entraîne le risque de générer des troubles de croissance chez les enfants touchés par cette maladie.
Les références
- Mathews, C., Van Holde, K., & Ahern, k. (2000). Biochimie (3e érigé.). San Francisco, Californie: Pearson.
- Murray, R., Bender, D., Botham, K., Kennelly, P., Rodwell, V., & Weil, P. (2009). Biochimie illustrée de Harper (28e Ed.). McGraw-Hill Medical.
- Nelson, D. L., & Cox, M. M. (2009). Principes de lehninger de la biochimie. Éditions Omega (5e Ed.). est ce que je.org
- Perecarz, P., Farri, L., & Papageorgiou, un. (1983). Les effets du lait maternel et des formules de faible protéines sur les taux de décalage total des protéines du corps et l'excrétion urinaire de la 3-méthylhistidine des nourrissons prématurés. Sciences cliniques, 64, 611-616.
- Chanson, B. C., Joo, n., Aldini, G., & Yeum, k. (2014). Fonction biologique des dipeptides d'histidine et du syndrome métabolique. Recherche et pratique en nutrition, 8(1), 3-10.
- « Propriétés d'oxygène, structure, risques, utilisations
- Historique des systèmes experts, caractéristiques, avantages, inconvénients »

