Structure des hydrocarbures cycliques, propriétés, exemples
- 3039
- 335
- Raphaël Meyer
Les hydrocarbures cycliques Ce sont des composés organiques constitués d'atomes de carbone et d'hydrogène qui sont liés pour provoquer des anneaux ou des structures cycliques. Il existe principalement trois types: alicle, aromatique et polycyclique.
Ces types d'hydrocarbures peuvent alors être composés des versions fermées d'alcanes, d'alcènes et d'alcynes; ont des anneaux avec des systèmes aromatiques, comme le benzène et ses dérivés; ou présenter des structures complexes et fascinantes. De tous, les alicycliques sont les plus simples et sont généralement représentés en utilisant des polygones.
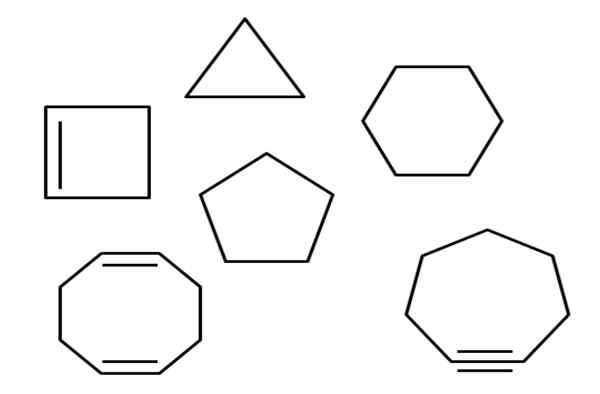
 Hydrocarbures alicycliques. Source: Gabriel Bolívar.
Hydrocarbures alicycliques. Source: Gabriel Bolívar. Ci-dessus, par exemple, il existe plusieurs hydrocarbures allicycliques. Ils semblent de simples polygones: un carré, un triangle, un pentagone, un hexagone, etc. Si l'un de ses liens C-C pouvait être coupé avec des ciseaux, le résultat serait un alcane, un alcène (s'il a des liens doubles) ou Alquino (si vous avez des liens triples).
Ses propriétés ne diffèrent pas trop des hydrocarbures à chaîne ouverte à partir desquels ils procèdent; Bien que, chimiquement, plus, plus ils seront stables, et son interaction avec un milieu moléculaire devient la plus prononcée (pour sa plus grande zone de contact).
[TOC]
Structure
En allant directement à la question qui concerne leurs structures, il convient de préciser que ceux-ci ne sont pas plats, même si dans leur représentation des polygones, ils semblent. La seule exception à cette affirmation se trouve dans le cyclopropane.
Il est également nécessaire de clarifier que les termes «cycles» et «anneaux» sont souvent interchangeables; Un anneau n'a pas à circuler et peut donc acquérir des géométries sans fin tant qu'elle est une structure fermée. On dit ensuite que le cyclopropane a un cycle anneau ou triangulaire.
Tous les carbones ont des hybridations SP3, Leurs géométries sont donc des tétraédrales et leurs liens doivent être idéalement séparés par un angle de 109,5 °; Cependant, cela n'est pas possible pour les structures aussi fermées que celles du cyclobutane (carré) ou du cyclopentano (pentagone).
Il peut vous servir: benzimidazole (C7H6N2): histoire, structure, avantages, inconvénientsIl est alors question d'une tension qui déstabilise la molécule et est déterminée expérimentalement par la mesure des chaleurs de combustion moyennes de chaque groupe2.
Conformations
Et que se passe-t-il lorsqu'il y a des liens doubles ou triples? La tension augmente, car là où il y en a une, la structure sera obligée de "rétrécir" et de rester à plat; qui, consécutivement, forcerait une conformation au-dessus des autres, éclipsant probablement les atomes d'hydrogène voisins.
 Conformères pour le cyclohexane. Source: Sponk [domaine public]
Conformères pour le cyclohexane. Source: Sponk [domaine public] Dans l'image supérieure, deux confesseurs pour le cyclohexan tentent d'expliquer ce qui précède. Les atomes qui sont dans les positions pour soit et Ils seraient axiaux ou équatoriaux, respectivement. Notez qu'au lieu d'un hexagone plat, vous avez une chaise (à gauche) et un bateau (à droite).
Ces structures sont dynamiques et établissent un équilibre entre elles. Si les atomes pour Ils sont très volumineux, l'anneau "s'adaptera" à les positionner dans des positions équatoriales; Puisqu'il y est orienté vers les côtés de l'anneau (qui renforcerait ou nuirait aux interactions intermoléculaires).
Si nous observons chaque carbone séparément, on verra que ce sont des tétraédiques. Ce ne serait pas le cas s'il y avait une double liaison: ses hybridations SP2 Ils forceraient la structure à s'aplatir; et avoir un triple lien, pour aligner. La structure plate du benzène est la représentation maximale de ce.
Propriétés
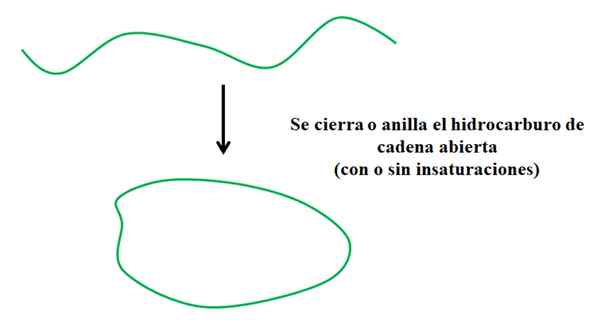 Processus simplifié dans lequel se forme un hydrocarbure cyclique. Source: Gabriel Bolívar.
Processus simplifié dans lequel se forme un hydrocarbure cyclique. Source: Gabriel Bolívar. Supposons que vous ayez un hydrocarbure à chaîne ouverte (avec ou sans insaturation ou ramifications). Si nous pouvions rejoindre leurs extrémités, un anneau ou un cycle serait créé (comme dans l'image supérieure).
D'après l'optique de la synthèse organique, cela ne se produit plus; Il doit y avoir de bons groupes sortants liés aux extrémités de la chaîne, qui en partant, favorisez que la chaîne se ferme (si la solution est très diluée).
Peut vous servir: heptano (C7H16): structure, propriétés et utilisationsDans cet esprit, on peut voir que l'hydrocarbure des traits verts ne souffre qu'une transformation par rapport à sa structure; Sans la rupture ou l'ajout de nouveaux liens avec d'autres atomes. Cela signifie que chimiquement, il continue d'être le même avant et après la fermeture ou la sonnerie.
Par conséquent, les propriétés chimiques ou physiques de ces hydrocarbures allicyle ne diffèrent pas trop de ceux de leurs homologues de chaîne ouverte. Les deux sont des réactifs à la même espèce (pour dire, les halogènes sous la lumière utraviolet) et peuvent subir de fortes oxydations ou une combustion en libérant.
Forces intermoléculaires
Il y a un fait indéniable: l'anneau a une plus grande zone de contact que la chaîne ouverte, et donc ses interactions intermoléculaires sont plus fortes.
Le résultat est que ses points d'ébullition et de fusion ont tendance à être plus importants, tout comme leurs densités. Beaucoup de différences peuvent être remarquées dans leurs taux de réfraction ou leurs pressions de vapeur.
Nomenclature
Revenant à l'exemple de l'hydrocarbure Green Strod, sa nomenclature reste inchangée une fois qu'il a fermé sur lui-même (en tant que serpent qui mord sa propre queue). Par conséquent, les règles de nomenclature restent les mêmes; À moins que les hydrocarbures polycycliques ou aromatiques ne soient abordés.
Trois composés sont présentés ci-dessous, qui recevront leurs noms appropriés:
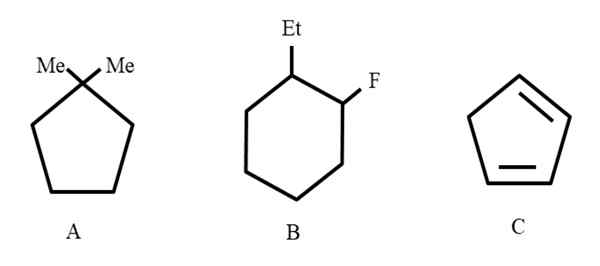 Trois exemples d'hydrocarbures cycliques pour attribuer leurs nomenclations. Source: Gabriel Bolívar.
Trois exemples d'hydrocarbures cycliques pour attribuer leurs nomenclations. Source: Gabriel Bolívar. Pour commencer, lorsqu'ils sont des structures fermées, le cycle du préfixe est utilisé pour y faire référence (ici, l'anneau de mots est relégué).
De gauche à droite, nous avons: un cyclopentano, un cyclohexan et un autre cyclopentano. Les carbones sont répertoriés de telle manière que les nombres mineurs sont affectés aux remplacements, et ils sont également mentionnés dans l'ordre alphabétique.
Peut vous servir: Renio: découverte, propriétés, structure, utilisationsAinsi, il devient: 1,1-diméthylcyclopentano. En B, il commence par mentionner le substituant éthylique avant le fluor, donc son nom est: 1-éthyl-2-fluorciclohexano. Et puis pour C, les doubles liaisons sont prises en tant que substituants, le nombre de carbones qui le forment doivent être indiqués: 1,3-cyclopentadiieno.
Exemples
Tout au long de l'article, il a été mentionné de plusieurs hydrocarbures cycliques. Dans la première image, ils peuvent être trouvés: cycloopropan, cyclobutane, cyclopentano, cyclohexan, cycloheptane et cyclooctane.
À partir d'eux, un large éventail de dérivés peut être obtenu, et il suffit de placer des liaisons doubles ou triples pour avoir des cycloalques ou des cycloalquins, respectivement. Et en ce qui concerne les hydrocarbures aromatiques, il suffit de garder à l'esprit l'anneau de benzène et de le remplacer ou de le reproduire en deux dimensions.
Cependant, les plus extraordinaires (et problématiques lors de la compréhension de leur nomenclature) sont les hydrocarbures polycycliques; c'est-à-dire qu'il ne suffit pas avec des polygones simples pour les représenter de manière simple. Trois d'entre eux méritent d'être mentionnés: Cuban, Basket et Pagodano (Images inférieures).
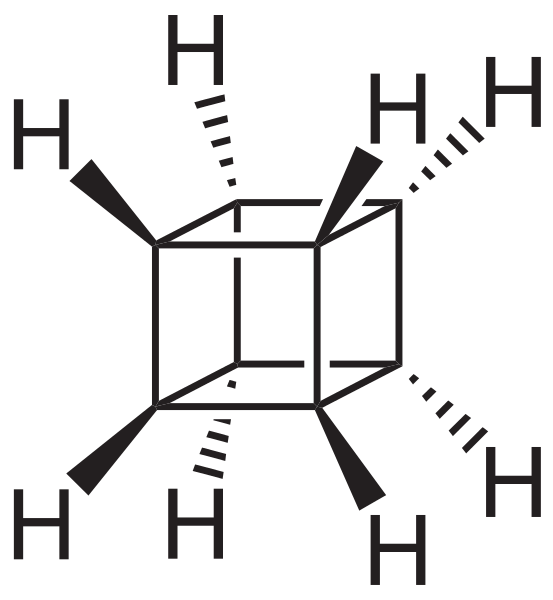 Squelette cubain. Source: Neurotoger [domaine public].
Squelette cubain. Source: Neurotoger [domaine public].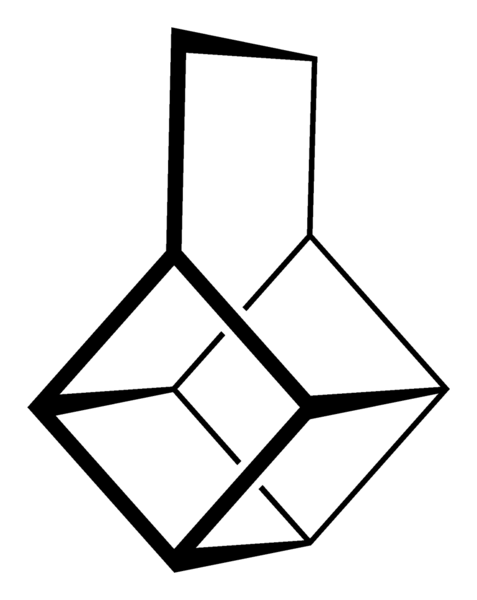 Squelette de canastano. Source: Benjah-Bmm27 [domaine public].
Squelette de canastano. Source: Benjah-Bmm27 [domaine public]. Squelette de pagode. Source: Puppy8800 [domaine public]
Squelette de pagode. Source: Puppy8800 [domaine public]
Chacun d'eux a sa méthodologie de synthèse complexe, son histoire, son art et une fascination latente pour les possibilités structurelles infinies auxquelles les hydrocarbures simples peuvent atteindre.
Les références
- Morrison, R. T. Et Boyd, R, n. (1987). Chimie organique. 5e édition. Éditorial Addison-Wesley Inter-American.
- Carey F. (2008). Chimie organique. (Sixième édition). Mc Graw Hill.
- Graham Salomons t.W., Craig B. Fryhle. (2011). Chimie organique. Amines. (10e édition.). Wiley Plus.
- Reid Danielle. (2019). Hydrocarbures cycliques: définition et exemple. Étude. Récupéré de: étudier.com
- Fondation CK-12. (5 juin 2019). Hydrocarbures cycliques. CHIMISTER BOOLISTexts. Récupéré de: Chem.Bibliothèque.org
- Wikipédia. (2019). Composé cyclique. Récupéré de: dans.Wikipédia.org
- Cowboy de Miguel. (2019). Hydrocarbures cycliques. Récupéré de: décias.filet
- « Mécanismes de corrosion galvanique, exemples, protection
- Histoire, caractéristiques et importance des totipotentialités »

