Hydrolyse ce qui consiste et des exemples de réactions
- 4560
- 10
- Noa Da silva
La hydrolyse C'est une réaction chimique qui peut se produire à la fois dans les molécules ou les ions inorganiques et organiques, et qui implique la participation de l'eau pour la rupture de ses liaisons. Son nom provient du grec, de «l'hydro» de l'eau et de la «lyse» de rupture.
La molécule d'eau, h2Ou, il établit un équilibre avec les ions des sels acides et des bases faibles, apparaissant pour la première fois ce concept en études générales de la chimie et de la chimie analytique. C'est donc l'une des réactions chimiques les plus simples.
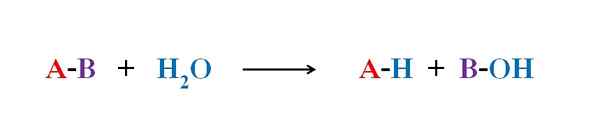 Équation générale pour une réaction d'hydrolyse. Source: Gabriel Bolívar.
Équation générale pour une réaction d'hydrolyse. Source: Gabriel Bolívar. Dans plusieurs exemples d'hydrolyse, l'eau seule est incapable de rompre une certaine liaison covalente. Lorsque cela se produit, le processus accélère ou catalyse par acidification ou alcalisation du milieu; c'est-à-dire en présence d'ions H3SOIT+ ou oh-, respectivement. Il existe également des enzymes qui catalysent l'hydrolyse.
L'hydrolyse occupe une place spéciale en termes de biomolécules, car les liens qui maintiennent leurs monomères ensemble sont sensibles à l'hydrolyzar dans certaines conditions. Par exemple, les sucres sont hydrolysés pour décomposer les polysaccharides dans leurs monosaccharides constitutifs grâce à l'action des enzymes de la glucosidase.
[TOC]
Qu'est-ce que l'hydrolyse?
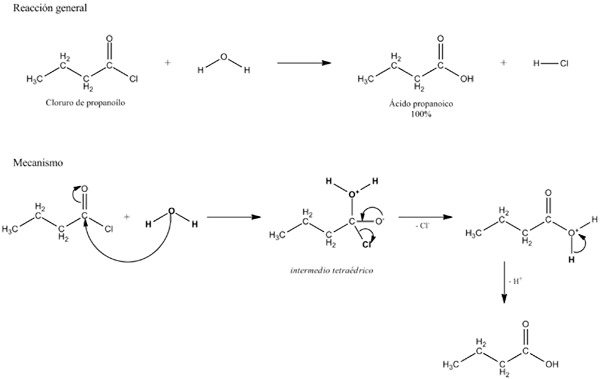
L'image supérieure explique quelle est l'hydrolyse. Notez que non seulement la molécule ou le substrat (s'ils médient les enzymes) rompent leur lien, mais aussi l'eau elle-même, qui est "fracture" dans H+ et oh-, Où h+ se termine par A, et oh- avec B. A-B réagit avec une molécule d'eau à l'origine de deux produits, A-H et B-OH.
L'hydrolyse est donc la réaction contraire à la condensation. Dans la condensation, deux produits, pour dire A-H et B-OH, sont liés par la libération d'une petite molécule: l'eau. Dans l'hydrolyse, une molécule est consommée, tandis qu'en condensation, il est libéré ou produit.
Il peut vous servir: groupe carbonyle: caractéristiques, propriétés, nomenclature, réactivitéRevenant à l'exemple des sucres, supposons que A-B correspond à un dimère de saccharose, où il représente le glucose et le fructose B. Le lien glucosidique A-B peut hydrolyzariser pour créer les deux monosaccharides séparément et en solution, et il en va de même pour l'oligo et les polysaccharides s'ils médient les enzymes dans de telles réactions.
Notez que dans cette réaction, celle de A-B, la flèche n'a qu'une seule adresse; c'est-à-dire, c'est une hydrolyse irréversible. Cependant, de nombreuses hydrolyse sont en fait des réactions réversibles qui atteignent un équilibre.
Exemples de réactions d'hydrolyse
- ATP
L'ATP est stable entre les valeurs de pH de 6,8 et 7,4. Cependant, à des valeurs de pH extrêmes, il est spontanément hydrolysé. Chez les êtres vivants, l'hydrolyse est catalysée par des enzymes appelées atasas:
ATP + H2O => ADP + PI
Cette réaction est fortement exergonique, car l'entropie de l'ADP est supérieure à celle de l'ATP. La variation énergétique libre de Gibbs (ΔGº) est - 30,5 kJ / mol. L'énergie produite par l'hydrolyse de l'ATP est utilisée dans de nombreuses réactions d'enders.
Réactions couplées
Dans certains cas, l'hydrolyse ATP est utilisée pour la conversion d'un composé dans un composé (b).
A + ATP + H2Ou b + adp + pi + h+
- Eau
Deux molécules d'eau peuvent réagir l'une à l'autre dans une hydrolyse apparente:
H2Ou + h2Ou h3SOIT+ + Oh-
C'est comme si l'une de ces molécules d'eau fracturées en h+ et oh-, va lier le h+ À l'atome d'oxygène de l'autre molécule d'eau, ce qui provoque l'ion hydrum, H3SOIT+. Cette réaction, plus que l'hydrolyse, concerne l'auto-propotolyse de l'eau.
Peut vous servir: énergie d'activation- Protéines
Les protéines sont des macromolécules stables et pour obtenir leur hydrolyse complète, dans les acides aminés qui les constituent, des conditions extrêmes sont nécessaires; comme une concentration d'acide chlorhydrique (6 m) et de températures élevées.
Cependant, les êtres vivants sont dotés d'un arsenal enzymatique qui permet l'hydrolyse des protéines dans les acides aminés dans le duodénum. Les enzymes impliquées dans la digestion des protéines sont presque complètement sécrétées par le pancréas.
Il existe des enzymes exopectidases qui dégradent les protéines, à partir de leurs extrémités: l'amipeptidase à travers l'extrémité amino et la carboxypeptidase à travers l'extrémité carboxyle. Les enzymes de l'endopeptidase exercent leur action à l'intérieur de la chaîne de protéines, par exemple: triple, pepsine, chimotripsin, etc.
- Amidas et esters
Les amides lorsqu'ils sont chauffés dans un milieu alcalin proviennent d'un acide carboxylique et d'une amine:
Rconh2 + H2O => rcoo- + NH2
Les abeats dans un milieu aqueux sont hydrolysés dans un acide carboxylique et de l'alcool. Le processus est catalysé soit par une base ou un acide:
Rco-or '+ h2O => rcooh + r'oh
Ceci est la célèbre réaction de saponification.
- Base acide
Dans l'eau, plusieurs espèces sont hydrolysées pour acidifier ou alcaliser l'environnement aqueux.
Ajout d'un sel de base
L'acétate de sodium, un sel de base, se dissocie dans l'eau donnant des ions na+ (sodium) et cho3Roucouler- (acétate). Sa basicité est parce que l'acétate est hydrolysé pour générer des ions oh-, Alors que le sodium reste inchangé:
Ch3Roucouler- + H2Ou ch3COOH + OH-
Il peut vous servir: salicylate de méthyleOH- Il est responsable du pH pour augmenter et devenir basique.
Ajout d'un sel acide
Chlorure d'ammonium (NH4Cl) est formé par l'ion chlorure (Cl-) de l'acide chlorhydrique (HCl), un acide fort et le cation ammonium (NH4+) à partir de l'hydroxyde d'ammonium (NH4Oh), une base faible. Le CL- Il ne se dissocie pas dans l'eau, mais le cation ammonium est transformé en eau de la manière suivante:
NH4+ + H2Ou NH3 + H3SOIT+
L'hydrolyse du cation ammonium produit des protons qui augmentent l'acidité d'un milieu aqueux, il est donc conclu que le NH4Cl est un sel acide.
Ajout d'un sel neutre
Le chlorure de sodium (NaCl) est un produit de sel de la réaction d'une base forte (NaOH) avec un acide fort (HCL). Lors de la dissolution du chlorure de sodium dans l'eau, le cation sodium est produit (na+) et l'anion (Cl-). Les deux ions ne se dissocient pas dans l'eau, donc ils n'ajoutent pas H+ ou oh-, Garder votre pH constant.
Par conséquent, on dit que le chlorure de sodium est un sel neutre.
Les références
- Mathews, C. K., Van Holde, K. ET. Et ahern, k. g. (2002). Biochimie. (Troisième édition). Modifier. Pearson-Addison Wesley.
- Whitten, Davis, Peck & Stanley. (2008). Chimie. (8e Ed.). Cengage Learning.
- Helmestine, Anne Marie, Ph.D. (13 janvier 2019). Hydrolyse: définition et exemple. Récupéré de: Thoughtco.com
- Theresa Phillips. (28 avril 2019). Une explication du processus d'hydrolyse. Récupéré de: the balance.com
- Les éditeurs d'Enyclopaedia Britannica. (16 novembre 2016). Hydrolyse. Encyclopædia Britannica. Récupéré de: Britannica.com
- Wikipédia. (2019). Hydrolyse. Récupéré de: dans.Wikipédia.org
- « Caractéristiques de Hyracotherium, nutrition, espèces, reproduction
- History of Origins Games vidéo à la réalité virtuelle »

