Hafnium

- 1270
- 173
- Raphaël Meyer
 Échantillon de hafnio métallique. Source: Images haute résolution d'éléments chimiques [cc par (https: // createVecommons.Org / licences / par / 3.0)]
Échantillon de hafnio métallique. Source: Images haute résolution d'éléments chimiques [cc par (https: // createVecommons.Org / licences / par / 3.0)] Qu'est-ce que Hafnio?
Il hafnium C'est un métal de transition dont le produit chimique est HF et a un nombre atomique de 72. Il s'agit du troisième élément du groupe 4 du tableau périodique, congelant dans le titane et la circonstance. Avec ce dernier, il partage de nombreuses propriétés chimiques, étant situées ensemble dans des minéraux de la croûte terrestre.
La recherche du Hafnio cherche où le zirconium, car c'est un sous-produit de son extraction. Le nom de ce métal vient du mot latin «Hafnia», dont le sens est le nom de Copenhague, une ville où il a été découvert dans les minéraux du zircon et la controverse s'est terminée par rapport à sa véritable nature chimique.
Ce métal prend la distinction d'être le dernier des éléments les plus stables découverts ici sur terre; c'est-à-dire que les autres découvertes ont constitué une série d'isotopes UltraSados, radioactifs et / ou artificiels.
Les composés hafnio sont analogues au titane et à la circonium, principalement le numéro d'oxydation +4, comme HFCL4, HFO2, HFI4 et hfbr4. Certains d'entre eux mènent la liste des matériaux les plus réfractaires jamais créés, ainsi que des alliages de grande résistance thermique et agit également comme d'excellents absorbants à neutrons.
Pour cette raison, le Hafnio a beaucoup de participation à la chimie nucléaire, en particulier aux réacteurs d'eau de pression.
Découverte
Transition métal ou terres rares
La découverte du Hafnio a été entourée de controverses, bien que son existence soit déjà prévue depuis 1869 grâce au tableau périodique de Mendeleev.
Le problème était qu'il était positionné sous le zirconium, mais a coïncidé dans la même période des éléments des terres rares: Lantanoides. Les chimistes à l'époque ne savaient pas s'il s'agissait d'un métal de transition ou d'un métal de terres rares.
 99,9% de hafnium bar. Source-Alchemist-HP (www.Pse-mendelejew.de), cc by-sa 2.0, via Wikimedia Commons
99,9% de hafnium bar. Source-Alchemist-HP (www.Pse-mendelejew.de), cc by-sa 2.0, via Wikimedia Commons Le chimiste français Georges Urbain, découvreur de Luthacio, métal voisin du Hafnio, a déclaré en 1911 qu'il avait découvert l'élément 72, que Celtio a appelé et proclamé qu'il s'agissait d'un métal des terres rares. Mais trois ans plus tard, il a été conclu que ses résultats étaient mauvais et qu'il n'avait isolé qu'un mélange de Lantanoides.
Ce n'est que lorsque les éléments ont été ordonnés par leur nombre atomique, grâce au travail d'Henry Moseley en 1914, que le quartier entre Luthate et Element 72 était la preuve du même groupe que le titane et les métaux de circontiement.
Peut vous servir: floculation: réaction, types, applications, exemplesDétection à Copenhague
En 1921, après les études de la structure atomique de Niels Bohr et sa prédiction du spectre d'émission des rayons x pour l'élément 72, ce métal a été arrêté dans les minéraux des terres rares; Et au lieu de cela, sa recherche sur les minéraux de la circonium s'est concentré, car les deux éléments ont dû partager plusieurs propriétés chimiques.
Le chimiste danois Dirk Coster et le chimiste hongrois Georg von Hevesy en 1923 ont finalement reconnu le spectre prévu de Niels Bohr dans des échantillons de zircon de Norvège et du Groenland. Après avoir fait la découverte à Copenhague, ils ont appelé l'élément 72 par le nom latin de cette ville: Hafnia, qui a dérivé plus tard 'Hafnio'.
Isolement et production
Cependant, ce n'était pas une tâche facile. Bien qu'en 1924 une méthode ait été conçue par recristallisation fractionnaire pour obtenir du tétrachlorure de hafnio, HFCL4, Ce sont les produits chimiques néerlandais Anton Eduard Van Arkel et Jan Hendrik de Boer qui l'ont réduit au hafnium métallique.
Pour ce faire, le HFCL4 Il a subi une réduction en utilisant du magnésium métallique (procédé Kroll):
HFCL4 + 2 mg (1100 ° C) → 2 mgcl2 + HF
D'un autre côté, à partir de Hafnio Tetrayoduro, Hfi4, Cela a été vaporisé pour subir une décomposition thermique sur un filament de tungstène à incandescence, sur lequel le hafnium métallique a été déposé pour provoquer une barre d'apparence polycristalline (processus de barre cristalline ou processus Arkel-Boer):
HFI4 (1700 ° C) → Hf + 2 I2
Structure hafnio
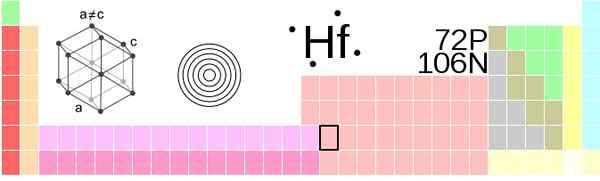 Hafnio Emplacement dans le tableau périodique. Fontaine: !Original: Ahoteseiervector: Sushant Savla, CC BY-SA 3.0, via Wikimedia Commons
Hafnio Emplacement dans le tableau périodique. Fontaine: !Original: Ahoteseiervector: Sushant Savla, CC BY-SA 3.0, via Wikimedia Commons Hafnio, les atomes HF, sont regroupés en pression ambiante sur une structure hexagonale compacte cristal, HCP, tout comme les métaux en titane et en zirconium. Ce cristal de hcp hafnio devient sa phase α, qui reste constant jusqu'à une température de 2030 K, lorsqu'il souffre d'une transition vers la phase β, avec une structure cubique centrée dans le corps, BCC.
Ceci est compris si la chaleur "détend" le verre est considéré et, par conséquent, les atomes HF cherchent à se positionner de telle manière que leur compactage diminue. Ces deux phases sont suffisantes pour considérer le polymorphisme du hafnium.
Il présente également un polymorphisme qui dépend des pressions élevées. Les phases α et β existent à une pression de 1 atm; Tandis que le ω, une phase hexagonale mais encore plus compactée que le HCP ordinaire, apparaît lorsque les pressions dépassent 40 GPa. Fait intéressant, lorsque les pressions continuent d'augmenter, la phase β réapparaît, la moins dense.
Peut vous servir: acide sélénhydrique (H2SE): Qu'est-ce que la structure, les propriétés, les utilisationsPropriétés de Hafnio
Apparence physique
Selon blanc en argent, qui montre des tons sombres s'il a une couche d'oxyde et de nitrure.
Masse molaire
178,49 g / mol
Point de fusion
2233 ºC
Point d'ébullition
4603 ºC
Densité
À température ambiante: 13,31 g / cm3, Être deux fois plus dense que le circon
Juste au point de fusion: 12 g / cm3
Chaleur de fusion
27,2 kJ / mol
Chaleur de vaporisation
648 kJ / mol
Électronégativité
1.3 sur l'échelle Pauling
Énergies d'ionisation
Premièrement: 658,5 kJ / mol (HF+ gazeux)
Deuxième: 1440 kJ / mol (HF2+ gazeux)
Troisième: 2250 kJ / mol (HF3+ gazeux)
Conductivité thermique
23,0 w / (m · k)
Résistivité électrique
331 nΩ · m
Dureté mohs
5.5
Réactivité
À moins que le métal ne soit Pula et Burns, tirant des étincelles à une température de 2000 ºC, il n'a pas de sensibilité à l'oxydation ou à la course, car une fine couche de son oxyde le protège. En ce sens, c'est l'un des métaux les plus stables. En fait, les acides ou les bases fortes peuvent le dissoudre; À l'exception de l'acide fluorhorhorique et des halogènes capables de l'oxyder.
Configuration électronique
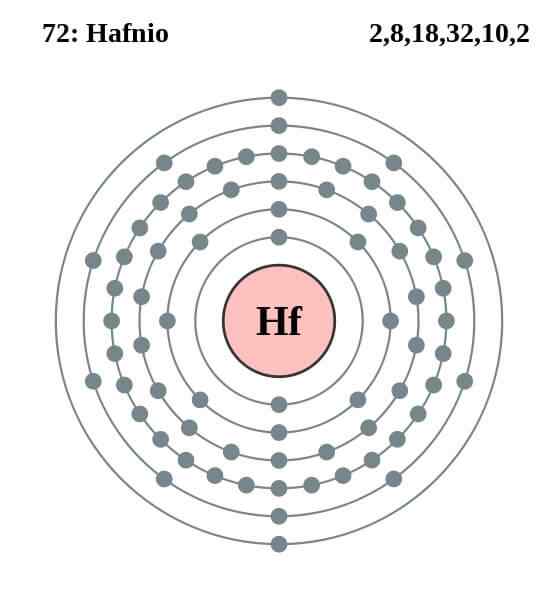 Configuration électronique Hafnio
Configuration électronique Hafnio L'atome de Hafnio a la configuration électronique suivante:
[XE] 4F14 5 D2 6s2
Cela coïncide avec le fait d'appartenir au groupe 4 du tableau périodique, avec le titane et le circonium, car il a quatre électrons de Valence dans les orbitales 5D et 6S. Notez que le Hafnio ne pourrait pas être un lantanoide, car il a ses orbitales 4F complètement complètes.
Nombres d'oxydation
La même configuration électronique révèle le nombre d'électrons capables de perdre un atome de hafnio lorsqu'il fait partie d'un composé. En supposant qu'il perd ses quatre électrons de Valence, il serait un cation tétravalent hf4+ (Par analogie avec vous4+ et zr4+), Et aurait donc un nombre d'oxydation de +4.
C'est en fait le plus stable et le plus commun de ses nombres d'oxydation. Les autres moins pertinents sont: -2 (hf2-), +1 (hf+), +2 (hf2+) et +3 (hf3+).
Isotopes
Hafnio est présenté sur Terre comme cinq isotopes stables et radioactifs avec un très grand moment de la vie:
-174HF (0,16%, avec une demi-vie de 2 · 10quinze années, il est donc considéré comme pratiquement stable)
-176HF (5,26%)
-177HF (18,60%)
Peut vous servir: bases faibles-178HF (27,28%)
-179HF (13,62%)
-180HF (35,08%)
Notez qu'il n'y a pas un tel isotope en tant que tel qui se démarque en abondance, et cela se reflète dans la masse atomique moyenne du Hafnio, 178.49 Uma.
De toutes les isotopes radioactifs du Hafnio, qui avec les indigènes total un total de 34, le 178m2HF est le plus controversé car dans sa décroissance radioactive libère le rayonnement gamma, ces atomes pourraient donc être utilisés comme une pistolet de guerre.
Utilisations / applications
 Hafnio recouvert d'une fine couche d'oxyde. Source: Alchemist-HP (Talk) (www.Pse-mendelejew.De), fal, via Wikimedia Commons
Hafnio recouvert d'une fine couche d'oxyde. Source: Alchemist-HP (Talk) (www.Pse-mendelejew.De), fal, via Wikimedia Commons Réactions nucléaires
Hafnio est un métal résistant à l'humidité et des températures élevées, en plus d'être un excellent absorbant à neutrons. Pour cette raison, il est utilisé dans les réacteurs à eau de pression, ainsi que dans la fabrication de barres de contrôle pour les réacteurs nucléaires, dans les revêtements duquel ils sont en ultrapuro circu.
Alliages
Les atomes de hafnio peuvent intégrer d'autres cristaux métalliques pour donner naissance à différents alliages. Ceux-ci sont caractérisés par un tenace et thermiquement résistant, ils sont donc destinés à des applications spatiales, comme dans la construction de buses de moteur pour les roquettes.
D'un autre côté, certains alliages et composés solides de Hafnio ont des propriétés spéciales; comme leurs carbures et nituros, HFC et HFN, respectivement, qui sont des matériaux très réfractaires. Tantalo et Hafnio Carbide, Ta4HFC5, Avec un point de fusion de 4215 ºC, c'est l'un des matériaux les plus réfractaires jamais connus.
Catalyse
Les métalocènes de Hafnio sont utilisés comme catalyseurs organiques pour la synthèse du polymélène tels que le polyéthylène et le polystyrène.
Des risques
On ne sait pas à ce jour quel impact les ions HF pourraient avoir dans notre corps4+. D'un autre côté, parce qu'ils se trouvent dans la nature dans les minéraux du zirconium, il n'est pas cru qu'ils puissent modifier l'écosystème de libération de leurs sels à l'environnement.
Maintenant, il est recommandé de manipuler soigneusement les composés de Hafnio, comme s'ils étaient toxiques, même s'il n'y a pas d'études médicales qui prouvent qu'elles sont nocives pour la santé.
Le véritable danger du Hafnio réside dans les particules de son solide finement moulu, qui peut brûler juste au moment où ils entrent en contact avec l'oxygène de l'air.
Cela explique pourquoi, lorsqu'il est poli, une action qui gratte sa surface et dégage des particules de métal pur, des étincelles brûlantes sont libérées avec une température de 2000 ºC; c'est-à-dire que le Hafnio présente la pyroporicité, la seule propriété qui implique des risques d'incendie ou de brûlures graves.

