Caractéristiques de Fucosa, structure, fonctions
- 2160
- 639
- Lucas Schneider
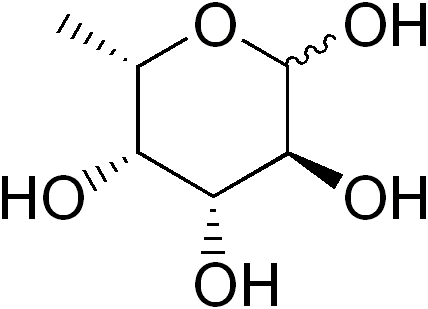
La Fucosa (FUC abrégé), ou 6-L-dexi-galactose, c'est un monosaccharide partiellement de la désoxigène (Deoxiazúcar) de six carbones dont la formule empirique est C est C est6H12SOIT5. Comme les autres monosaccharides, c'est un sucre polyhydroxylé.
Lorsqu'un groupe hydroxyle est remplacé par un atome d'hydrogène, un désoxiazúcar est dérivé. Bien que théoriquement, ce remplacement pourrait affecter tout groupe hydroxyle de tout monosaccharide, il y a peu de variété de dexiazúcús.
 Source: EDGAR181 [Domaine public]
Source: EDGAR181 [Domaine public] Certains déoxiazúces sont: 1) la désoxyribosa (2-di-disoxxi-d-libose), dérivée du d-libose, qui fait partie de l'ADN; 2) Le Ramnosa (6-D-Dexxi-marso), dérivé du D-Manosa; 3) Fucosa, dérivée du l-galactose. Ce dernier est plus fréquent que d-fucosa, dérivé du d-galactose.
[TOC]
Caractéristiques et structure
Fucosa est également connu avec des noms 6-disoxxi-scalact-hexose, fucopiranous, galactométhyl et rade.
Bien qu'il forme normalement des polysaccharides et des glycoprotéines, isolés comme monosaccharide est plus doux que le galactose. En effet.
Les groupes Hydroxyle Fucosa peuvent subir les mêmes réactions que les autres sucres, produisant une grande variété d'acétals, de glycosides, d'éthers et d'esters.
Une biomolécule fucosilate. Lorsque l'hydrolyse des liaisons glycosidiques se produit par l'action d'une fucosidase, séparant ainsi la fucosa, il est dit que la biomolécule a été déficosylée.
Lorsque les glucanos fucosyl, des glucanes plus complexes appelés fucanos sont générés, ce qui peut ou non faire partie des glycoprotéines. Les fucans sulfate sont définis comme les polysaccharides qui contiennent des résidus de sulfate de L-Fucosa. Ils sont typiques des algues brunes. À titre d'exemples, ils peuvent être nommés Ascophilano, Sargasano et le Pelvetano.
L'un des fucanos les mieux étudiés est le fucoidano, obtenu à partir des algues brunes Fucus vesiculosus, qui est commercialisé (Sigma-Aldrich Chemical Company) depuis des décennies.
Peut vous servir: quel est l'erristeneo?Distribution dans la nature
Le D-fucose est présent dans les substances antibiotiques produites par les microbes, et dans les glycosides végétaux, tels que le convolage, la charrtreusine, le ledienosida et la Queirotoxine.
Le L-fucose est un constituant des polysaccharides des algues, les feuilles de la prune, les doublures du linge, du soja et du canola, le caoutchouc tragacanto, les parois cellulaires de la pomme de terre, les tubes du Cassava, le fruit du kiwi, Le cortex du ceiba et du mucigel du caliptra de maïs, ainsi que d'autres plantes.
La Fucosa est également présente dans les œufs d'oursin et dans la gelée qui protège les œufs de grenouille.
Chez les mammifères, les fucans atteints de l-fucosa forment les ligands qui agissent dans l'adhésion leucocytaire-endothéliale médiée par la sélection et participent à de nombreux événements ontogénétiques.
La Fucosa abonde dans les fucosphingolipides de l'épithélium gastro-intestinal et de la moelle osseuse, et apparaît dans de petites proportions dans le cartilage et les structures kératiennes.
Chez l'homme, les fucanos atteints de l-fucosa font partie des glycoprotéines de salive et des jus gastriques. Ils font également partie des antigènes qui définissent les groupes sanguins ABO. Ils sont présents dans plusieurs oligosaccharides de lait maternel.
Métabolisme de la fucosa
Les fucosyltransférases utilisent le PIB-fucose, une forme fucosa activée par des nucléotides, comme donneur de fucosa dans la construction d'oligosaccharides fucosylés.
Le PIB-Fucosa est dérivé du PIB-Manosa pour l'action successive de deux enzymes: le PIB-Manasea 4.6-dehydratasa et le PIB-4-ZO-6-Desoximanosa 3.5-Epimeasa-4-réducase.
Uitlisant un cofacteur NADP +, la première enzyme catalyse la déshydratation du PIB-Many. La réduction de la position 6 et l'oxydation de la position 4 produisent le PIB-6-desoxi-4-céto-koaming (pendant la réaction, l'hybride est transféré de la position 4 à 6 du sucre).
La deuxième enzyme, qui dépend du NADPH, catalyse l'épimérisation des positions 3 et 5, et le réseau du groupe 4-ZO, du PIB-6-desoxi-4-ecto-marsa.
Les bactéries peuvent se développer en utilisant la fucosa comme une seule source de carbone et d'énergie à travers une opeone inductible par la fucosa qui code pour les enzymes cataboliques pour ce sucre.
Peut vous servir: acide carboxyliqueLe processus précédent implique: 1) l'entrée de Fucosa libre à travers la paroi cellulaire avec médiation d'une perméase; 2) l'isomérisation de la fucosa (un aldosa) pour former un fucucule (un zea); 3) phosphorylation du fuculeuse pour former un phosphate fuucule-1; 4) une réaction de l'aldolase pour former le lactaldéhyde et la dihydroxyacétone phosphate à partir de phosphate fuucule-1-phosphate.
Les fonctions
Papier cancer
Parmi les symptômes de nombreux types de tumeurs cancérigènes figurent la présence de protéines liées au glucane qui se distinguent par une composition altérée des oligosaccharides. La présence de ces glucanes anormaux, parmi lesquels des fucanos se démarquent, est lié à la tumeur maligne et au potentiel métastatique de ces tumeurs.
Dans le cancer du sein, les cellules tumorales intègrent la fucosa dans les glycoprotéines et les glycolipides. Fucosa contribue à la progression de ce cancer, favorisant l'activation des cellules souches cancéreuses, des métastases hématogènes et l'invasion des tumeurs à travers des matrices extracellulaires.
Dans le carcinome pulmonaire et l'hépatocarcinogenèse, l'expression augmentée de la fucosa est liée à un potentiel métastatique élevé et à une faible probabilité de survie.
En tant que homologue, certains fucanos sulfatés sont des substances prometteuses dans le traitement du cancer, comme déterminé.
Papier dans d'autres maladies
L'expression augmentée des fucanos dans les immunoglobulines sériques a été liée à la polyarthrite rhumatoïde juvénile et adulte.
La carence en adhésion des leucocytes II est une maladie congénitale rare due à des mutations qui modifient l'activité d'un transporteur FDP-fucose situé dans l'appareil de Golgi.
Les patients souffrent de retard mental et psychomotrice et souffrent d'infections bactériennes récurrentes. Cette maladie répond favorablement aux doses de fucosa orales.
Potentiel biomédical
Les fucanos sulfate obtenus à partir d'algues brunes sont des réservoirs importants de composés avec un potentiel thérapeutique.
Il peut vous servir: ititrum: structure, propriétés, utilisations, obtentionIls ont des propriétés anti-inflammatoires et antioxydantes, inhibant la migration des lymphocytes dans les sites d'infection et favorisant la libération de cytokines. Augmentez la réponse immunitaire en activant les lymphocytes et les macrophages.
Ils ont des propriétés anticoagulantes. Il a été prouvé chez les patients humains qui inhibent oralement l'agrégation plaquettaire.
Ils ont un potentiel antibiotique et antiparasite et inhibent la croissance des bactéries pathogènes de l'estomac Helicobacter pylori. Tuer les parasites Plasmodium spp. (Agent causal du paludisme) et Leishmania Donovani (Agent causal de la leishmaniose viséotrope américaine).
Enfin, ils ont de puissantes propriétés antivirales, inhibant l'entrée dans la cellule de plusieurs virus d'une grande importance pour la santé humaine, notamment Arénavirus, Cytomégalovirus, Hantavirus, Hépadnavirus, VIH, virus de l'herpès simplex et virus de la grippe.
Les références
- Becker, D. J., Lowe, J. B. 2003. Fucose: biosynthèse et fonction biologique chez les mammifères. Glycobiology, 13, 41R-53R.
- Deniaud-bouët, e., Hardouin, k., Potin, p., Kloareg, B., Hervé, C. 2017. Une revue sur les parois cellulaires des algues brunes et les polysaccharides sulfatés contenant du fucose: contexte de la paroi cellulaire, propriétés biomédicales et défis de recherche clés.Polymères glucidiques, http: // dx.est ce que je.org / 10.1016 / j.Carbo.2017.07.082.
- Fleurs H. M. 1981. Chimie et biochimie de D et L-fucose. Advances in Garbohydrate Chimistry and Biochemistry, 39, 279-345.
- Listinsky, J. J., Siegal, G. P., Listinsky, c. M. 2011. L'importance émergente de α-L-fucose dans le cancer du sein humain: une revue. SUIS. J. Traduire. Bœuf., 3, 292-322.
- Murray, R. K., et al. 2003. Biochimie illustrée de Harper. McGraw-Hill, New York.
- Pereira, l. 2018. Utilisations thérapeutiques et nutritionnelles des algues. CRC Press, Boca Raton.
- Staudacher, E., Altmann, F., Wilson, je. B. H., März, L. 1999. Fucose en n-glycanes: de plante à l'homme. Biochimica et Biophysica Acta, 1473, 216-236.
- Tanner, W., Loewus, F. POUR. 1981. Glucides végétaux II. Glucides extracellulaires. Springer, New York.
- Vanhohen, P. T., Vandamme, e. J. 1999. L-fucose: occurrence, rôle physiologique, synthèse chimique, enzymatique et microbienne. Journal of Chemical Technology and Biotechnology, 74, 479-497.
- « Emplacement du cercle polaire de l'Antarctique, caractéristiques, flore et faune
- Phases de chimiosynthèse, organismes, différences avec la photosynthèse »

