Etano
- 1870
- 513
- Raphaël Charles
 Structure estano
Structure estano Qu'est-ce que l'éthane?
Il Etano C'est un hydrocarbure de formule C simple2H6 Avec une nature incolore et des gaz toilettes qui a une utilisation très précieuse et diversifiée dans la synthèse de l'éthylène. De plus, c'est l'un des gaz terrestres qui a également été détecté dans d'autres planètes et corps d'étoiles autour du système solaire. Il a été découvert par le scientifique Michael Faraday en 1834.
Parmi le grand nombre de composés organiques formés par des atomes de carbone et d'hydrogène (appelés hydrocarbures), il y a ceux qui sont dans un état gazeux à des températures et des pressions environnementales, qui sont grandement utilisées dans de nombreuses industries.
Ceux-ci proviennent généralement du mélange gazeux appelé «gaz naturel», un produit de grande valeur pour l'humanité et constituent les types de méthane, d'éthane, de propane et de butane, entre autres; se qualifier en fonction de la quantité d'atomes de carbone dans sa chaîne.
Structure chimique de l'éthane
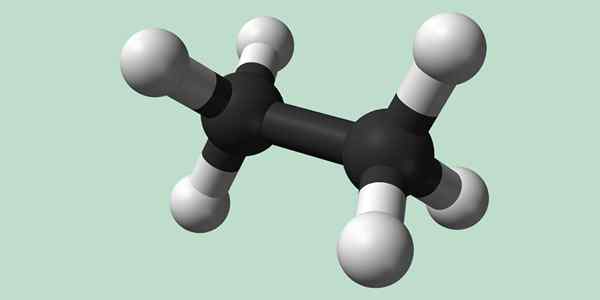
Estano est une molécule de formule C2H6, généralement considéré comme une union de deux groupes méthyles (-ch3) Pour former les hydrocarbures d'une simple liaison carbone-carbone. C'est aussi le composé organique le plus simple après le méthane, se représentant:
H3C-ch3
Les atomes de carbone dans cette molécule ont une hybridation du type SP3, Les liaisons moléculaires ont donc une rotation libre.
Il existe également un phénomène intrinsèque d'Etano, qui est basé sur la rotation de sa structure moléculaire et l'énergie minimale requise pour produire une rotation de liaison à 360 degrés, que les scientifiques ont appelé "Etano Barrera".
Pour cette raison, Ethan.
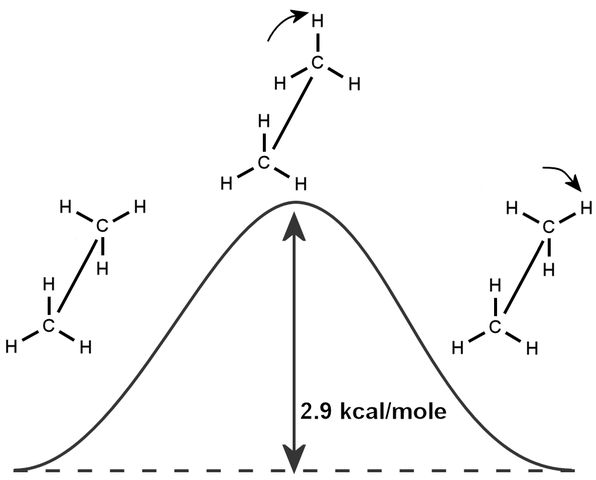 Structure chimique de l'éthane. Source: Wikimedia Commons
Structure chimique de l'éthane. Source: Wikimedia Commons Synthèse de l'éthane
Estano peut facilement être synthétisé à partir de l'électrolyse de Kolbe, une réaction organique dans laquelle deux étapes se produisent: une décarboxylation électrochimique (élimination du groupe carboxyle et libération du dioxyde de carbone) de deux acides carboxyliques, et la combinaison des intermédiaires de produits pour former une liaison covalente, et la combinaison des produits intermédiaires pour former une liaison covalente.
De même, l'électrolyse en acide acétique entraîne la formation de dioxyde d'éthane et de carbone, et cette réaction est utilisée pour synthétiser le premier.
L'oxydation de l'anhydride acétique par l'action des peroxydes, un concept similaire à l'électrolyse de Kolbe, entraîne également la formation de l'éthane.
Peut vous servir: contributions de la chimie à l'humanitéDe la même manière, il peut être séparé efficacement du gaz naturel et du méthane par un processus de liquéfaction, en utilisant des systèmes cryogéniques pour capturer ce gaz et le séparer des mélanges avec d'autres gaz.
Le processus d'extension turbo est le favori pour ce rôle: le mélange de gaz est fabriqué par une turbine, générant une expansion de celui-ci, jusqu'à ce que sa température tombe en dessous de -100 ° C.
Déjà à ce stade, les composants du mélange peuvent être différenciés, donc l'éthane liquide du méthane gazeux et les autres espèces impliquées dans l'utilisation d'une distillation seront séparées.
Propriétés estano
Estano est présenté dans la nature comme des toilettes et du gaz incolore aux pressions et températures standard (1 atm et 25 ° C). Il a un point d'ébullition de -88,5 ° C et un point de fusion de -182,8 ° C. De plus, il n'est pas affecté par l'exposition à de forts acides ou bases.
Solubilité de l'éthane
Les molécules Etano sont une configuration symétrique et ont des forces d'attraction faibles qui les maintiennent ensemble, appelées forces de dispersion.
Lorsque l'éthane essaie de se dissoudre dans l'eau, les forces d'attraction formées entre le gaz et le liquide sont très faibles, de sorte que l'éthane se joindra à peine aux molécules d'eau.
Pour cette raison, la solubilité de l'éthane est considérablement faible, augmentant légèrement lorsque la pression du système augmente.
Cristallisation de l'éthane
Estano peut être solidifié, faisant des cristaux d'éthane instables avec une structure cristalline cubique.
Avec une diminution de la température au-delà de -183,2 ° C, cette structure devient monoclinique, augmentant la stabilité de sa molécule.
Combustion de l'éthane
Cet hydrocarbure, même lorsqu'il n'est pas largement utilisé comme carburant, peut être utilisé dans les processus de combustion pour générer du dioxyde de carbone, de l'eau et de la chaleur, qui est représenté comme suit:
2 c2H6 + 7e2 → 4CO2 + 6h2O + 3120 KJ
Il existe également la possibilité de brûler cette molécule sans excès d'oxygène, qui est connu sous le nom de "combustion incomplète", et qui se traduit par la formation de carbone amorphe et de monoxyde de carbone dans une réaction indésirable, selon la quantité d'oxygène appliqué:
Peut vous servir: STEROLS: Structure, fonctions et exemples2 c2H6 + 3e2 → 4C + 6H2Ou + chaleur
2 c2H6 + 4e2 → 2C + 2CO + 6H2Ou + chaleur
2 c2H6 + 5e2 → 4CO + 6H2Ou + chaleur
Dans ce domaine, la combustion se produit par une série de réactions radicales libres, qui sont numérotées dans les centaines de réactions différentes. Par exemple, dans des réactions de combustion incomplètes, des composés tels que le formaldéhyde, l'acétaldéhyde, le méthane, le méthanol et l'éthanol peuvent être formés.
Cela dépendra des conditions dans lesquelles la réaction et les réactions des radicaux libres impliqués se produisent. L'éthylène peut également se former à des températures élevées (600-900 ° C), qui est un produit hautement souhaité par l'industrie.
Estano dans l'atmosphère et dans les corps célestes
Estano est présent dans l'atmosphère de la planète Terre en traces, et on soupçonne que l'être humain a réussi à doubler cette concentration depuis qu'il a commencé à pratiquer les activités industrielles.
Les scientifiques pensent qu'une grande partie de la présence actuelle de l'ETA dans l'atmosphère est due à la combustion de combustibles fossiles, bien que l'émission mondiale de l'éthane ait diminué presque à moitié depuis que les technologies de production de gaz Lutita ont été améliorées (une source de gaz naturel).
Cette espèce se produit également naturellement par l'effet des rayons solaires sur le méthane atmosphérique, qui recombines et forme une molécule d'éthane.
Il y a une éthane à l'état liquide à la surface de Titan, l'une des lunes de Saturne. Ceci est présenté en plus grande quantité sur la rivière VID Flumina, qui coule sur plus de 400 kilomètres à l'une de ses mers. Ce composé a également été mis en évidence sur les comètes et à la surface de Pluton.
Utilisations de l'éthane
Production d'éthylène
L'utilisation de l'éthane est principalement basée sur la production d'éthylène, le produit organique d'une plus grande utilisation dans la production mondiale, à travers un processus connu sous le nom de Steam Stage.
Ce processus consiste à passer un Ethan dilué.
La réaction se produit à une température extrêmement élevée (entre 850 et 900 ° C), mais le temps de séjour (le temps que l'éthane passe dans le four) doit être bref pour que la réaction soit efficace. À des températures plus élevées, plus d'éthylène est généré.
Peut vous servir: néon: historique, propriétés, structure, risques, utilisationsFormation chimique de base
Etano a également été étudié comme composant principal de la formation de produits chimiques de base. La chloration oxydative est l'un des processus soulevés pour obtenir du chlorure de vinyle (un composant en PVC), remplaçant les autres moins économiques et plus compliqués.
Réfrigérant
Enfin, l'éthane est utilisé comme réfrigérant dans les systèmes cryogéniques communs, montrant également des capacités de petits échantillons de gel en laboratoire pour analyse.
C'est un très bon substitut à l'eau, qui prend plus pour refroidir les échantillons délicats, et peut également générer la formation de cristaux de glace nocifs.
Risques d'éthane
-Estano a la capacité de devenir enflammé, principalement lorsqu'il rejoint l'air. Un pourcentages de 3,0 à 12,5% de volume d'éthane dans l'air, un mélange explosif peut être formé.
-Il peut limiter l'oxygène dans l'air dans lequel il se trouve, et pour cette raison, il présente un facteur de risque de suffocation pour les personnes et les animaux présents et exposés.
-L'éthane sous forme de liquide congelé peut sérieusement brûler la peau si elle entre en contact direct avec elle, et également agir comme un milieu cryogénique pour tout objet qui touche, le congelant en quelques instants.
-Les vapeurs de l'éthane liquide sont plus lourdes que l'air et se concentrent sur le sol, cela peut présenter un risque d'allumage qui peut générer une réaction de combustion de chaîne.
-L'ingestion d'étano peut provoquer des nausées, des vomissements et des hémorragies internes. L'inhalation, en plus de la suffocation, provoque des maux de tête, une confusion et un changement d'humour. La mort due à un arrêt cardiaque est possible lors d'expositions élevées.
-Il représente un gaz à effet de serre qui, avec le méthane et le dioxyde de carbone, contribue au chauffage mondial et au changement climatique généré par la pollution humaine. Heureusement, il est moins abondant et durable que le méthane, et absorbe moins de rayonnement que cela.
Les références
- Britannica, E. (s.F.). Éthane. Obtenu de Britannica.com
- Nes, g. V. (s.F.). Structures monocristallines et distribution de densité électronique de l'éthane, de l'éthhylène et de l'acétylène. Le tapis récupéré.Nl
- Sites, g. (s.F.). Éthane: sources et puits. Obtenu à partir de sites.Google.com
- Softschools (s.F.). Formule d'éthane. Récupéré des écoles softs.com
- Wikipedia (s.F.). Éthane. Obtenu à partir de.Wikipédia.org

