Structure tertiaire des principales caractéristiques Caractéristiques
- 4131
- 903
- Raphaël Charles
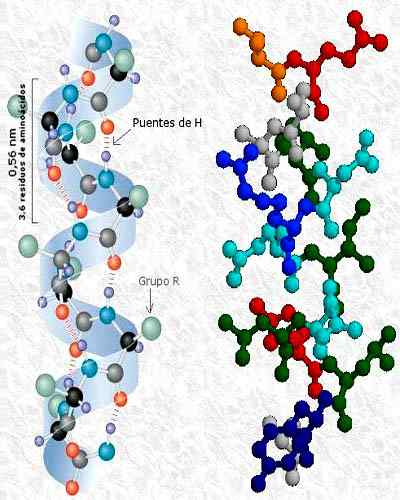
La Structure tertiaire des protéines C'est la conformation à trois dimensions que les chaînes de polypeptides acquièrent lorsqu'ils se plient sur eux-mêmes. Cette conformation apparaît par des interactions entre les chaînes latérales des déchets d'acides aminés du polypeptide. Les chaînes latérales peuvent interagir indépendamment de leur position dans la protéine.
Parce que cela dépend des interactions entre les groupes R, la structure tertiaire montre des aspects non perpétitifs de la chaîne, car ces groupes sont différents pour chaque résidu d'acide aminé. La structure secondaire, en revanche, dépend des groupes carboxyle et aminés, qui sont présents dans tous les acides aminés.
 Structure tertiaire de la protéine de la kinase phosphatase, avec des structures secondaires en alpha et en feuilles bêta. Pris et édité à partir de: A2-33. Modifié par Alejandro Porto. [CC BY-SA 3.0 (https: // CreativeCommons.Org / licences / by-sa / 3.0)].
Structure tertiaire de la protéine de la kinase phosphatase, avec des structures secondaires en alpha et en feuilles bêta. Pris et édité à partir de: A2-33. Modifié par Alejandro Porto. [CC BY-SA 3.0 (https: // CreativeCommons.Org / licences / by-sa / 3.0)].
Certains auteurs suggèrent que les protéines fibreuses ont une structure tertiaire simple, mais néanmoins, d'autres auteurs soulignent que cette structure est typique des protéines globulaires.
[TOC]
Protéines fibreuses
Dans les protéines fibreuses, les chaînes de polypeptides sont disposées sous forme de longs filaments ou de longues feuilles; Ils sont généralement constitués d'un type unique de structure secondaire. Cette structure secondaire est, dans la plupart des cas, plus importante que la structure tertiaire pour déterminer la forme des protéines.
Sa fonction biologique est structurelle, conférant une force et / ou une élasticité aux organes et aux structures où ils se trouvent, tout en les gardant ensemble. Toutes les protéines fibreuses sont insolubles dans l'eau, en raison de la grande quantité d'acides aminés hydrophobes qu'ils présentent.
Parmi ces protéines fibreuses figurent les kératines et le collagène. Les premiers se trouvent dans des tissus conjonctifs et dans des structures telles que les poils, les ongles (α-quératines), les échelles et les plumes (β-cheetés). Le collagène, quant à lui, se trouve dans les os, les tendons et la peau, entre autres.
α-questionnas
Ces protéines font partie des protéines des filaments intermédiaires SO appelés, qui jouent un rôle important dans le cytosquelette des organismes multicellulaires. De plus, ils sont le principal constituant des poils, des ongles, de la laine, des cornes, des sabots et l'une des principales protéines de la peau animale.
Peut vous servir: tache KinyounLa structure de la molécule est une hélice α. Deux brins d'α-quératine peuvent être disposés en parallèle et en inscrire l'un sur l'autre avec leurs groupes hydrophobes interagissant entre eux. De cette façon, une structure de superhéque ou de balle est créée avec un enroulement vers la gauche.
La structure tertiaire de la kératine α est simple et est dominée par la structure secondaire de l'hélix α. En revanche, la structure quaternaire est également présente, car deux molécules participent à la structure superhélicoïde, qui interagissent par des liaisons non covalentes.
β-questionnas
La structure principale est similaire à celle des α-quératines, mais sa structure secondaire est dominée par les feuilles β. Ils sont le principal constituant des échelles des reptiles et des plumes des oiseaux.
Collagène
Cette protéine peut représenter plus de 30% de la masse totale des protéines de certains animaux. Il se trouve dans les cartilagos, les os, les tendons, la cornée et la peau, entre autres tissus.
La structure secondaire du collagène est unique, représentée par une hélice Levogira avec 3,3 déchets d'acide aminé pour chaque tour. Trois chaînes d'hélice lévogie (α).
Les molécules de tropocollagènes se réunissent pour former une fibre de collagène qui a une grande résistance, supérieure à l'acier et comparable au cuivre à haute résistance.
Autres protéines fibreuses
Les autres types de protéines fibreux sont les fibroine et l'élastine. Le premier d'entre eux est formé par des feuilles β, principalement constituées par la glycina, l'alanine et la sérine.
Les chaînes latérales de ces acides aminés sont petites, donc elles peuvent être étroitement emballées. Le résultat est une fibre qui est à la fois très résistante et très non prouvée.
Peut vous servir: tampon de phosphate (PBS): fondation, préparation et utilisationsDans l'élastine, en attendant, la Valine remplace la sérine parmi ses principaux acides aminés constitutifs. Contrairement à Fibroine, Elastin est très extensible, d'où son nom. Dans la Constitution de la molécule, la lysine agit également, qui peut participer à la fulging.
Protéines globulaires
Les protéines globulaires, contrairement aux fibreuses, sont solubles et ont généralement plusieurs types de structures secondaires. Cependant, dans ces conformations à trois dimensions plus importantes qu'ils acquièrent lorsqu'ils se plient sur eux-mêmes (structure tertiaire).
Ces conformations à trois dimensions particulières donnent une activité biologique spécifique à chaque protéine. La fonction principale de ces protéines est la régulation, comme avec les enzymes.
Caractéristiques de la structure tertiaire des protéines globulaires
La structure tertiaire des protéines globulaires a des caractéristiques importantes:
- Les protéines globulaires sont compactes grâce à l'emballage lorsque la chaîne polypeptidique se replie.
- Les déchets d'acides aminés distants dans la structure primaire des chaînes polypeptidiques sont proches, pouvoir interagir les uns avec les autres en raison du pliage.
- Des protéines globulaires plus grandes (plus de 200 acides aminés) peuvent avoir plusieurs segments compacts, indépendants entre eux et avec des fonctions particulières, et chacun de ces segments est appelé domaine. Un domaine peut avoir entre 50 et 350 déchets d'acides aminés.
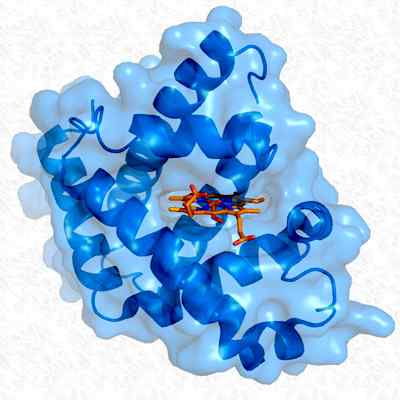 Structure tertiaire de la myoglobine. Pris et édité à partir de: Thomas Splettstoesser. Modifié par Alejandro Porto. [CC BY-SA 3.0 (https: // CreativeCommons.Org / licences / by-sa / 3.0)].
Structure tertiaire de la myoglobine. Pris et édité à partir de: Thomas Splettstoesser. Modifié par Alejandro Porto. [CC BY-SA 3.0 (https: // CreativeCommons.Org / licences / by-sa / 3.0)].
Règles générales du repliement des protéines mondiales
Comme déjà indiqué, les protéines ont des formes de pliage particulières, qui leur donnent également des caractéristiques particulières. Ce pliage n'est pas aléatoire et est favorisé à la fois par la structure primaire et secondaire et par certaines interactions non covalentes, et il y a aussi des restrictions physiques au pliage, donc certaines règles ont été formulées:
Peut vous servir: organes lymphoïdes primaires- Toutes les protéines globulaires ont défini des schémas de distribution, avec des groupes hydrophobes dirigés vers la molécule et les déchets hydrophiles dans la couche externe dans la couche externe. Pour cela, au moins deux couches de structure secondaire sont nécessaires. La boucle β-α-β et le sommet α-α peuvent contribuer ces deux couches.
- Les feuilles β sont généralement disposées sous une forme roulée de lévogira.
- Dans une chaîne polypeptidique, différents virages peuvent se produire pour passer d'une structure secondaire à une autre structure, telle que des virages β ou γ, qui peuvent investir la direction de la chaîne en quatre déchets d'acides aminés ou moins.
- Les protéines globulaires ont des feuilles α, β, des torsions et des segments structurés irrégulièrement.
Dénaturation des protéines
Si une protéine perd sa structure à trois dimensions indigène (naturelle), elle perd son activité biologique et la plupart de ses propriétés spécifiques. Ce processus est connu sous le nom de dénaturation.
La dénaturation peut se produire lorsque les conditions environnementales naturelles changent, par exemple par une température variable ou un pH. Le processus est irréversible dans de nombreuses protéines; Cependant, d'autres peuvent récupérer spontanément leur structure naturelle en restaurant des conditions environnementales normales.
Les références
- C.K. Mathews, k.ET. Van Hold & K.g. Ahern (2002). Biochimerie. 3e édition. Benjamin / Cummings Publishing Company, Inc.
- R.Murray, P. Mayes, D.C. Granner & V.W. Rodwell (1996). Biochemery de Harper. Appleton & Lange.
- J.M. Berg, J.L. Tymoczko & l. Stryer (2002). Biochimerie. 5e édition. W. H. Freeman et compagnie.
- W.M. Becker, L.J. Kleinsmith & J. Hardin (2006) World of the Cell. 6e édition. Pearson Education Inc.
- POUR.Lehninger (1978). Biochimie. Éditions Omega, S.POUR.
- T. McKee & J.R. McKee (2003). Biochimie: la base moléculaire de la vie. 3e édition. The McGraw-Hiii Companies, Inc.
- « Propriétés, applications et exemples des condensats fermioniques
- Structure de sulfate de sodium (SDS) DoDecil, propriétés, utilisations »

