Structure quaternaire des protéines caractéristiques
- 1281
- 95
- Mlle Ambre Dumont
La Structure quaternaire des protéines définit les relations spatiales entre chacune de ses sous-unités de polypeptides liés par des forces non covalentes. Dans les protéines polymères, chacune des chaînes polypeptidiques qui le composent sont appelées sous-unités ou protomères.
Les protéines peuvent être formées par une (monomère), deux (dimérica), plusieurs (oligomères) ou plusieurs protomères (polymère). Ces protomères peuvent avoir une structure moléculaire similaire ou très différente entre elles. Dans le premier cas, il est dit qu'ils sont des protéines homotypiques et dans le deuxième cas, hétérotypique.
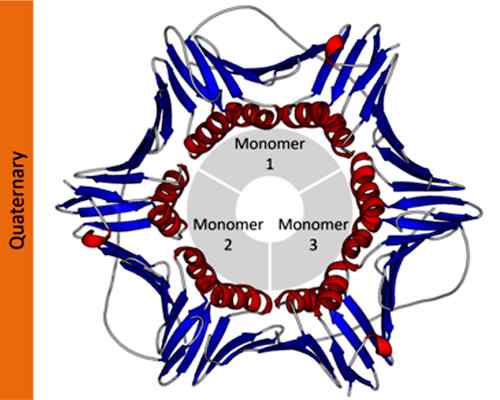
 Exemple de structure quaternaire d'une protéine d'antigène nucléaire cellulaire de prolifération. Pris et édité à partir de: Thomas Shafee [CC par 4.0 (https: // CreativeCommons.Org / licences / par / 4.0)].
Exemple de structure quaternaire d'une protéine d'antigène nucléaire cellulaire de prolifération. Pris et édité à partir de: Thomas Shafee [CC par 4.0 (https: // CreativeCommons.Org / licences / par / 4.0)]. En notation scientifique, les biochimistes utilisent des lettres grecques avec des indices pour décrire la composition des protomères protéiques. Par exemple, une protéine homotypique tétramérique est désignée comme α4, Tandis qu'une protéine tétramérique formée par deux dimères différents est désignée comme α2β2.
[TOC]
Structure des protéines
Les protéines sont des molécules complexes qui acquièrent différentes configurations à trois dimensions. Ces configurations sont exclusives pour chaque protéine et leur permettent d'exécuter des fonctions très spécifiques. Les niveaux d'organisation structurelle des protéines sont les suivants.
Structure primaire
Il se réfère à la séquence dans laquelle les différents acides aminés de la chaîne polypeptidique sont disposés. Cette séquence est donnée par la séquence d'ADN qui code pour une telle protéine.
Structure secondaire
La plupart des protéines ne sont pas de longues chaînes d'acides aminés complètement étendus, mais ont des régions qui sont régulièrement pliées sous forme d'hélices ou de feuilles. Ce pliage est celui qui est appelé structure secondaire.
Structure tertiaire
Les zones pliées de la structure secondaire peuvent, à leur tour, se plier et s'assembler dans des structures plus compactes. Ce dernier pli est celui qui donne à la protéine sa forme à trois dimensions.
Structure quaternaire
Dans les protéines qui sont formées par plus d'une sous-unité, les structures quaternaires sont les relations spatiales qui existent entre chaque sous-unité, qui sont liées par des liaisons non covalentes.
Peut vous servir: comment les champignons respirent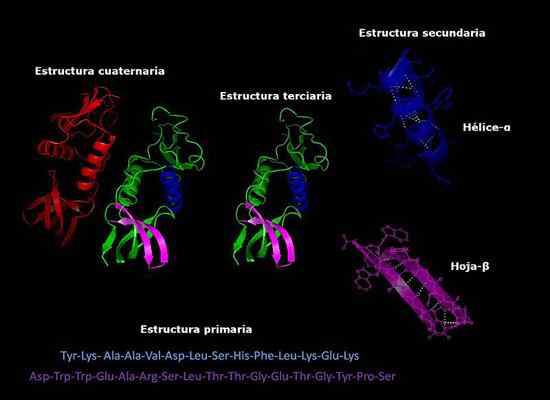 Structures primaires, secondaires, tertiaires et quaternaires des protéines, conformation à trois dimensions. Pris et édité à partir de: Alejandro Porto [CC BY-SA 3.0 (https: // CreativeCommons.Org / licences / by-sa / 3.0)].
Structures primaires, secondaires, tertiaires et quaternaires des protéines, conformation à trois dimensions. Pris et édité à partir de: Alejandro Porto [CC BY-SA 3.0 (https: // CreativeCommons.Org / licences / by-sa / 3.0)]. Stabilité de la structure quaternaire
La structure à trois dimensions des protéines est stabilisée par des interactions faibles ou non covalentes. Bien que ces liens ou interactions soient beaucoup plus faibles que les liaisons covalentes normales, celles-ci sont nombreuses et leur effet cumulatif est puissant. Ensuite, nous verrons certaines des interactions les plus courantes.
Interactions hydrophobes
Certains acides aminés contiennent des chaînes latérales hydrophobes. Lorsque les protéines possèdent ces acides aminés, le pliage de la molécule ordonne ces chaînes latérales dans la protéine et les protège de l'eau. La nature des différentes chaînes latérales les fait contribuer de différentes manières dans l'effet hydrophobe.
Interactions de van der Waals
Ces interactions se produisent lorsque des molécules ou des atomes qui ne sont pas unis par des liaisons covalentes s'approchent trop entre eux, et à cause de cela, leurs orbitales électroniques les plus externes commencent à se chevaucher.
À cette époque, une force de répulsion est établie entre ces atomes qui se développent très rapidement à mesure que leurs centres respectifs se rapprochent. Ce sont les "forces" de van der Waals ".
Interactions de chargement de chargement
C'est l'interaction électrostatique qui se produit entre quelques particules chargées. Dans les protéines, ce type d'interactions se produit, à la fois en raison de la charge électrique nette de la protéine et de la charge individuelle des ions contenus à l'intérieur. Ce type d'interactions est parfois appelé puente salino.
Liaisons hydrogène
Une liaison hydrogène est établie entre un atome d'hydrogène attaché, par des moyens.
Ce type de liaison est très important, car les propriétés de nombreuses molécules, y compris celles de l'eau et des molécules biologiques, sont largement dues à des liaisons hydrogène. Partager les propriétés des liaisons covalentes (les électrons sont partagés) et également d'interactions non covalentes (interaction de chargement de chargement).
Peut vous servir: cultures transitoiresInteractions dipolos
Dans les molécules, y compris les protéines, qui ne présentent pas la charge nette, une disposition non uniforme de leurs charges internes peut être soumise, avec une extrémité légèrement plus négative qu'un autre. C'est ce que l'on appelle un dipôle.
Cette condition dipolaire de la molécule peut être permanente, mais elle peut également être induite. Les dipolos peuvent être attirés par des ions ou d'autres dipôles. Si les dipôles sont permanents, l'interaction a une plus grande portée que ce qui est présenté avec des dipôles induits.
En plus de ces interactions non covalentes, certaines protéines oligomères stabilisent leur structure quaternaire au moyen d'un type de liaison covalente, le lien disulfure. Ceux-ci sont établis entre les groupes sulfhydrillo des cystéons de différents protomères.
Les liaisons disulfuro aident également à stabiliser la structure secondaire des protéines, mais dans ce cas, les déchets de cystéine se connectent à l'intérieur du même polypeptide (liaisons disulfure d'intrapopolipeptide).
Interactions entre les protomères
Comme indiqué précédemment, dans les protéines composées de plusieurs sous-unités ou protomères, ces sous-unités peuvent être similaires (homotypiques) ou différentes (hétérotypiques).
Interactions homotypiques
Les sous-unités qui composent une protéine sont des chaînes de polypeptides asymétriques. Cependant, dans les interactions homotypiques, ces sous-unités peuvent être associées de différentes manières en réalisant divers types de symétrie.
Les groupes qui interagissent avec chaque protomère sont généralement situés dans différentes positions, ils sont donc appelés interactions hétérologues. Les interactions hétérologues entre les différentes sous-unités se produisent parfois de telle manière que chaque sous-unité est tordu par rapport au précédent, une structure hélicoïdale et une structure hélicoïdale peuvent être obtenues.
À d'autres occasions, les interactions sont données de manière à ce que des groupes de sous-unités définis soient disposés autour d'un ou plusieurs axes de symétrie, dans ce qui est connu sous le nom de symétrie ponctuelle - groupe. Lorsqu'il y a plusieurs axes de symétrie, chaque sous-unité brisée par rapport à son voisin à 360 ° / n (où N représente le nombre d'axes).
Il peut vous servir: flore et faune australienne: espèces représentativesParmi les types de symétrie obtenus de cette manière figurent par exemple, hélicoïdal, cubique et icosaédrique.
Lorsque deux sous-unités interagissent à travers un axe binaire, chaque unité s'est cassée à 180 ° par rapport à l'autre, autour de cet axe. Cette symétrie est connue sous le nom de symétrie C2. Dans ce document, les sites d'interaction dans chaque sous-unité sont identiques; Dans ce cas, on ne parle pas d'interaction hétérologue, mais d'une interaction isologue.
Si, au contraire, l'association entre les deux composantes du dimère est hétérologue, alors un dimère asymétrique sera obtenu.
Interactions hétérotypiques
Pas toujours les sous-unités qui interagissent dans une protéine sont de la même nature. Il y a des protéines formées par douze sous-unités différentes ou plus.
Les interactions qui maintiennent la stabilité de la protéine sont les mêmes que dans les interactions homotypiques, mais des molécules complètement asymétriques sont généralement obtenues.
L'hémoglobine, par exemple, est un testeur qui présente deux paires de sous-unités différentes (α2β2).
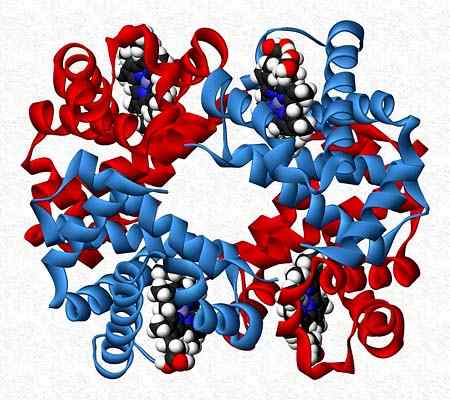 Structure quaternaire de l'hémoglobine. Pris et édité à partir de: Benjah-bmm27. Modifié par Alejandro Porto. [CC0].
Structure quaternaire de l'hémoglobine. Pris et édité à partir de: Benjah-bmm27. Modifié par Alejandro Porto. [CC0]. Les références
- C.K. Mathews, k.ET. Van Hold & K.g. Ahern (2002). Biochimerie. 3e édition. Benjamin / Cummings Publishing Company, Inc.
- R.K. Murray, P. Mayes, D.C. Granner & V.W. Rodwell (1996). Biochemery de Harper. Appleton & Lange
- J.M. Berg, J.L. Tymoczko & l. Stryer (2002). Biochimerie. 5e édition. W. H. Freeman et compagnie.
- J. Koolman & k.-H. Roehm (2005). Atlas de la couleur de la biochimie. 2e édition. Thieme.
- POUR. Lehninger (1978). Biochimie. Éditions Omega, S.POUR.
- L. Stryer (1995). Biochimerie. W.H. Freeman and Company, New York.
- « 19e siècle dans la population du Chili, la société, l'économie et la politique
- Caractéristiques, structure, fonctions et utilisations de la vimentine »

