Propriétés à l'échelle microscopique, comptage des particules, exemples
- 1269
- 98
- Noa Da silva
La Échelle microscopique C'est celui qui est utilisé pour mesurer les tailles et les longueurs qui ne peuvent pas être vues à l'œil nu et qui sont en dessous du millimètre de longueur. De plus élevé au plus bas, les échelles microscopiques du système métrique sont:
- Le millimètre (1 mm), qui est le dixième d'un centimètre ou le millième d'un mètre. En cela, c'est l'échelle que nous avons l'une des plus grandes cellules du corps, qui est l'ovule, dont la taille est de 1,5 mm.
 Figure 1. Les globules rouges sont des cellules à l'échelle microscopique. Source: Pixabay
Figure 1. Les globules rouges sont des cellules à l'échelle microscopique. Source: Pixabay - Le dixième de millimètre (0,1 mm). C'est l'échelle de l'épaisseur ou du diamètre des cheveux humains.
- Le micromètre ou le micra (1 μm = 0,001 mm). Sur cette échelle se trouvent les cellules végétales et animales et les bactéries.
Les cellules végétales sont de l'ordre de 100 μm. Les cellules animales sont dix fois mineures, elle est de l'ordre de 10 μm; Tandis que les bactéries sont 10 fois moins que les cellules animales et sont de l'ordre de 1 μm.
[TOC]
Échelle nanométrique
Il existe encore des mesures plus petites que l'échelle microscopique, mais qui ne sont généralement pas utilisées sauf dans certains contextes spéciaux. Ensuite, nous verrons certaines des mesures nanométriques les plus importantes:
- Le nanomètre (1 ηm = 0,001 μm = 0,000001 mm) est le millionième d'un millimètre. Sur cette échelle se trouvent certains virus et molécules. Les virus sont de l'ordre du 10ηm et des molécules de l'ordre de 1ηm.
- L'angstrom (1å = 0,1ηm = 0,0001 μm = 10-7mm). Cette mesure forme l'échelle ou la taille atomique.
- Le fantomomètre (1fm = 0,00001å = 0,000001ηm = 10-12mm). Il s'agit de l'échelle des noyaux atomiques, qui sont comprises entre 10 mille et 100 mille fois plus petits que l'atome. Cependant, malgré sa petite taille, le noyau concentre 99,99% de la masse atomique.
- Il y a des échelles plus petites au noyau atomique, car celles-ci sont composées de particules telles que des protons et des neutrons. Mais il y en a plus: ces particules sont à leur tour constituées par des particules plus fondamentales telles que les quarks.
Instruments pour l'observation microscopique
Lorsque les objets sont entre le millimètre et l'échelle micrométrique (1 mm - 0,001 mm), ils peuvent être observés avec un microscope optique.
Cependant, si les objets ou les structures se trouvent entre les nanomètres et les microscopes électroniques ou nanoscope seront nécessaires.
En microscopie électronique au lieu de lumière, des électrons à haute énergie sont utilisés qui ont une longueur d'onde beaucoup plus faible que la lumière. L'inconvénient du microscope électronique est qu'il n'est pas possible.
Peut vous servir: choc magnétique: unités, formules, calcul, exemplesD'un autre côté, la lumière laser est utilisée dans le nanoscope, et il a l'avantage sur la microscopie électronique que les structures et les molécules peuvent être regardées et enregistrées à l'intérieur d'une cellule vivante.
La nanotechnologie est la technologie avec laquelle les circuits, les structures, les pièces et même les moteurs sont fabriqués sur les échelles allant du nanomètre à l'échelle atomique.
Propriétés microscopiques
En physique, dans une première approche, le comportement de la matière et les systèmes sont étudiés du point de vue macroscopique. De ce paradigme, la question est un continuum infiniment divisible; Et ce point de vue est valable et adéquat pour de nombreuses situations de la vie quotidienne.
Cependant, certains phénomènes du monde macroscopique n'ont expliqué que si les propriétés microscopiques de la question sont prises en compte.
Dans le point de vue microscopique, la structure moléculaire et atomique de la matière est prise en compte. Contrairement à l'approche macroscopique, à cette échelle, il existe une structure granulaire avec des trous et des espaces entre les molécules, les atomes et même à l'intérieur.
L'autre caractéristique du point de vue microscopique en physique, c'est qu'une matière, quelle que soit la petite taille, est composée d'un grand nombre de particules séparées les unes des autres et en mouvement continu.
-La matière est un immense vide
Dans une petite tarte.
C'est-à-dire qu'un élément de matière sur l'échelle microscopique est un énorme vide avec des concentrations d'atomes et de noyaux qui occupent une très petite fraction du volume total total. En ce sens, l'échelle microscopique a une similitude avec l'échelle astronomique.
Des objets macroscopiques à la découverte de l'atome
Les premiers produits chimiques, qui étaient les alchimistes, ont réalisé que les matériaux pouvaient être de deux types: pur ou composés. Cela a atteint l'idée des éléments chimiques.
Il peut vous servir: gradient de pression: qu'est-ce que c'est et comment il est calculéLes premiers éléments chimiques ont été découverts étaient les sept métaux de l'antiquité: l'argent, l'or, le fer, le plomb, l'étain, le cuivre et le mercure. Au fil du temps, ils ont été découverts dans la mesure où des substances ont été trouvées qui ne pouvaient pas se décomposer dans d'autres.
Ensuite, les éléments ont été classés en fonction de leurs propriétés et caractéristiques dans les métaux et les non-métaux. Tous ceux qui avaient des propriétés chimiques similaires et une affinité.
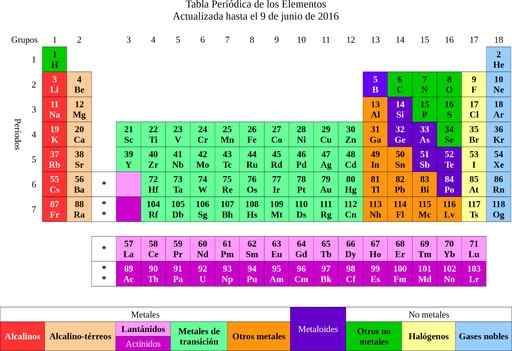 Figure 2. Tableau des éléments périodiques. Source: Wikimedia Commons.
Figure 2. Tableau des éléments périodiques. Source: Wikimedia Commons. Des éléments qu'il est allé à l'idée des atomes, un mot qui signifie indivisible. Peu de temps après, les scientifiques ont remarqué que les atomes avaient une structure. De plus, les atomes avaient deux types de charge électrique (positif et négatif).
Particules subatomiques
Dans les expériences de Rutherford dans lesquelles il a bombardé les atomes d'une fine plaque d'or avec des particules alpha, la structure de l'atome a été révélée: un petit noyau positif entouré d'électrons.
Ils ont continué à bombarder les atomes de plus en plus de particules d'énergie et à faire, afin de démêler les secrets et les propriétés du monde microscopique de plus en plus à plus petite échelle.
De cette façon, le modèle standard a été atteint, ce qui établit que les vraies particules élémentaires sont celles dont les atomes sont composés. À son tour, les atomes donnent naissance aux éléments, ceux-ci aux composés et toutes les interactions connues (sauf la gravitation). Au total, il y a 12 particules.
Ces particules fondamentales ont également leur tableau périodique. Il y a deux groupes: les particules fermioniques de spin ½ et le bosonique. Bosonic est responsable des interactions. Les fermioniques sont 12 et sont celles qui donnent naissance à des protons, des neutrons et des atomes.
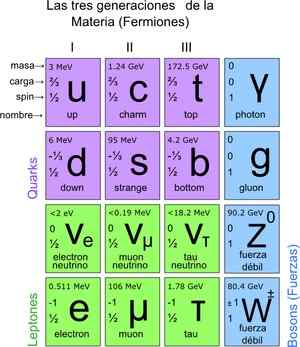 figure 3. Particules fondamentales. Source: Wikimedia Commons.
figure 3. Particules fondamentales. Source: Wikimedia Commons. Comment compter les particules à l'échelle microscopique?
Au fil du temps, les chimistes découvraient les masses relatives des éléments à partir de mesures précises dans les réactions chimiques. Par exemple, il pourrait être déterminé que le carbone est 12 fois plus lourd que l'hydrogène.
Il a également été déterminé que l'hydrogène est l'élément le plus léger, de sorte que cet élément s'est vu attribuer la masse relative 1.
D'un autre côté, les produits chimiques nécessaires pour connaître le nombre de particules impliquées dans une réaction, de sorte qu'aucun réactif ne manque. Par exemple, une molécule d'eau nécessite deux atomes d'hydrogène et un oxygène.
Peut vous servir: phénomènes ondulésDe ce contexte, le concept de mol est né. Une mole de toute substance est une quantité fixe de particules équivalentes à sa masse moléculaire ou atomique en grammes. Ainsi, il a été déterminé que 12 grammes de carbone ont le même nombre de particules que 1 gramme d'hydrogène. Ce nombre est connu comme le numéro Avogadro: 6,02 x 10 ^ 23 particules.
-Exemple 1
Calculez combien d'atomes d'or sont en 1 gramme d'or.
Solution
On sait que l'or a un poids atomique de 197. Ces données peuvent être trouvées dans le tableau périodique et indique qu'un atome d'or est 197 fois plus lourd que celui de l'hydrogène et 197/12 = 16 416 fois plus lourd que le carbone.
Une mol d'or a 6,02 × 10 ^ 23 atomes et a le poids atomique exprimé en grammes, c'est-à-dire 197 grammes.
Dans un gramme d'or, il y a 1/197 moles d'or, qui est 6,02 × 10 ^ 23átomos / 197 = 3,06 x10 ^ 23 atomes d'or.
-Exemple 2
Déterminez le nombre de molécules de carbonate de calcium (CACO3) qu'il y a dans 150 grammes de cette substance. Dites également combien d'atomes de calcium, combien de carbone et combien d'oxygène il y a dans ce composé.
Solution
La première chose est de déterminer la masse moléculaire du carbonate de calcium. Le tableau périodique indique que le calcium a un poids moléculaire de 40 g / mol, carbone 12 g / mol et oxygène 16 g / mol.
Puis la masse moléculaire de (caco3) être :
40 g / mol + 12 g / mol + 3 x 16 g / mol = 100 g / mol
Tous les 100 grammes de carbonate de calcium sont 1 mol. Puis en 150 grammes correspondent à 1,5 moles.
Chaque mol de carbonate a 6,02 x 10 ^ 23 molécules de carbonate, donc en 1,5 moles de carbonate, il y a 9,03 x 10 ^ 23 molécules.
Résumant, dans 150 grammes de carbonate de calcium, il y a:
- 9.03 x 10 ^ 23 molécules de carbonate de calcium.
- Atomes de calcium: 9,03 x 10 ^ 23 .
- Aussi 9,03 x 10 ^ 23 atomes de carbone
- Enfin, 3 x 9,03 x 10 ^ 23 atomes d'oxygène = 27,09 x 10 ^ 23 Atomes d'oxygène.
Les références
- Biologie appliquée. Quelles sont les mesures microscopiques?. Récupéré de: youtube.com
- Éducation chimique. Représentations macroscopiques, submicroscopiques et symboliques sur la matière. Récupéré de: SCIELO.org.mx.
- Garcia A. Cours de physique interactive. Macro-State, microstats. Température, entropie. Récupéré de: SC.Ehu.est
- La structure microscopique de la matière. Récupéré de: Alipso.com
- Wikipédia. Niveau microscopique. Récupéré de: Wikipedia.com

