Epmers
- 2589
- 594
- Prof Noah Collet
 Structure d'un épimer. Source: Gabriel Bolívar
Structure d'un épimer. Source: Gabriel Bolívar Quels sont les épigafts?
Les Epmers Ce sont des diaisomères dans lesquels un seul de ses centres aquiraux diffère de la configuration spatiale, contrairement aux éantiomères, où tous les centres aquiraux ont des configurations différentes, et représentent quelques images spéculaires qui ne peuvent pas chevaucher l'une sur l'autre.
Le reste des diasteroisomères (isomères géométriques, par exemple), peut avoir plus de deux centres avec des configurations différentes. Par conséquent, un grand pourcentage de stéréoisomères sont des diasomères.
Les EPMères se produisent fréquemment en glucides: par exemple, la glycose D et le D-manosa diffèrent en C2, qui est le premier atome de carbone chiral.
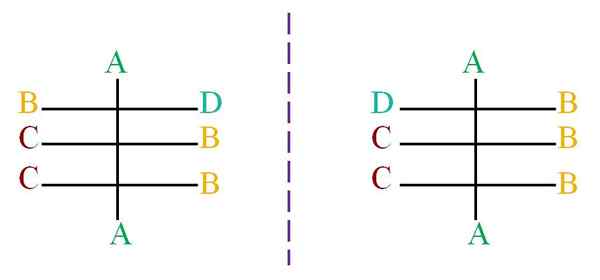
Supposons une structure avec un squelette d'atomes noirs liés aux lettres A, B, C et D (image supérieure).
La ligne pointillée représente le miroir, démontrant que le couple des molécules ci-dessus ne sont pas des éantiomères, car tous ses centres chiraux ont la même configuration, à l'exception du premier centre, lié aux lettres B et D.
La molécule à gauche a la lettre D regardant vers le côté droit, tandis que la lettre D de la molécule droite, regarde vers le côté gauche. Pour savoir ce que la configuration de chacun doit être utilisée au système (R-S) de Cahn-Ingold-Prelog.
Caractéristiques des épigmers
- La principale caractéristique des épigmers ne se trouve que dans un centre aquiral (ou stéréogénique).
La modification de l'orientation spatiale de D et B peut provoquer des conformères plus stables ou instables, c'est-à-dire que les rotations des liens simples provoquent deux atomes ou groupes d'atomes volumineux ou s'éloigner.
Ainsi, un épimer peut être beaucoup plus stable que l'autre. Celui qui fait pivoter ses liens génère des structures plus stables, sera l'épimerus avec la plus grande tendance à se former dans un équilibre.
Peut vous servir: système inhomogèneRevenant aux lettres, D et B peuvent être très encombrants, tandis que C est un petit atome. Ainsi, être l'épimer de la droite est plus stable, car D et C trouvé à gauche des deux premiers centres souffrent d'un obstacle moins stérique.
- Microscopiquement, cela devient une caractéristique pour la paire d'épithéliles considérés.
- Macroscopiquement, les différences sont accentuées et finissent, par exemple, des points de fusion, des indices de réfraction, différents spectres RMN (en plus de nombreuses autres propriétés).
- Dans le domaine de la biologie et des réactions catalysées par les enzymes, c'est là que les épithémères diffèrent encore plus. L'un pourrait être métabolisé par le corps, tandis que l'autre ne.
Entraînement
Les EPMers sont formés par une réaction chimique appelée épimérisation. Si les deux épitakers ne diffèrent pas dans un large degré de stabilité, un équilibre d'épimérisation est établi, ce qui n'est rien de plus qu'une interconversion:
EPB EPA
Où l'EPA est épimer A, et epb l'épimer. Si l'un d'eux est beaucoup plus stable que l'autre, il aura une concentration plus grande et provoquera ce que l'on appelle la mutarrotation. En d'autres termes, il pourra modifier la direction d'un faisceau de lumière polarisée.
L'épimérisation peut ne pas être un équilibre et, par conséquent, être irréversible. Dans ces cas, un mélange de diastéoisomères EPA / EPA est obtenu.
La route synthétique des épitars varie en fonction des réactifs impliqués, des moyens de réaction et des variables de processus (utilisation des catalyseurs, pression, température, etc.).
Pour cette raison, la formation de chaque paire d'épitars doit être étudiée individuellement à partir d'autres, chacune avec ses propres mécanismes et systèmes chimiques.
Il peut vous servir: réduction de l'agent: concept, les plus forts, des exemplesTautomérisation
Parmi tous les processus de formation d'épithémer, la tautomérisation de deux jours à deux jours peut être considérée comme un exemple général.
Cela consiste en un équilibre où la molécule adopte une forme cétone (c = o) ou l'écluse (c-oh). Une fois la forme cétonique convertie, la configuration du carbone adjacente au groupe carbonyle (si elle est chirale) change, générant quelques épithémères.
Un exemple de la susmention est le couple cis-décalone et trans-décalone.
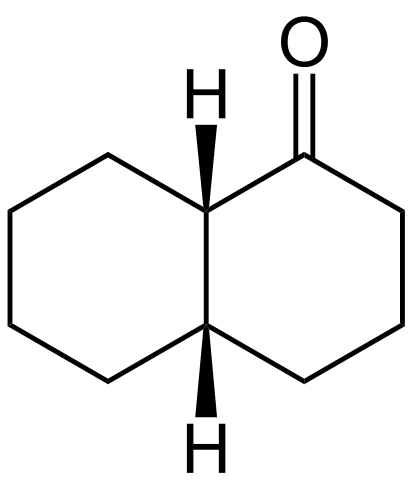 Structure cis-decalona. Source: Wikimedia Commons
Structure cis-decalona. Source: Wikimedia Commons La structure du cis-decalona est indiquée ci-dessus. Les atomes H sont situés en haut des deux anneaux, tandis que dans le trans-décalone, l'un est au-dessus des anneaux, et l'autre est en dessous.
Le carbone à gauche du groupe C = O est le centre quiral, et, par conséquent, celui qui différencie les épitches.
Exemples
Anomères du glucose
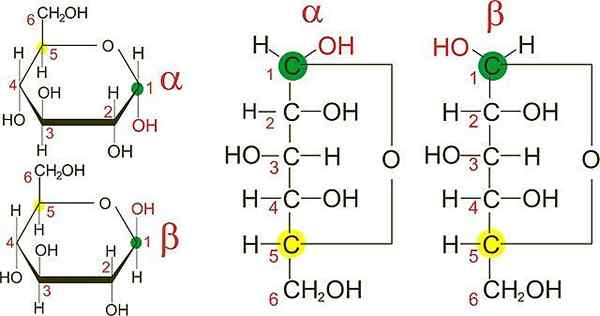 Anomères D-glucose. Source: Wikimedia Commons
Anomères D-glucose. Source: Wikimedia Commons Dans l'image supérieure, vous avez les anneaux furanieux des deux anomères D-glycose: α et β. D'après les anneaux, on peut voir que les groupes OH dans le carbone 1 se trouvent soit dans la même direction de l'OH adjacent, dans l'anomère α, soit dans des directions opposées, comme dans l'anomère β.
Les projections Fisher des deux anomères (à droite de l'image) rendent la différence entre les deux épithémères encore plus claire, qui sont, à leur tour, des anomères.
Cependant, deux anomères α peuvent avoir des configurations spatiales différentes dans l'un des autres carbones, et par conséquent, des épithémeurs.
Dans le C-1 de la projection de Fisher pour l'anomère α, le groupe OH "regarde" à droite, tandis que dans l'anomère β "look" β.
Peut vous servir: Faraday constanteIsomères de mentol
 Stéréoisomères de mentol. Source: Wikimedia Commons
Stéréoisomères de mentol. Source: Wikimedia Commons Dans l'image, vous avez tous les stéréoisomères de la molécule de mentol. Chaque colonne représente une paire d'énantiomères (observer soigneusement), tandis que les rangs correspondent aux diastéréoisomères.
Ainsi, les épitars doivent être celles qui ne différencient à peine rien de plus que dans la position spatiale d'un carbone.
Le (+) - le mentol et le (-) - le néoisomentol sont Epithes, ainsi.
S'il est observé en détail, dans les deux groupes -OH et -CH3 Ils quittent l'avion (au-dessus de l'anneau), mais dans le (-) - Neoisomentol, le groupe isopropile souligne également de l'avion.
Non seulement le (+) - le mentol est l'épimer de (-) - néoisomentol, mais aussi (+) - neomentol. Ce dernier ne diffère que le groupe -ch3 pointe dans l'avion. D'autres Epithes sont:
- (-) - isomentol et (-) - Neomentol
- (+) - isomentol et (+) - Neomentol
- (+) - Neoisomentol et (-) - Neomentol
- (+) - Neomentol et (-) - Neoisomentol
Ces stéréoisomères représentent un exemple pratique pour clarifier le concept des épithémères, et on peut voir que, de plusieurs diastéréoisomères, beaucoup ne peuvent être différenciés que dans un seul carbone asymétrique ou chiral.
Les références
- Carey F. (2008). Chimie organique. Mc Graw Hill.
- Epmers. Récupéré des salles de classe.Uruguayeduca.Édu.Oh

