Caractéristiques des enzymes caractéristiques, mécanismes d'action, exemples
- 1751
- 344
- Prof Ines Gaillard
Ongle Enzyme alostérique (Depuis le grec: allo, différents + stéréos, espace à trois dimensions) est une protéine dans laquelle des interactions indirectes sont produites entre des sites topographiquement différents, par l'union des substrats et des molécules régulatrices (ligands).
L'union d'un ligand à un site spécifique est influencée par l'union d'un autre ligand effecteur (ou modulation du ligand) à un autre site différent (alostérique) de l'enzyme. Ceci est connu sous le nom d'interactions allesthériques ou d'interactions coopératives.
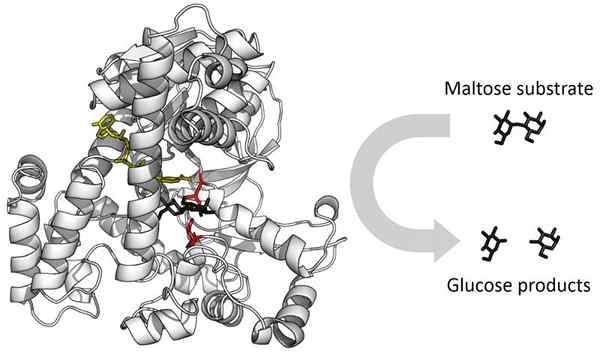
 Exemple d'enzyme. Source: Thomas Shafee [CC BY-SA 4.0 (https: // CreativeCommons.Org / licences / by-sa / 4.0)]
Exemple d'enzyme. Source: Thomas Shafee [CC BY-SA 4.0 (https: // CreativeCommons.Org / licences / by-sa / 4.0)] Lorsque le ligand effecteur augmente l'affinité de l'union d'un autre ligand à l'enzyme, la coopérative est positive. Lorsque l'affinité diminue la coopération est négative. Si deux ligands égaux participent à l'interaction coopérative, l'effet est homotrope, et si les deux ligands sont différents, l'effet est hétérotrope.
L'interaction coopérative produit des changements réversibles dans la structure moléculaire de l'enzyme, au niveau de la structure tertiaire et quaternaire. Ces changements sont connus sous le nom de changements conformationnels.
[TOC]
Histoire
Le concept d'interaction Alestric a émergé il y a plus de 50 ans. Il a évolué au fil du temps, à savoir:
-En 1903, la courbe sigmoïdale de l'hémoglobine d'oxygène a été observée.
-En 1910, la courbe sigmoïdale de l'union de o2 L'hémoglobine a été décrite mathématiquement par l'équation de Hill.
-En 1954, Novick et Szilard ont montré qu'une enzyme située au début d'une voie métabolique était inhibée par le produit final de cette route, qui est connue sous le nom de rétroaction négative.
-En 1956, Umbarger a découvert que le chagrin L-Treonine, la première enzyme de la biosynthèse de la L-isoléucine, a été inhibé par la L-isoleucine, et qu'il ne présentait pas une cinétique typique de Michaelis -Elté avec une courbe hyperbolique, mais qui avait eu une courbe sigmoïde.
-En 1963, Perutz et al., Ils ont découvert par les changements de change conformationnels à la structure de l'hémoglobine lors de la liaison à l'oxygène. Monod et Jacob ont renommé les sites de réglementation comme des "sites aériens".
-En 1965, Monod, Wyman et Changeux proposent le modèle symétrique, ou modèle MWC (lettres initiales de Monod, Wyman et Changeux) pour expliquer les interactions alesthériques.
-En 1966, Koshland, Nemethy et Filmer proposent le modèle de couplage séquentiel ou induit, ou modèle KNF, pour expliquer les interactions alesthériques.
-En 1988, la structure X-Ray du Transcarbamilasa Aspartate a démontré le modèle symétrique postulé par Monod, Wyman et Changeux.
-Dans les années 1990, les mutations, les modifications covalentes et les changements de pH ont été considérés comme des effecteurs alostériques.
-En 1996, la structure des rayons x LAC transitions démontrées vers la theotérique.
Mécanismes d'action et exemples
-Caractéristiques des modèles MWC et KNF de la régulation alostérique
Modèle MWC
L'hypothèse du modèle MWC original a proposé ce qui suit (Monod, Wyman, Changeux, 1965)
Peut vous servir: flore et faune des entrées: espèces représentativesLes protéines alostérales sont des oligomères constitués par des protomères liés symétriquement. Les protomères sont constitués de sous-unités ou de chaînes de polypeptides.
Les oligomères ont au moins deux états de conformation (R et T). Les deux États (de la structure quaternaire) établissent spontanément un équilibre, avec ou sans lien.
Lorsque la transition d'un état à une autre se produit, la symétrie est préservée et l'affinité d'un site (ou de plusieurs) site spécifié vers un ligand est modifié.
De cette façon, la Ligandos Cooperative Union continue à partir de l'interaction coopérative entre les sous-unités.
Modèle KNF
L'hypothèse du modèle KNF a proposé ce qui suit (Koshland, Nemethy, Filmer, 1966): Le syndicat de liaison produit un changement dans la structure tertiaire dans une sous-unité. Ce changement de conformation affecte les sous-unités voisines.
L'affinité de liaison au ligand protéique dépend du nombre de ligands qui se maintient ensemble. Par conséquent, les protéines theotériques ont plusieurs états conformationnels qui incluent des états intermédiaires.
Au cours des cinq dernières décennies, les modèles MWC et KNF ont été évalués par des études biochimiques et structurelles. Il a été démontré que de nombreuses protéines alhéstriques, y compris des enzymes, se conforment à ce qui est proposé dans le modèle MWC, bien qu'il y ait des exceptions.
Le modèle MWC et les enzymes allesthériques (ou enzymes régulatrices)
Les enzymes alostériques sont souvent plus grandes et plus complexes que les enzymes non aléshériques. L'aspartate transcarbamilase (Aspcarbamilasa ou Atcasa) et le phosphofductiona-1 (PFK-1) sont des exemples classiques d'enzymes alesthériques qui répondent au modèle MWC.
Atcasa de ET. coli
L'ATCASA catalyse la première réaction de la biosynthèse des nucléotides pyrimidine (CTP et UTP) et utilise ASP comme substrat. La structure de l'ATCASA se compose de sous-unités catalytiques et réglementaires. Atcasa a deux états conformationnels r et t. La symétrie entre ces deux états est préservée.
La cinétique d'Atcasa (la vitesse initiale des ATCA. Cela indique qu'Atcasa a un comportement coopératif.
Atcasa est inhibé par la rétroaction CTP. La courbe sigmoïde d'Atcasa, en présence de CTP, est à droite de la courbe sigmoïde d'ATCA. Une augmentation de la valeur de la constante de Michaelis-mouchante (Km).
C'est-à-dire en présence de CTP, ATCAVMax), Par rapport à Atcasa en l'absence de CTP.
Il peut vous servir: granulopoyèse: caractéristiques, hématologie, phases et facteursEn conclusion, le CTP est un effecteur négatif hétérotrope parce que l'affinité de l'ATCASA par l'aspartate diminue. Ce comportement est connu sous le nom de coopérativité négative.
PFK-1
Le PFK-1 catalyse la troisième réaction de la voie de glycolyse. Cette réaction consiste en le transfert d'un groupe phosphate de l'ATP au 6-phosphate fructose. La structure du PFK-1 est un tétramètre, qui présente deux états conformationnels r et t. La symétrie entre ces deux états est préservée.
La cinétique du PFK-1 (la vitesse initiale avec différentes concentrations de 6-phosphate fructose) présente une courbe sigmoïde. Le PFK-1STá soumis à une régulation alostrique complexe par l'ATP, l'AMP et le frutosa-2,6-biphosphate, à savoir:
La courbe sigmoïde du PFK-1, en présence d'une concentration élevée d'ATP, est à droite de la courbe sigmoïde à une faible concentration d'ATP (figure 4). Une augmentation de la valeur de la constante de Michaelis-mouchante (Km).
En présence d'une concentration d'ATP élevée, PFK-1 nécessite une concentration de fructose à 6 phosphate de 6 pour atteindre la moitié de la vitesse maximale (VMax).
En conclusion, l'ATP, en plus d'être un substrat, est un alostroérique hétérotrope négatif.
La courbe sigmoïde du PFK-1, en présence d'ampli, est située à gauche de la courbe sigmoïde du PFK-1 en présence d'ATP. C'est-à-dire que l'ampli élimine l'effet inhibiteur de l'ATP.
En présence d'AMP, PFK-1 nécessite une concentration de fructose à 6 phosphate de 6VMax). Ceci se manifeste dans le fait qu'il y a une diminution de la valeur de la constante de Michaelis -Mente (Km).
En conclusion, l'ampli est un alostroariste hétérotrope positif car l'affinité de l'union PFK-1 augmente par le 6-phosphate fructose. Frutosa-2,6-Biphosphate (F2.6bp) est un puissant activateur alostrique du PFK-1 (figure 5), et son comportement est similaire à celui de l'ampli.
Le modèle MWC est commun, mais pas universel
Sur les structures protéiques totales déposées dans PDB (Banque de données protéiques), la moitié sont des oligomères et l'autre moitié sont des monomères. Il a été démontré que la coopérativité n'a pas besoin de plusieurs ligands, ni de plusieurs sous-unités. C'est le cas de la glycoquinase et d'autres enzymes.
La glucoquinase est monomère, a une chaîne de polypeptides et présente une cinétique sigmoïdale en réponse à l'augmentation de la concentration de glycémie (Porter et Miller, 2012; Kamata et al., 2004).
Peut vous servir: parasitisme: concept, types et exemplesIl existe différents modèles qui expliquent la cinétique coopérative dans les enzymes monomères, à savoir: modèle mnémonique, modèle de transition lent induit par lent, ajout randomisé de substrats dans les réactions biomoléculaires, types de changements de conformation lents, entre autres, entre autres.
Des études de structure de la glycoquinase ont soutenu le modèle mnémonique
La glycocinase humaine normale a un Km 8 mm pour le glucose. Cette valeur est proche de la concentration de glycémie.
Il y a des patients souffrant d'hyperinsulinémie pessista de l'enfance (acronyme en anglais, phhi). La glycokinase de ces patients a un Km Pour le glucose avec une valeur inférieure que les glycocines normales, et la coopérative est importante.
Par conséquent, ces patients ont une variante de glycokinase hyperactive, qui dans les cas graves peut être mortel.
Applications d'alostératisme
Alostería et la catalyse sont intimement liés. En raison de cela, les effets alhésiques peuvent affecter les caractéristiques de la catalyse telles que la liaison du ligand, ligand libération.
Les sites de l'union alostérique peuvent être des cibles de nouveaux médicaments. Cela est dû au fait que l'effecteur alcal peut influencer la fonction de l'enzyme. L'identification des sites alostériques est la première étape de la découverte de médicaments qui améliorent la fonction des enzymes.
Les références
- Changeux, J.P. 2012. Allostery et le modèle Monod-Wyman-Changeux après 50 ans. Revue annuelle de la biophysique et de la structure biomoléculaire, 41: 103-133.
- Changeux, J.P. 2013. 50 ans d'interactions allostériques: les rebondissements des modèles. Biologie des cellules moléculaires, dans Nature Reviews, 14: 1-11.
- Goodey, n.M. et Benkovic, s.J. 2008. La régulation allostérique et la catalyse émergent par voie commune. Nature Chemical Biology, 4: 274-482.
- Kamata, k., Mitsuya, m., Nishimura, t., Eiki, Jun-Hichi, Nagata et. 2004. Base structurelle pour la régulation allostérique de l'enzyme allostérique monomère glucokinase humaine. Structure, 12: 429-438.
- Koshland, D.ET. JR., Néméthy, g., Filmer, D. 1966. Comparaison des données de liaison expérimentales et des modèles théoriques dans les protéines CONTOUNS. Biochimie, 5: 365-385.
- Monod, J., Wyman, J., Changeux, J.P. 1965. Sur la nature des transitions allostériques: au modèle plausible. Journal of Molecular Biology, 12: 88-118.
- Nelson, D.L. et Cox, m.M., 2008. Lehninger-primeciples de biochimie. W.H. Freeman and Company, New York.
- Porter, C.M. et Miller, B.g. 2012. Coopérativité dans les enzymes monomères avec des sites de liaison au ligand unique. Chimie bioorganique, 43: 44-50.
- Voet, D. Et Voet, J. 2004. Biochimie. John Wiley and Sons, USA.
- « Fonction bijective Qu'est-ce que, comment se fait-il, des exemples, des exercices
- Théories de l'évolution biologique, processus, tests et exemples »

