Caractéristiques des électrodes de référence, fonction, exemples
- 2408
- 155
- Prof Ines Gaillard
Il électrode de référence Il s'agit d'un appareil qui est utilisé dans une analyse potentiométrique et voltamétrique pour la détermination quantitative d'un analyte. Son importance est, comme son nom l'indique, à servir de référence pour estimer la véritable valeur du potentiel dans la réaction d'un semi-elk électrochimique.
Les potentiels d'un semi-média dépendent de la concentration d'un ion dans l'intérêt, car il réagit en gagnant ou en perdant des électrons. De cette façon, il est possible de déterminer leur concentration à travers ces potentiels. Cependant, leurs valeurs ne sont pas absolues mais liées à l'électrode hydrogène standard (elle en anglais).
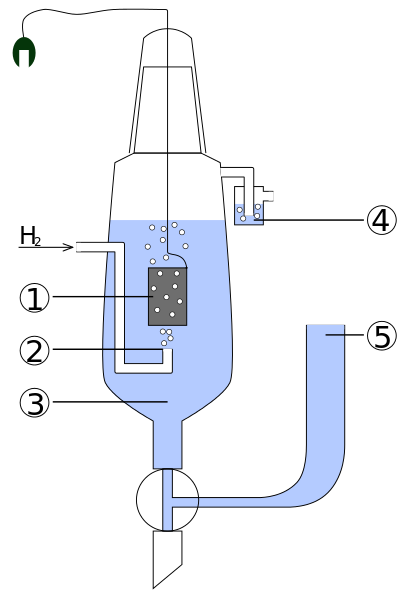
 Diagramme des parties d'un électro d'hydrogène standard. Source: standard_hydrogen_electrode.JPG: KaverinderveriveVative Work: Henry Muelpfordt / CC By-S (http: // CreativeCommons.Org / licences / by-sa / 3.0 /)
Diagramme des parties d'un électro d'hydrogène standard. Source: standard_hydrogen_electrode.JPG: KaverinderveriveVative Work: Henry Muelpfordt / CC By-S (http: // CreativeCommons.Org / licences / by-sa / 3.0 /) Par convention, les potentiels d'électrodes hydrogène sont égaux à 0V. Le problème est que ces électrodes sont difficiles à manipuler, elles ne sont donc pas pratiques de les installer dans toutes les analyses. C'est là que les électrodes de référence entrent, beaucoup plus simples, et dont le potentiel est différent de 0v.
Certaines des électrodes de référence, telles que l'électrode saturée de Calomel (ESC), peuvent être construites dans le même laboratoire avant que l'analyse ne soit effectuée. De même, ils sont obtenus ouvertement sur le marché avec leurs spécifications appropriées, et les risques de contaminer l'échantillon de l'analyte sont minimes.
[TOC]
Caractéristiques des électrodes de référence
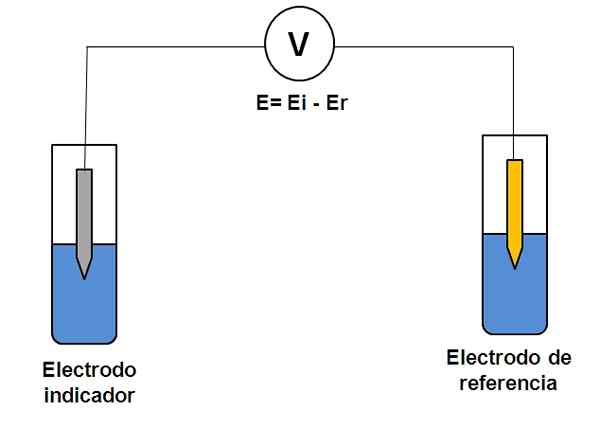 Représentation simple d'un système d'électrodes en potentiométrie. Source: Gabriel Bolívar.
Représentation simple d'un système d'électrodes en potentiométrie. Source: Gabriel Bolívar. Considérez le système des deux électrodes ci-dessus. L'un est l'indicateur (gris), où la réaction d'intérêt a lieu, et l'autre est la référence (or). Cette cellule d'électrochimie aura un potentiel et, qui sera égal à la différence des potentiels des deux électrodes (EI-E). Par conséquent, toute variation de E doit être due au potentiel de l'électrode indicatrice.
Peut vous servir: cyanure de potassium (KCN): propriétés, utilisations, structures, risques,À partir de ce qui précède, il est conclu que l'électrode de référence a les caractéristiques suivantes:
-Il a un potentiel stable pendant le temps et est reproductible. C'est-à-dire ce devrait être le même, quel que soit l'endroit ou combien de fois les mesures sont effectuées.
-Sa composition chimique est constante et insensible, donc elle subit à peine des changements lorsqu'elle interagit avec la solution de l'analyte ou s'immerge dans un milieu aqueux.
-Il est facile à construire et à monter, contrairement à l'électrode hydrogène standard, qui exige l'utilisation d'un réservoir d'hydrogène et coule des risques d'explosion lorsque l'hydrogène se mélange avec l'air avec l'air.
L'électrode indicatrice est sensible à la concentration de l'analyte.
Fonction d'électrode de référence
Les potentiels d'électrodes de référence sont mesurés par rapport à l'électrode hydrogène standard, donc leurs valeurs sont différentes de 0V. Grâce à ces électrodes d'hydrogène, la construction des tables de potentiel standard standard et º est possible, qui apparaissent dans les textes de chimie pour les réactions redox symphines.
Cependant, en pratique, il ne charge pas d'électrode d'hydrogène partout. Au lieu de cela, des électrodes de référence sont utilisées, beaucoup plus simples et en toute sécurité pour manipuler.
Comme ses potentiels sont constants et stables, les lectures potentielles de la cellule électrochimique sont exclusivement dues à l'électrode indicatrice; c'est-à-dire aux variations de concentration de l'analyte en question.
Ainsi, la fonction d'électrode de référence consiste à déterminer le potentiel de toute réaction dans l'un des semi-limits du système électrochimique. Si leurs potentiels n'étaient pas stables, alors les déterminations quantitatives de l'analyte ne seraient pas fiables. Toute analyse potentiométrique ou voltamétrique doit spécifier quelle électrode de référence qu'ils ont utilisée pour signaler leurs résultats.
Il peut vous servir: acide courageux (HBRO2): propriétés physiques et chimiques et utilisationsExemples d'électrodes de référence
Il existe plusieurs électrodes de référence disponibles sur le marché. Certains utilisés pour des déterminations très spécifiques. Cependant, il y a deux électrodes parmi toutes qui se distinguent grâce à leur simplicité et leur praticité: l'électrode calomel et le cllorure d'argent argenté, tous deux très récurrents dans de nombreuses analyses potentiométriques et voltamletriques.
Électrode de calomel
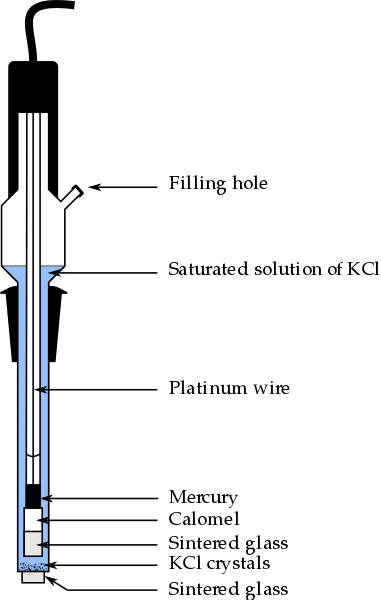 Parties de l'électrode Calomel, l'une des électrodes de référence les plus utilisées en chimie analytique. Source: Bachi-Bouzouk via Wikipedia.
Parties de l'électrode Calomel, l'une des électrodes de référence les plus utilisées en chimie analytique. Source: Bachi-Bouzouk via Wikipedia. Dans l'image supérieure, les parties conventionnelles d'une électrode de calomel saturée sont représentées, ECS. On dit qu'il est saturé car il contient une solution saturée de KCl (bleu), qui présente également des déroulements de KCL.
La colonne interne, parcourue par un fil de platine, est remplie de mercure, qui à son tour contacte une pâte de calomel, Hg2CL2 o chlorure de mercure (i), et la solution saturée de KCl. Ainsi, dans cette électrode, la concentration des ions CL est importante-, Puisque sa valeur modifie le potentiel de l'électrode.
La réaction qui a lieu est la suivante:
HG2CL2(s) + 2e- ⇌ 2Hg (l) + 2cl-
Et il a un eº de 0.241 V.
À l'extrémité inférieure de l'ECS, il y a un frit poreux, qui est mis en contact électrique avec la solution de l'analyte et permet l'échange contrôlé d'ions ions-. Sinon, il y aurait une contamination des chlorures dans l'échantillon, et l'électrode perdrait sa précieuse solution de KCL saturée.
Cette électrode est utilisée pour les mesures de pH et en général de tout analyte dont la concentration peut être déterminée dans un milieu aqueux.
Il peut vous servir: alcool thermique: structure, propriétés, risques et utilisationsElectrode d'argent en argent
 Electro argenté en argent. Source: TenofallTrades (Talk) (Téléchargements). / Domaine public
Electro argenté en argent. Source: TenofallTrades (Talk) (Téléchargements). / Domaine public Semblable à l'électrode de Calomel, l'électrode en argent en argent se compose d'un fil d'argent recouvert de chlorure d'argent, et également immergé dans une solution saturée d'un mélange de KCL et AGCL.
Toutes ses pièces sont protégées dans un tube en plastique, qui a une ouverture poreuse à travers laquelle il établit un contact électrique avec la solution.
La réaction qui définit son potentiel, eº = 0.197 V, est le suivant:
AGCL (S) + E- ⇌ AG (S) + CL-
Cette électrode présente des utilisations et des préférences plus importantes que celles du calomel, qui est due à l'impact négatif du mercure sur l'environnement. D'un autre côté, les électrodes en argent solide en argent sont plus simples, sûres et bon marché à construire dans le laboratoire.
Nous disons alors que l'électrode à fourche argentée remplace les Calomel dans bon nombre de ses applications (degrés potentiométriques, tests de corrosion, analyse électrochimique, etc.).
C'est également l'une des options préférées en biologie et en médecine, en particulier à l'électrocardiographie et à l'électroencéphalographie, car l'argent ou leur sel sont des substances relativement toxiques pour le corps.
Les références
- Jour, r., & Underwood, un. (1965). Chimie analytique quantitative. (Fifth Ed.). Pearson Prentice Hall.
- Skoog d.POUR., Ouest D.M. (1986). L'analyse instrumentale. (Deuxième Ed.). Inter-américain., Mexique.
- Wikipédia. (2020). Référence d'électrode. Récupéré de: dans.Wikipédia.org
- Elsevier B.V. (2020). Référence d'électrode. ScienceDirect. Récupéré de: ScienceDirect.com
- CHIMISTER BOOLISTexts. (9 juin 2020). Électrodes de référence. Récupéré de: Chem.Bibliothèque.org
- « Emplacement du phare d'Alexandrie, histoire, description, ruines
- Emily Dickinson Biographie, réalisations, œuvres, phrases »

