Coprécipitation
- 4439
- 91
- Louna Baron
Qu'est-ce que la coprécipitation?
La Coprécipitation C'est la précipitation d'un solide qui traîne normalement des substances solubles et qui se produisent à l'intérieur du solide ou sur sa surface en même temps que ce précipité.
Vu de cette manière, vous pouvez générer une contamination d'une substance insoluble qui transporte des solutés dissous du milieu liquide. Le mot «pollution» est appliqué aux cas où des solutés solubles précipités par un support insoluble ne sont pas souhaitables, mais quand ils ne le sont pas, il s'agit d'une méthode analytique ou synthétique alternative.
D'un autre côté, le support insoluble est la substance précipitée. Cela peut transporter le soluté soluble à l'intérieur (absorption) ou à sa surface (adsorption). La façon dont elle changera complètement les propriétés physicochimiques du solide résultant.
Bien que le concept de coprécipitation puisse sembler un peu déroutant, il est plus courant qu'on ne le pense, car plus que de simples solides contaminés, des solutions solides de structures complexes et des composants inestimables sont formés. La terre à partir desquelles les plantes sont nourries, est un exemple de coprécipitation.
De même, les minéraux, la céramique, les argiles et les impuretés sur la glace sont également un produit de ce phénomène. Sinon, les sols perdraient une grande partie de leurs éléments essentiels, les minéraux ne seraient pas comme ils sont connus, et il n'y aurait pas non plus de méthode importante pour la synthèse de nouveaux matériaux.
Exemple de coprécipitation
Pour mieux comprendre l'idée de coprécipitation, l'exemple suivant est proposé.
 Exemples de coprécipitation. Source: Gabriel Bolívar
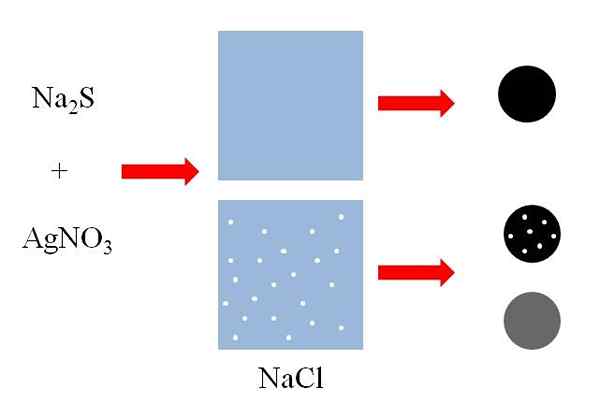
Exemples de coprécipitation. Source: Gabriel Bolívar En haut (image supérieure) Il y a deux conteneurs avec de l'eau, dont on contient du NaCl dissous. NaCl est un sel de sel très soluble, mais les tailles de points blancs sont exagérés à des fins explicatives. Chaque point blanc deviendra de petits agrégats NaCl dans une solution au bord de la saturation.
Peut vous servir: Fermio (FM)Ajouté aux deux récipients un mélange de sulfure de sodium, na2S et nitrate d'argent, Agno3, Il précipitera un soufre en argent noir insoluble solide, AGS:
N / A2S + Agno3 => AGS + Nano3
Comme on peut le voir dans le premier récipient avec de l'eau, un noir solide (sphère noire) précipite. Cependant, ce solide dans le récipient NaCl dissous transporte des particules de ce sel (sphère noire avec des points blancs). NaCl est soluble dans l'eau, mais lorsque l'AGS précipite, il s'adsorbe sur la surface noire.
On dit ensuite que le NaCl a coprécipité sur l'AGS. Si le solide noir était analysé, les micro-étapes de NaCl pouvaient être observées à la surface.
Cependant, ces cristaux pourraient également être à l'intérieur de l'AGS, donc le solide "tournerait" gris (blanc + noir = gris).
Types de Coprécipitation
La sphère noire avec des points blancs et la sphère grise montrent qu'un soluté soluble peut coprocipiter de différentes manières.
Dans le premier, il le fait superficiellement, adsorbé sur le support insoluble (AGS dans l'exemple précédent), tandis que dans la seconde, il le fait en interne, "changeant" la couleur noire du précipité.
Les autres types de solides peuvent-ils être obtenus? C'est-à-dire une sphère avec des phases noires et noires, c'est-à-dire d'Ags et de NaCl (avec Nano3 qui aussi coprecipita). C'est là que survient l'ingéniosité de la synthèse de nouveaux solides et matériaux.
Cependant, revenant au point initial, fondamentalement le soluté de coprécipita soluble générant différents types de solides. Les types de coprécipitation et les solides qui en résultent seront mentionnés ci-dessous.
Il peut vous servir: des matériaux qui ont peu de résistance au passage de l'électricitéInclusion
On parle d'inclusion lorsque, dans le réseau cristallin, l'un des ions peut être remplacé par une partie de la substance soluble coprécipitée.
Par exemple, si NaCl avait coprégé par inclusion, les ions na+ Ils auraient occupé la place de l'Ag+ Dans une section de la disposition cristalline.
Cependant, de tous les types de coprécipitation, c'est le moins probable, car, pour qu'elle se produise, les radios ioniques doivent être très similaires. De retour à la sphère grise de l'image, l'inclusion serait représentée par l'un des tons gris plus clairs.
Comme mentionné, l'inclusion est donnée dans les solides cristallins et les obtenir, le domaine de la chimie des solutions et de plusieurs facteurs (T, pH, temps d'agitation, relations molaires, etc.).
Occlusion
En occlusion, les ions sont piégés dans le réseau cristallin mais sans remplacer aucun ion de l'arrangement. Par exemple, dans les AG, vous pouvez former des cristaux d'ocluido. Graphiquement, il pourrait être visualisé comme un cristal blanc entouré de cristaux noirs.
Ce type de coprécipitation est l'un des plus courants, et grâce à lui, il y a la synthèse de nouveaux solides cristallins. Les particules obluides ne peuvent pas être éliminées avec des lavages simples. Pour ce faire, il serait nécessaire de recrit l'ensemble entier, c'est-à-dire le support insoluble.
L'inclusion et l'occlusion sont des processus d'absorption donnés dans les structures cristallines.
Adsorption
Dans l'adsorption, le solide coprécipité est à la surface du support insoluble. La taille des particules de ce support définit le type de solide obtenu.
Peut vous servir: IsóbarosS'ils sont petits, un solide coagulé sera obtenu, à partir de laquelle il est facile d'éliminer les impuretés. Mais s'ils sont très petits, le solide absorbe les quantités abondantes d'eau et sera gélatineuse.
Revenant dans la sphère noire avec des points blancs, des cristaux de NaCl coprécipités sur l'AG peuvent être lavés à l'eau distillée. Ainsi, jusqu'à purifier l'AGS, qui peut ensuite être chauffant pour évaporer toute l'eau.
Applications du Coprécipitation
Certaines des applications de coprécipitation sont les suivantes:
- Permet de quantifier des substances solubles qui ne sont pas facilement précipitées à partir du milieu. Ainsi, grâce à un soutien insoluble, il mène, par exemple, des isotopes radioactifs, tels que Francio, pour une étude et une analyse ultérieures.
- Lorsque les ions coprécipitants dans des solides gélatineux, le milieu liquide est purifié. L'occlusion est encore plus souhaitée dans ces cas, car l'impureté ne pourra pas s'échapper.
- La coprécipitation permet d'incorporer des substances dans des solides pendant leur formation. Si le solide est un polymère, il absorbera les solutés solubles qui copirera alors à l'intérieur, en lui donnant de nouvelles propriétés. S'il s'agit de la cellulose, par exemple, le cobalt (ou tout autre métal) pourrait être fait en coprécipite.
- En plus de tout ce qui précède, la coprécipitation est l'une des principales méthodes de synthèse des nanoparticules sur un support insoluble. Grâce à cela, les bionanomatériaux et les nanoparticules de magnétite ont été synthétisés, entre autres.
Les références
- Précipitations et co-précipitations. Nptel a récupéré.CA.dans
- Qu'est-ce que la coprécipitation. Récupéré de Wisegeek.com

