Caractéristiques, formation, exemples
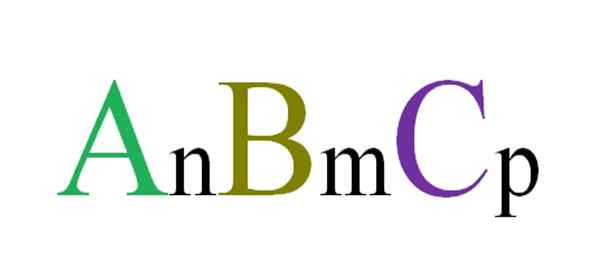
- 2608
- 575
- Prof Noah Collet
Les Composés ternaires Ce sont tous ceux qui sont composés de trois atomes ou ions différents. Ils peuvent être très diversifiés, des substances acides ou de base, aux alliages métalliques, minéraux ou matériaux modernes. Les trois atomes peuvent appartenir au même groupe du tableau périodique ou procéder avec des emplacements arbitraires.
Cependant, pour que le composé ternaire se produise, il doit y avoir une affinité chimique entre ses atomes. Tous ne sont pas compatibles les uns avec les autres, et vous ne pouvez donc pas simplement choisir au hasard les trois intégreront et définiront le composé ou le mélange (en supposant le manque de liaisons covalentes).
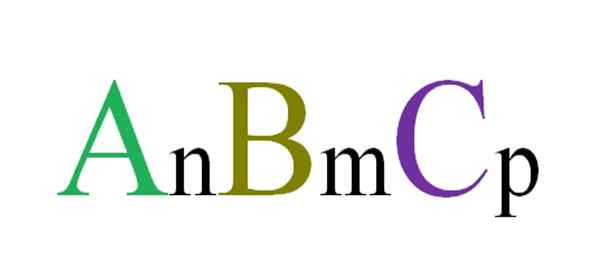 Formule générale et aléatoire pour les composés ternaires. Source: Gabriel Bolívar.
Formule générale et aléatoire pour les composés ternaires. Source: Gabriel Bolívar. Par exemple, trois lettres sont choisies au hasard qui régiront un composé ternaire ABC (image supérieure). Les indices n, m et p indiquent les relations stoechiométriques entre les atomes ou les ions A, B et C. Variant les valeurs de ces indices et les identités des lettres, des composés ternaires sans fin sont obtenus.
Cependant, formule AnBmCp Il ne sera valable que s'il rencontre l'électroneutralité; c'est-à-dire que la somme de vos charges doit être égale à zéro. Dans cet esprit, il existe des limites physiques (et chimiques) qui guident si la formation dudit composé ternaire est possible ou non.
[TOC]
Caractéristiques des composés ternaires
Ses caractéristiques ne sont pas générales mais varient en fonction de leur nature chimique. Par exemple, les oxoacides et les bases sont des composés ternaires, et chacun d'eux partage ou non une série de caractéristiques représentatives.
Maintenant, avant un composé hypothétique ABC, cela peut être ionique, si les différences d'électronégativité entre A, B et C ne sont pas importantes; ou covalent, avec des liens a-b-c. Ces derniers sont donnés dans des exemples infinis dans la chimie organique, comme avec les alcools, les phénols, les éthers, les glucides, etc., dont les formules peuvent être décrites avec CnHm SOITp.
Peut vous servir: propriétés mécaniques des métauxAinsi, les caractéristiques sont très variées et oscillent dans le degré élevé d'un composé ternaire à un autre. Le composé CnHmSOITp On dit qu'il est oxygéné; tandis que cnHmNp, D'un autre côté, c'est de l'azote (c'est une amine). D'autres composés peuvent être du soufre, des phosphorés, des fluorisations ou un caractère métallique marqué.
Bases et acides
En progressant dans le domaine de la chimie inorganique, vous avez des bases métalliques, mnSOITmHp. Donner.
Par exemple, la base de Naoh, compte tenu de ces indices, devrait être écrite comme NA1SOIT1H1 (qui serait chaotique). De plus, il serait supposé que h est un cation h+, Et pas comment cela apparaît vraiment: faire partie de l'anion oh-. En raison de l'action de OH- Sur la peau, ces bases sont des savons et caustiques.
Les bases métalliques sont des substances ioniques, et bien qu'elles se composent de deux ions, mn+ et oh- (N / A+ et oh- Pour le naOH), ce sont des composés ternaires pour avoir trois atomes différents.
Les acides, en revanche, sont covalents, et leur formule générale est Hao, où un atome non métallique est généralement. Cependant, étant donné sa facilité d'ionisé dans des hydrogènes de libération d'eau, ses ions H+ Corroen et blesser la peau.
Nomenclature
Comme les caractéristiques, la nomenclature des composés ternaires est très variée. Pour cette raison, seules les bases, les oxoacides et les oxisaux seront considérés comme superficiellement.
Bases
Les bases en métal sont d'abord mentionnées avec le mot «hydroxyde» suivi du nom du métal et de sa valence en nombre romain entre parenthèses. Ainsi, NaOH est l'hydroxyde de sodium (I); Mais comme le sodium a une valence unique de +1, il reste simplement comme un hydroxyde de sodium.
Il peut vous servir: AlceansL'al (oh)3, Par exemple, il s'agit d'hydroxyde d'aluminium (III); et cu (oh)2, Hydroxyde de cuivre (II). Bien sûr, tout selon la nomenclature systématique.
Oxoacides
Les oxóacides ont une formule assez générale du type Hao; Mais en réalité, ils sont mieux décrits comme AOH. Le lien de Ha-H émerge le h est libéré+.
La nomenclature traditionnelle est la suivante: le mot «acide» commence, suivi du nom de l'atome central, précédé ou précédé de leurs préfixes respectifs (hypo, per) ou suffixes (ours, ICO) selon qu'il travaille avec ses mineurs ou valences plus anciennes.
Par exemple, les oxoacides de brome sont HBRO, HBRO2, HBRO3 et hbro4. Ce sont des acides: hypobromous, bromèques, bromiques et perbromiques, respectivement. Notez que dans chacun d'eux, il y a trois atomes avec des valeurs différentes pour leurs indices.
Oxysales
Également appelées sels de nullion, ils sont les plus représentatifs des composés ternaires. La seule différence de les mentionner est que l'ours et l'ICO Sufijos changent pour ITO et ATO, respectivement. De plus, H est remplacé par un cation métallique, produit de la neutralisation acide-base.
Poursuivant avec du brome, ses oxisaux de sodium seraient: Nabro, Nabro2, Nabro3 et nabro4. Leurs noms deviendraient: hipobromito, bromito, bromato et perbromate de sodium. Sans aucun doute, le nombre d'oxistes possibles dépasse celui des oxoacides.
Entraînement
Encore une fois, chaque type de composé ternaire a son propre processus d'origine ou de formation. Cependant, il est juste de mentionner que ceux-ci ne peuvent être formés que s'il existe une affinité suffisante entre les trois membres d'atomes. Par exemple, des bases métalliques existent grâce aux interactions électrostatiques entre les cations et OH-.
Peut vous servir: acide citriqueQuelque chose de similaire se produit avec les acides, qui ne pouvaient pas être formés s'il n'y avait pas de liaison covalente a-o-h.
Sur la base de la question, comment se forment les composés principaux? La réponse directe est la suivante:
- Les bases métalliques sont formées en dissolvant des oxydes métalliques dans l'eau, ou dans une solution alcaline (généralement fournie par NaOH ou l'ammoniac).
- Les oxoacides sont le produit de la dissolution des oxydes non métalliques dans l'eau; Parmi eux, le CO2, CLO2, NON2, Swin3, P4SOITdix, etc.
- Et puis, des oxisaux surgissent lorsque les oxoacides sont alcalisés ou neutralisés avec une base métallique; De là viennent les cations métalliques qui fournissent h+.
D'autres composés ternaires sont formés à la suite d'un processus plus compliqué, comme avec certains alliages ou minéraux.
Exemples
Enfin, une série de formules pour différents composés ternaires sera affichée comme une liste:
- Mg (oh)2
- CR (OH)3
- Kmno4
- N / A3Bêle3
- CD (OH)2
- Grand frère3
- Feaso4
- Bacr2SOIT7
- H2Swin4
- H2Teo4
- HCN
- Il y a
D'autres exemples moins courants (et même hypothétiques) sont:
- Cofcu
- Algasn
- Ucapb
- Perceur2
Les indices N, M et P ont été omis de manière à ne pas compliquer les formules; Bien qu'en réalité, ses coefficients stoechiométriques (sauf pour le meilleur pour le perceur2), peut même avoir des valeurs décimales.
Les références
- Fhiver & Atkins. (2008). Chimie inorganique. (Quatrième édition). Mc Graw Hill.
- Whitten, Davis, Peck & Stanley. (2008). Chimie. (8e Ed.). Cengage Learning.
- MME. Hilfstein. (s.F.). Comununds ternaires. Récupéré de: Tenafly.K12.New Jersey.nous
- Wikipédia. (2019). Banale ternaire. Récupéré de: dans.Wikipédia.org
- Carmen Bello, Arantxa Isasi, Ana Puerto, Germán Tomás et Ruth Vicente. (s.F.). Composés ternaires. Récupéré de: iesdmjac.Éduquer.Aragon.est
- « Caractéristiques des composés quaternaires, formation, exemples
- Caractéristiques spéciales des composés, formation, utilisations »

