Structure d'acide sulfonique, nomenclature, propriétés, utilisations
- 3448
- 637
- Jade Duval
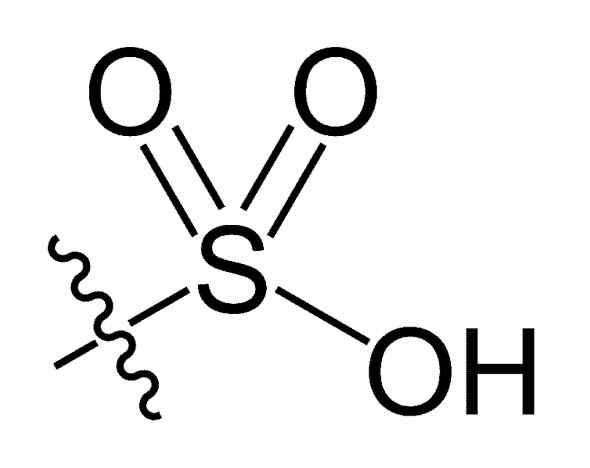
Est appelé acide sulfonique À tous les composés appartenant à une famille d'acides organiques qui ont un ou plusieurs groupes - SO3H. Certains auteurs indiquent que le composé du père est H-S (= O)2-Oh, ou h-so3H, appelé par un «acide sulfonique», cependant, son existence n'a pas été prouvée, ni celle de son tautomère ho-s (= o) -OH appelé «acide de soufre» (H2Swin3), ni en solution ni à l'état solide.
Ce dernier est dû au dioxyde de soufre (IV) (donc2) En solution aqueuse, il devient des ions bisulfites (HSO3-) et pyrosulfite (s2SOIT52-) Et non à h-s (= o)2-Oh ou ho-s (= o) -oh, qui a déjà été prouvé par de nombreux chercheurs en produits chimiques.
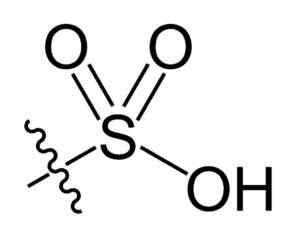 Groupe de sulfonil. Choij [domaine public]. Source: Wikipedia Commons
Groupe de sulfonil. Choij [domaine public]. Source: Wikipedia Commons Dans la formule chimique R-So3H des acides sulfoniques, le groupe R peut représenter les squelettes d'hydrocarbures tels que l'alcane, l'alqueno, l'alchene et / ou le sable. Ceux-ci peuvent contenir des fonctionnalités secondaires telles que l'ester, l'éther, la cétone, l'amino, les groupes amido, hydroxyle, carboxyle et phénol, entre autres.
Les acides sulfoniques sont des acides forts, comparables à l'acide sulfurique (H2Swin4). Cependant, le reste de ses propriétés dépend en grande partie de la nature du groupe R.
Certains ont tendance à Desulfonar à des températures élevées. Cela signifie perdre le groupe -3H, surtout quand R est sableux, c'est-à-dire avec une bague benzène.
Les acides sulfoniques ont de nombreuses utilisations en fonction de leur formule chimique. Ils sont utilisés pour fabriquer des colorants, des encres, des polymères, des détergents, des surfactants et comme catalyseurs, entre autres applications.
[TOC]
Structure
Les acides sulfoniques ont la structure générale suivante:
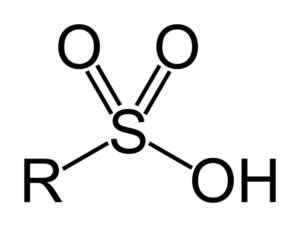 Formule générale des acides sulfoniques. Benjah-bmm27 [domaine public]. Source: Wikipedia Commons
Formule générale des acides sulfoniques. Benjah-bmm27 [domaine public]. Source: Wikipedia Commons Nomenclature
- Groupe sulfonil: -SO3H
- Acide loué ou arillesulfoniques: R-SO3H
Propriétés
Ils sont solides ou liquides en fonction du groupe R. Aucun acide sulfonique gazeux n'est connu.
Ses propriétés physiques et chimiques dépendent de la nature du groupe R. Comme comparaison, il existe certaines propriétés physiques de plusieurs acides sulfoniques, où P.F. C'est le point de fusion et P.et. C'est le point d'ébullition à une pression de 1 mm Hg:
- Acide métanosulfonique: p.F. 20 ºC; p.et. 122 ºC
- Acide Etanosofonic: P.F. -17 ºC; p.et. 123 ºC
- Acide proposulfonique: P.F. -37 ºC; p.et. 159 ºC
- Acide butanosulfonique: p.F. -15 ºC; p.et. 149 ºC
Peut vous servir: chlorure ferreux (FECL2): structure, utilisations, propriétés- Acide pentosulfonique: P.F. -16 ºC; p.et. 163 ºC
- Acide hexanosulfonique: p.F. 16 ºC; p.et. 174 ºC
- Acide benzonique: P.F. 44 ºC; p.et. 172 ºC (à 0,1 mm Hg)
- P-toluensulfonic Acid: P.F. 106 ºC; p.et. 182 ºC (à 0,1 mm Hg)
- 1 acide 1-naphtalensulnique: P.F. 78 ºC; p.et. Il se décompose
- 2-naphthalensulfonic acide: p.F. 91 ºC; p.et. Il se décompose
- Acide trifluorométhanosulfonique: p.F. aucun; p.et. 162 ºC (à 760 mm Hg)
La plupart sont très solubles dans l'eau.
Les acides sulfoniques sont encore plus d'acides que les acides carboxyliques. Ils ont une acidité similaire à celle de l'acide sulfurique. Ils se dissolvent dans l'hydroxyde de sodium aqueux et le bicarbonate aqueux.
Ils ont tendance à souffrir de décomposition thermique, se produisant leur désulfonation. Cependant, plusieurs des acides alkosulfoniques sont thermiquement stables. En particulier, l'acide trifique ou l'acide trifluorométhanesulfonique est l'un des acides les plus forts et les plus stables.
Obtention
Acides arilsulfoniques
Les acides aisulfoniques sont généralement obtenus par le processus de sulfonation qui consiste à ajouter un excès d'acide sulfurique de fumée (H2Swin4 + Swin3) Au composé organique, nous voulons du sulfonar. Par exemple dans le cas du benzène:
C6H6 + H2Swin4 C6H5Swin3H + H2SOIT
Arh + H2Swin4 ARSO3H + H2SOIT
La sulfonation est une réaction réversible, car si nous ajoutons à l'acide benzaulfonique un acide dilué et passez de la vapeur sur le mélange3 Et le benzène est distillé par volatilisation avec de la vapeur, déplaçant l'équilibre vers la désulfonation.
L'agent sulfonant peut également être de l'acide chlorosulfurique, de l'acide sulfamique ou des ions sulfites.
Acides alkylofoniques
Ceux-ci sont généralement préparés par sulfo-oxydation, c'est-à-dire le traitement des composés alkyle avec du dioxyde de soufre2 et oxygène ou2, ou directement avec le trioxyde de soufre3.
RH + 2SO2 + SOIT2 + H2Ou r-so3H + H2Swin4
Applications
Acides sulfoniques pour les tensioactifs et les détergents
Les acides alkybenphiques sont utilisés dans la fabrication de détergents, étant l'une des utilisations les plus répandues.
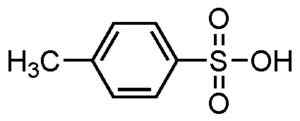 Acide p-méthylbenzefonique. Su-no-g. Source = selfmade. * Date = 21 août 2006. * Fabriqué avec ChemDraw. Source: Wikipedia Commons.
Acide p-méthylbenzefonique. Su-no-g. Source = selfmade. * Date = 21 août 2006. * Fabriqué avec ChemDraw. Source: Wikipedia Commons. Ils sont utilisés pour les détergents en poudre et liquide, les détergents pour les tâches lourdes ou légères, les mains et les savons de shampooing.
Les composants actifs sont généralement l'alkybenzène linéaire et les esters gras sulfonés.
Comme les tensioactifs sont des sulfonates d'alpha-oléfine communs, des sulfobétines, des sulfosuccinates et des disulfonates étére loués diffeniliques, qui sont tous dérivés d'acides sulfoniques.
Peut vous servir: oxalate de sodium (NA2C2O4): Structure, propriétés, utilisations, risquesCes tensioactifs trouvent une utilisation dans les produits de nettoyage des ménages, les cosmétiques, la polymérisation dans les émulsions et la fabrication de produits chimiques pour l'agriculture.
Les ligosulfonates sont dérivés sulfonés de la lignine, un composant du bois, et sont utilisés comme agents dispersants, hydratants et de liaison dans les trottoirs routiers, les additifs en béton et les additifs dans les aliments pour animaux.
Un acide 2-naphtalanosulfonique dérivé est utilisé pour augmenter la fluidité et la résistance du ciment.
Coloration à base d'acide sulfonique
Ceux-ci sont généralement caractérisés par des groupes Azo (R-N = N-R).
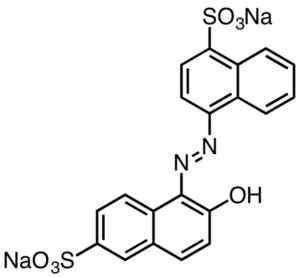 Coloration rouge acide. Smokefoot [cc by-sa 4.0 (https: // CreativeCommons.Org / licences / by-sa / 4.0)]. Source: Wikipedia Commons.
Coloration rouge acide. Smokefoot [cc by-sa 4.0 (https: // CreativeCommons.Org / licences / by-sa / 4.0)]. Source: Wikipedia Commons. Les colorants dérivés d'acide sulfonique ont une utilité dans l'industrie du papier, des encres telles que l'impression d'injection, des textiles tels que le coton et la laine, les cosmétiques, les savons, les détergents, la nourriture et le cuir.
Un dérivé d'acide 2-naphtalanosulfonique est également utilisé comme ingrédient de coloration pour les fibres de polyester et le bronzage en cuir.
Amides à base d'acides sulfoniques
Cette application met en évidence les acides acrylamidefoniques, qui ont des polymères, dans l'électrode métallique, comme les tensioactifs et les revêtements anti-companions transparentes.
Ils sont également utilisés dans l'amélioration de la récupération du pétrole, en tant qu'agents liblérés en composés sur le sol, dans des mélanges de ciment hydrauliques et en tant que résines aminoplasiques durcissant les accélérateurs.
Certains sulfonamides sont également utilisés dans les formules d'insecticide.
Acides sulfoniques fluorés et chlorofluor
Ce groupe met en évidence l'acide trifluorométhanosulfonique (cf3Swin3H), également appelé acide trifique. Ce composé a une catalyse des réactions de synthèse et de polymérisation organiques.
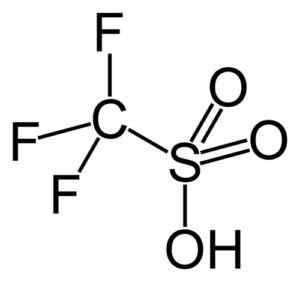 Acide. Capacio [cc by-sa 3.0 (https: // CreativeCommons.Org / licences / by-sa / 3.0)]. Source: Wikipedia Commons.
Acide. Capacio [cc by-sa 3.0 (https: // CreativeCommons.Org / licences / by-sa / 3.0)]. Source: Wikipedia Commons. Par exemple, il est utilisé dans la polymérisation des oléfines aromatiques et dans la préparation d'hydrocarbures paraffiniques hautement ramifiés avec un nombre d'octane élevé pour les utiliser comme additifs de carburant.
Une autre de ses applications réside dans la synthèse de polymères conducteurs, au moyen du dopage de polyacéthylène, produisant, par exemple, des semi-conducteurs de type p.
Acide pentafluoroetanosulfonique (cf3Cf2Swin3H), connu sous le nom d'acide pentaplique, est utilisé comme catalyseur organique.
L'acide trifique réagit avec l'antimoine pentafluorure (SBF5) Générer le "acide magique" si appelé, un catalyseur super acide qui sert à l'alkylation et à la polymérisation.
Peut vous servir: teinture d'iode: propriétés, utilisations, contre-indicationsNafion-H est une résine d'échange d'ions d'un acide sulfonique polymère parfumé. Il a la caractéristique d'être inerte envers les acides forts, les bases fortes et la réduction ou l'oxydation des agents.
Dans les applications biologiques
L'un des rares acides sulfoniques trouvés dans la nature est l'acide 2-aminoéthanosulfonique, mieux connu sous le nom de corrida, un acide essentiellement aminé en particulier pour les chats.
La combustion synthétique et naturelle est utilisée comme suppléments dans les aliments pour animaux de compagnie et les produits pharmaceutiques.
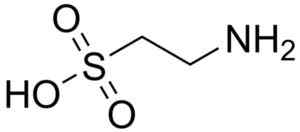 Molécule de taureaux. Harbinaire. Source: Wikipedia Commons
Molécule de taureaux. Harbinaire. Source: Wikipedia Commons L'acide taurocolique est une composante biliaire et participe à la digestion des graisses. L'acide 8-anilino-1-naphtalanosulfonique, un composé synthétique, est utilisé dans l'étude des protéines.
Les copolymères d'urée et l'acide biphényldisulfonique ont été utilisés comme inhibiteurs du virus de l'herpès simplex.
Certains dérivés d'acide sulfonique, tels que le polystyrène sulfoné et certains azocompiestos, ont montré des propriétés d'inhibition de l'immunodéficience humaine ou du virus du VIH, sans être excessivement toxique contre les cellules hôtes.
Dans l'industrie pétrolière
Certains mélanges de dérivés d'huile, qui incluent une combinaison variée de paraffines aromatiques et aromatiques polynucléaires, peuvent être sulfonées puis correctement neutralisées en générant les sulfonates d'huile SO appelés.
Ces sulfonates d'huile ont la propriété de réduire la tension chirurgicale dans l'eau. De plus, sa production est à très faible coût.
Pour cette raison, les sulfonates d'huile sont injectés dans des puits de pétrole existants aidant la récupération de pétrole brut qui est occlus entre les roches sous la surface.
Dans la formulation des lubrifiants et anticorrosifs
Les sulfonates de magnésium ont une large utilisation dans des formules lubrifiantes telles que la dispersion des additifs de détégents et pour éviter l'usure.
Les sulfonates de baryum sont utilisés dans les lubrifiants anti-flint pour les utilisations utilisées dans les applications à haut débit. Les sulfonates de sodium et de calcium ont des lubrifiants et des graisses pour améliorer les propriétés de pression extrême.
Les sels de magnésium d'acide sulfonique sont également utiles dans des applications anticorrosives telles que les revêtements, les graisses et les résines.
Les références
- Falk, Michael et Giguere, Paul A. (1958). Sur la nature de l'acide sulfureux. Canadian Journal of Chemistry, Vol. 36, 1958. Récupéré de nrCresearchPress.com
- Betts, R.H. et voss, r.H. (1970). La cinétique de l'échange d'oxygène entre l'ion sulfite et l'eau. Canadian Journal of Chemistry, Vol. 48, 1970. Récupéré de nrCresearchPress.com
- Coton, F.POUR. Et Wilkinson, G. (1980). Chimie inorganique avancée. Quatrième édition. Chapitre 16. John Wiley & Sons.
- Kirk-othmer (1994). Encyclopédie de la technologie chimique. Volume 23. Quatrième édition. John Wiley & Sons.
- Kosswig, Kurt. (2012). Tensioactif. Encyclopédie d'Ullmann de la chimie industrielle Vol. 35. Wiley-VCH Verlag GmbH & Co.
- « Structure du dioxyde de chlore (CLO2), utilisation, obtention, risques, propriétés
- Structure d'acide polyactique, propriétés, synthèse, utilisations »

