Structure du cycle (C5H10), propriétés et utilisations
- 3063
- 384
- Paul Dumas
Il cyclopentano Il s'agit d'hydrocarbures cycliques, en particulier un cycloalcano. À son tour, c'est un composé organique dont la formule moléculaire est C5Hdix. Peut être visualisé comme la version fermée du n-Pentano, chaîne ouverte, dans laquelle ses extrémités se sont jointes en perdant deux atomes d'hydrogène.
Dans l'image inférieure, le squelette du cyclopentano est montré. Notez à quel point votre squelette se porte géométrique, formant une bague pentagonale. Cependant, sa structure moléculaire n'est pas plate, mais présente des plis qui cherchent à stabiliser et à réduire les tensions à l'intérieur de l'anneau. Le vélo est un liquide très volatil et inflammable, mais pas autant que le n-Pentano.
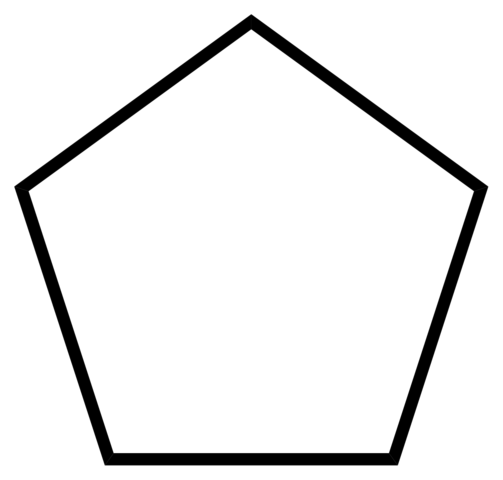 Squelette de carbone du cyclopentano. Source: CCROBERTS [Domaine public]
Squelette de carbone du cyclopentano. Source: CCROBERTS [Domaine public] En raison de sa capacité de solvant, le cyclopentano est l'un des solvants les plus utilisés dans les industries chimiques. Il n'est pas surprenant que de nombreux produits de forte odeur le contiennent parmi leur composition, étant donc inflammable. Il est également utilisé comme agent d'extension pour les mousses de polyuréthane utilisées dans les réfrigérateurs.
[TOC]
Structure de Ciclipentano
Interactions intermoléculaires
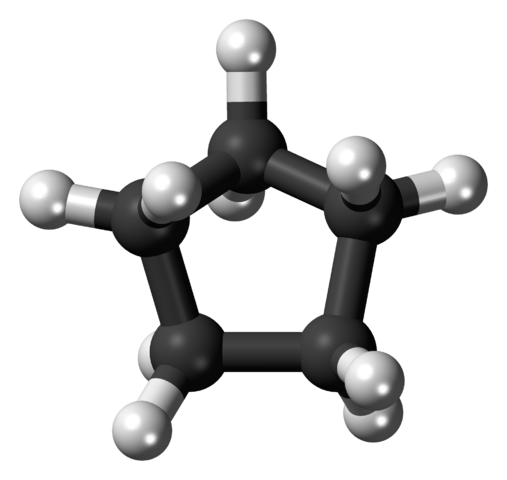
 Structure moléculaire du cyclopentano représenté par un modèle de sphères et de barres. Source: Jynto [CC0]
Structure moléculaire du cyclopentano représenté par un modèle de sphères et de barres. Source: Jynto [CC0] Dans la première image, le squelette du cyclopentano a été montré. Nous voyons maintenant qu'il s'agit plus qu'un simple pentagone: sur ses bords, les atomes d'hydrogène (sphères blanches) se démarquent, tandis que les atomes de carbone constituent l'anneau pentagonal (sphères noires).
N'ayant que des liaisons C-C et C, son moment dipolaire est insignifiant, donc les molécules de cyclopentano ne peuvent pas interagir entre elles par les forces dipol-dipolo. Au lieu de cela, ils restent cohésifs grâce aux forces dispersives de Londres, avec les anneaux essayant d'en empiler l'un sur l'autre.
Cette pile offre une certaine zone de contact que disponible entre les molécules linéaires de n-Pentano. En conséquence, le cyclopentano a un point d'ébullition plus élevé que le n-Pentano, ainsi qu'une pression de vapeur inférieure.
Il peut vous servir: 7 pratiques de laboratoire de chimie (simple)Les forces dispersives sont responsables de la forme du cyclopentano un cristal moléculaire lors du gel à -94 ºC. Bien qu'il n'y ait pas beaucoup d'informations sur sa structure cristalline, ceci est polymorphe et a trois phases: I, II et III, étant la phase II un mélange désordonné de I et III.
Conformation et tension anulaire
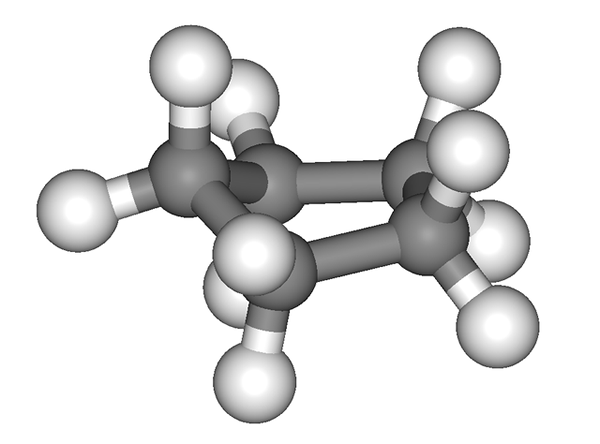 La bague Cyclopentano n'est pas totalement plate. Source: EDGAR181 [Domaine public]
La bague Cyclopentano n'est pas totalement plate. Source: EDGAR181 [Domaine public] L'image précédente donne la fausse impression que le cycle est plat; Mais ce n'est pas comme ça. Tous leurs atomes de carbone ont une hybridation SP3, Donc leurs orbitales ne sont pas situées dans le même plan. De même, comme si cela ne suffisait pas, les atomes d'hydrogène sont très proches les uns des autres, se réplant fortement lorsqu'ils sont éclipsés.
Ainsi, c'est parler de conformations, l'une d'entre elles étant la demi-chaise (image supérieure). De ce point de vue, il est clair que la bague Cyclopentano présente des plis, ce qui aide à réduire ses annulations annulées en raison de leurs atomes de carbone si près les uns des autres.
Cette tension est due au fait que les liaisons C-C ont des angles inférieurs à 109'5º, la valeur idéale pour le produit de l'environnement tétraédrique de leurs hybridations SP3.
Cependant, malgré cette tension, le cycle est un composé plus stable et moins inflammable que le pentan. Cela peut être vérifié en comparant ses rhombes de sécurité, dans lesquelles l'inflammabilité du cycle en a 3, tandis que celle du pentan, 4.
Propriétés de Ciclipentano
Apparence physique
Liquide incolore avec une odeur douce similaire à l'huile.
Peut vous servir: étapes de chimieMasse molaire
70,1 g / mol
Point de fusion
-93,9 ºC
Point d'ébullition
49.2 ºC
point de rupture
-37,2 ºC
Température d'auto-direction
361 ºC
Chaleur de vaporisation
28,52 kJ / mol à 25 ºC
Gelée
0,413 MPa · s
Indice de réfraction
14065
La pression de vapeur
45 kPa à 20 ° C. Cette pression correspond à environ 440 atm, cependant, cependant que celle de la n-Pentano: 57,90 kpa.
Ici, l'effet de la structure se manifeste: le cycle cyclopentano permet des interactions intermoléculaires plus efficaces, qui cohérentes et conservent ses molécules dans le sein du liquide par rapport aux molécules linéaires des molécules linéaires des molécules des molécules linéaires du n-Pentano. Par conséquent, ce dernier a une plus grande pression de vapeur.
Densité
0,751 g / cm3 à 20 ºC. D'un autre côté, ses vapeurs sont 2,42 fois plus denses que l'air.
Solubilité
Dans un litre d'eau à 25 ºC, 156 mg de cyclopentano dissous, en raison de son caractère hydrophobe. Cependant, il est miscible dans les solvants apolaires tels que les autres paraffines, étherres, benzène, tétrachlorure de carbone, acétone et éthanol.
Coefficient de partition octanol / eau
3
Réactivité
Le vélo est stable s'il est correctement stocké. Ce n'est pas une substance réactive car ses liens C-H ou C-C ne sont pas faciles à casser, même lorsqu'il entraînerait la libération d'énergie causée par la tension de l'anneau.
En présence d'oxygène, il brûlera dans une réaction de combustion, qu'ils soient complets ou incomplets. Comme le cycle est un composé très volatil, il doit être stocké dans des endroits où il ne peut être exposé à aucune source de chaleur.
Entre-temps, en l'absence d'oxygène, le cyclopentano subira une réaction de pyrolyse, se décomposant dans des molécules plus petites et insaturées. L'un d'eux est le 1-pentène, qui démontre que la chaleur brise l'anneau Cyclopentano pour créer un alcène.
Il peut vous servir: salicylate de méthyleD'un autre côté, le cyclopentano peut réagir avec le brome sous rayonnement ultraviolet. De cette façon, l'une de ses liaisons C-H est remplacée par C-Br, qui à son tour peut être remplacée par d'autres groupes; Et ainsi, les dérivés de cyclopentano émergent.
Applications
Solvant industriel
Le caractère hydrophobe et apolaire du cyclopentano est fabriqué par un degré de solvant, à côté des autres solvants paraffiniques. Pour cette raison, cela fait généralement partie des formulations de nombreux produits, tels que la colle, les résines synthétiques, les peintures, les adhésifs, le tabac et l'essence.
Source d'éthylène
Lorsque le cyclopentano est soumis à une pyrolyse, l'une des substances les plus importantes qu'elle génère est l'éthylène, qui possède d'innombrables applications dans le monde des polymères.
Mousses isolantes en polyuréthane
L'une des utilisations les plus remarquables de Cycopentano est en tant qu'agent d'expansion pour la fabrication de mousses isolantes en polyuréthane; C'est-à-dire que les vapeurs de cyclopentano, suivant leur grande pression, développent le matériau polymère jusqu'à ce qu'ils lui donnent une mousse avec des propriétés bénéfiques à utiliser dans le cadre des réfrigérateurs ou des congélateurs.
Certaines entreprises ont choisi de remplacer les HFC par Cyclopentano dans la fabrication de matériaux isolants, car il ne contribue pas à la détérioration de la couche d'ozone et réduit également la libération de gaz à effet de serre à l'environnement.
Les références
- Graham Salomons t.W., Craig B. Fryhle. (2011). Chimie organique. (dixe Édition.). Wiley Plus.
- Carey F. (2008). Chimie organique. (Sixième édition). Mc Graw Hill.
- Wikipédia. (2020). Cyclopentane. Récupéré de: dans.Wikipédia.org
- Centre national d'information sur la biotechnologie. (2020). Cyclopentane. Base de données PubChem, CID = 9253. Récupéré de: pubchem.NCBI.NLM.NIH.Gouvernement
- Elsevier B.V. (2020). Cyclopentane. ScienceDirect. Récupéré de: ScienceDirect.com
- Appareils GE. (11 janvier 2011). Réduction des émissions de gaz à effet de serre dans les installations de fabrication de réfrigérateur de GE. Récupéré de: salle de presse.Geais.com
- « Processus d'émulsion de l'émulsifiant, aspects moléculaires, applications
- Ville industrielle comment est né, la structure, les conséquences, les problèmes »

