Fondation de tampon de phosphate (PBS), préparation et utilisations

- 3941
- 881
- Prof Ines Gaillard
Il tampon de phosphate, BPS ou tampon phosphate salin Il s'agit d'une solution tampon et isotonique, dont la fonction est de maintenir le pH et la pression osmotique le plus proche de l'environnement naturel (physiologique). L'acronyme PBS signifie saline tamponnée au phosphate.
Le pH et l'osmolarité sont deux aspects très importants qui doivent être contrôlés dans certains protocoles de laboratoire. Dans le cas du pH, il est essentiel qu'il soit contrôlé, en particulier dans les réactions biochimiques, car elles peuvent varier ou ne pas s'exécuter si les réactifs sont dans un pH inapproprié.
 Tampon salino pbs phosphate en deux pH différents. Source: Pixinio.com
Tampon salino pbs phosphate en deux pH différents. Source: Pixinio.com Tandis que le contrôle de l'osmolarité est essentiel, surtout lorsque vous travaillez avec des cellules vivantes, car les membranes plasmatiques des cellules réagissent en fonction de la concentration de solutés dans lesquels ils se trouvent.
Si les cellules sont transférées sur un milieu hypertonique, ils se déshydrateront, car le gradient d'eau sera transporté sur le côté où il y a une plus grande concentration de solutés. Si, au contraire, les cellules sont placées dans un milieu hypotonique, les cellules absorberont le liquide jusqu'à ce qu'elles soient menti.
C'est pourquoi le tampon PBS pour les protocoles de laboratoire qui nécessitent une maintenance cellulaire est utilisé In vitro, De cette façon, les cellules ne seront pas endommagées.
Le PBS est composé d'une combinaison de sels, comme le chlorure de sodium, le phosphate de sodium, le chlorure de potassium et le phosphate de potassium. La composition PBS peut varier en fonction du protocole.
[TOC]
Base
Fondamentalement, la fonction du tampon de phosphate salin est de maintenir un pH physiologique constant à côté d'une concentration électrolytique similaire à celle à l'intérieur de l'organisme.
Dans cet environnement, les cellules peuvent rester stables, car les conditions physiologiques simulent autant que possible.
À la formulation PBS d'origine, d'autres composés d'être nécessaires peuvent être ajoutés, par exemple, l'ajout d'EDTA au tampon est utile pour le lavage des globules rouges dans le test d'incompatibilité croisée.
L'EDTA empêche la fraction du complément C1 présent dans le sérum, se diviser et le lise vers les globules rouges, c'est-à-dire éviter de faux résultats d'incompatibilité. De plus, l'EDTA aide à dissocier les cellules.
Peut vous servir: arbre phylogénétique: types et leurs caractéristiques, exemplespréparation
La quantité de sels qui doit être pesée pour l'élaboration du PBS du phosphate salin dépendra de la quantité nécessaire pour préparer:
-Tampon de solution de solution Salino phfosphate (PBS 10X)
Pour un litre de solution:
Peser:
80,6 g de NaCl,
2,2 g de KCL,
11,5 g de Na2HPO4,
2,0 g de kh2HPO4
Technique de préparation
Dans un bécher, placez les sels lourds, ajoutez suffisamment d'eau (80%) et mélangez sur la plaque d'agitation avec une barre magnétique jusqu'à ce que les sels se dissolvent.
 Préparation du PBS Utilisation de fer agitant avec barre magnétique . Source: utilisateur: ruhrfisch, wikipedia. com
Préparation du PBS Utilisation de fer agitant avec barre magnétique . Source: utilisateur: ruhrfisch, wikipedia. com Filtre pour éliminer les particules non liées. Utiliser des filtres avec des pores de 0,45 µm. Autoclave stérilice et distribue aseptiquement dans une cloche d'écoulement laminaire dans des pots en verre avec couvercle.
À la solution 10x (concentrée) n'ajuste pas le pH. Le réglage est effectué une fois dilué à la concentration du tampon PBS 1x (dilution 1:10).
-Tampon de phosphate salin (PBS 1x)
Le PBS 1x peut être préparé directement, pesant les quantités correspondantes de chaque sel ou peut préparer la dilution de la solution mère (1:10) avec de l'eau distillée stérile.
-Pour préparer directement un litre de phosphate salin PBS 1x regrets:
8,06 g de NaCl,
0,22 g de KCL,
1,15 g de Na2HPO4,
0,20 g de kh2HPO4
Technique de préparation
Procéder comme expliqué dans la solution concentrée. Par la suite, le pH doit être ajusté. Pour ce faire, mesurez le pH et selon le résultat, utilisez l'acide (HCl) ou la base (NaOH) pour abaisser ou télécharger le pH respectivement si nécessaire, jusqu'à 7.4.
L'acide ou la base est ajouté à la chute de chute lors de la surveillance de la valeur de pH de la solution à l'aide d'un pH-mètre. Filtre, autoclave stérilice et distribue aseptiquement dans des tubes ou des bouteilles coniques si nécessaire.
-Pour préparer le PBS 1X de la solution mère 10x:
Faire une dilution 1:10. Par exemple, pour préparer 1 litre de PBS 1x, mesurez 100 ml de la solution mère et ajoutez 700 ml d'eau distillée stérile. Ajustez le pH et complétez la quantité d'eau jusqu'à ce qu'elle atteigne 1000 ml.
Peut vous servir: sélection directionnelle: qu'est-ce que la définition, des exemplesLe tampon PBS préparé est incolore et transparent.
PBS à usage quotidien peut être stocké à température ambiante et le reste au réfrigérateur.
.Solutions pour le réglage du pH
HCL
Pour 100 ml de HCl (acide chlorhydrique) à 1 molaire.
Mesurez 91 ml d'eau distillée et placez-la dans un navire précipité de 250 ml de capacité.
Mesurez 8,62 ml de HCl concentré et ajoutez-le lentement au bécher contenant l'eau (ne le fait jamais à l'envers). Prenez des mesures de biosécurité pertinentes lors de la gestion des acides forts (substance hautement corrosive).
Mélanger pendant 5 minutes à l'aide d'une plaque d'agitation avec une barre magnétique à l'intérieur du verre. Allez sur une balle de 100 ml et rincez à 100 ml avec H2Ou distillé.
Naoh
Pour 100 ml de NaOH (hydroxyde de sodium) 10 molaires.
Mesurez 40 ml d'eau distillée et placez-la dans un bécher de capacité de 250 ml. Mesurez 40 GR de NaOH et ajoutez à l'eau. Mélanger à l'aide d'une plaque d'agitation avec une barre magnétique à l'intérieur du verre.
Accédez à une balle agricole de 100 ml et rincez avec de l'eau distillée. Respectez les normes de biosécurité, car cette réaction est exothermique (libère de l'énergie sous forme de chaleur).
Si vous souhaitez préparer d'autres quantités de solution de phosphate saline, vous pouvez consulter le tableau suivant:
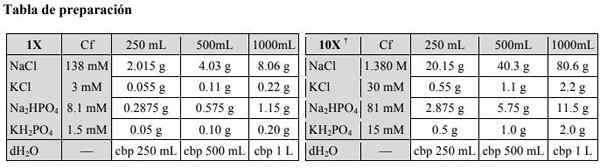 Source: "Laboratoire de génomique virale et humaine, École de médecine UASLP"
Source: "Laboratoire de génomique virale et humaine, École de médecine UASLP" Applications
Il est principalement utilisé dans les laboratoires de biologie cellulaire, l'immunologie, l'immunohistochimie, la bactériologie, la virologie et la recherche.
Il est idéal pour faire le lavage cellulaire par centrifugation (globules rouges), monocapas cellulaire lavé, dans des techniques d'ellipsométrie spectroscopiques, dans la quantification des biofilms bactériens, dans le maintien des cultures cellulaires pour les virus, comme solution de lavage dans la technique de l'indirect immunofluorescence et techniques de caractérisation des anticorps monoclonaux.
Il sert également à transporter des cellules ou des tissus, comme diluant pour le comptage des cellules, la préparation des enzymes cellulaires (triple), comme diluant de la méthode de dessiccation des biomolécules et à préparer d'autres réactifs.
Peut vous servir: Hétérotrophe Nutrition: Caractéristiques, étapes, types, exemplesD'un autre côté, Martin et les collaborateurs en 2006 ont montré que le PBS est utile dans les laboratoires de médecine légale, en particulier dans la récupération des spermatozoïdes à partir de frottis vaginal, ou dans la récupération des cellules vaginales de frottis pénien. De cette façon, il peut être établi s'il y a eu une relation sexuelle.
Limites
-Certains tampons PBS apportent une substance en tant que substance appelée azide de sodium. Ce composé peut générer des substances explosives si elle entre en contact avec le plomb ou le cuivre. Pour cette raison, des soins spéciaux doivent être pris en charge lors de la rejette de ce réactif pour le drainage. S'il est rejeté par cette voie, une eau abondante doit être ajoutée pour diluer au maximum.
-Le tampon de phosphate ne doit pas être ajouté du zinc, car il précipite certains sels.
-Wangen et des collaborateurs en 2018 ont déterminé que l'utilisation de PBS ne convenait pas au lavage de la leucémie myéloïde aiguë primaire (LMA) extraite du sang périphérique, car de nombreuses cellules sont perdues par lyse, avec une forte diminution du matériau protéique.
Par conséquent, ils ont déterminé que les cellules primaires de la LMA ne devraient pas être lavées avec du PBS après le stockage dans de l'azote liquide.
Les références
- Coll J. (1993). Techniques de diagnostic en virologie. Ed Díaz de Santos. 360 PG
- Rodríguez M, Ortiz T. Culture de cellules. Changement de médium. Département de l'histologie normale et pathologique Université de Séville. Disponible en personnel.nous.est
- Préparation de solution saline tamponnée au phosphate (PBS). (2008). Procédures opérationnelles standard (SOPS) Faculté de médecine du laboratoire de génomique virale et humaine UASLP. Disponible chez: Genomics.Uaslp.mx
- "Buff de phosphate salin." Wikipedia, encyclopédie gratuite. Avril 2019, 19:36 UTC. Avril 2019, 02:57 est.Wikipédia.org.
- Pietrasanta L, von-bilderling C.Sujets en biophysique moléculaire. Disponible sur: utilisateurs.Df.Uba.ardente
- Redosser. Manuel d'instructions. PBS + EDTA. Disponible sur: Felsan.com.ardente
- Martin NC, Pirie AA, Ford LV, Callaghan CL, McTurbate K, Lucy D, Scrimger DG. L'utilisation de saline tamponnée au phosphate pour la récupération des cellules et des spermatozoïdes des écouvillons. Justice. 2006; 46 (3): 179-84. Disponible en: NCBI.NLM.NIH.Gouvernement
- Wangen R, Aasebø E, Treeni A, et al. Méthode de préservation et lavage saline tampon. Int J Mol Sci. 2018; 19 (1): 296. Disponible en: NCBI.NLM.NIH.Gouvernement
- Martínez R, Gragera R. (2008). Fondations théoriques et pratiques de l'histochimie. Conseil supérieur des enquêtes scientifiques. Madrid. Disponible sur: livres.Google.co.aller
- « José María Gabriel et Galán Biographie, style et œuvres
- Types de compétences spécifiques, quels sont les utilisations et les exemples »

