Benzyl Hydrogène Brouil, carbocations, radicaux benzyliques

- 1510
- 442
- Paul Dumas
Il benchilo ou benzyle C'est un groupe de substitut commun en chimie organique dont la formule est C6H5Ch2- ou bn-. Structurellement, il se compose simplement de l'union d'un groupe de méthylène, CHO2, Avec un groupe phényle, C6H5; C'est-à-dire un sp3 Lié directement à un anneau de benzène.
Par conséquent, le groupe Benchilo peut être considéré comme un anneau aromatique attaché à une petite chaîne. Dans certains textes, l'utilisation de l'abréviation BN est préférée au lieu de C6H5Ch2-, Reconnaissez-le facilement dans n'importe quel composé; Surtout lorsqu'il est lié à un atome d'oxygène ou d'azote, O-BN ou NBN2, respectivement.
 Groupe de bicrots. Source: Intraralhaosuli [domaine public]
Groupe de bicrots. Source: Intraralhaosuli [domaine public] Ce groupe est également implicitement dans une série de composés largement connus. Par exemple, à l'acide benzoïque, C6H5COOH, pourrait être considéré comme un benchilo dont le carbone de la voiture3 a subi une oxydation exhaustive; ou benzaldéhyde, c6H5Cho, d'oxydation partielle; et alcool benzylique, C6H5Ch2Oh, encore moins oxydé.
Un autre exemple quelque peu évident de ce groupe est à Tolueno, C6H5Ch3, qui peut subir un certain nombre de réactions après la stabilité inhabituelle résultant de radicaux ou de carbocations benzyliques. Cependant, le groupe Burcho sert à protéger les groupes OH ou NH2 de réactions qui modifient indépendante le produit pour synthétiser.
[TOC]
Exemples de composés avec Grupo Benchilo
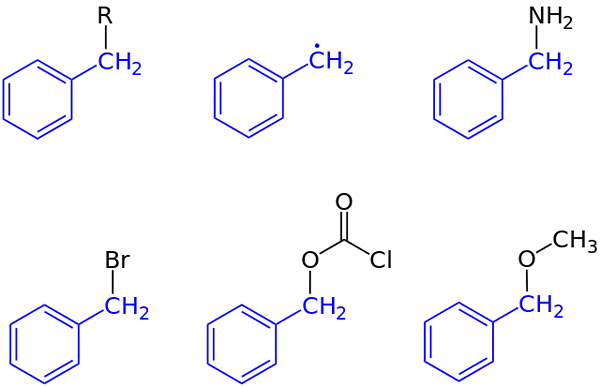 Composés du groupe Burcho. Source: Jü [domaine public]
Composés du groupe Burcho. Source: Jü [domaine public] Dans la première image, la représentation générale d'un composé avec un groupe de crayons a été montrée: C6H5Ch2-R, où r peut être tout autre fragment moléculaire ou atome. Ainsi, la variation de R peut obtenir un nombre élevé d'exemples; Quelques simples, d'autres juste pour une région spécifique d'une structure ou d'un plus grand ensemble.
L'alcool benzylique, par exemple, découle du remplacement de R par OH: C6H5Ch2-Oh. Si au lieu de oh, c'est le groupe NH2, Ensuite, le composé de bancelamine surgit: C6H5Ch2-NH2.
Peut vous servir: borohydride de sodium (NABH4): structure, propriétés, utilisationsSi l'atome qui remplace R est BR, le composé originaire est le bromure de bancl: C6H5Ch2-BR; R par CO2Le CL provient d'un ester, du chlorocarbonate bancil (ou du chlorure de carobenzoxyle); et och3 originaire de l'éther méthylique benzil, C6H5Ch2-Och3.
Même (mais pas du tout correctement), R peut être supposé par un électron solitaire: le radical benzyl, C6H5Ch2·, Produit de la libération du radical r ·. Un autre exemple, bien qu'il ne soit pas inclus dans l'image, est le phénylacétonitrile ou le cyanure de benchilo, C6H5Ch2-CN.
Il y a des composés où le groupe Benchilo représente à peine une région spécifique. Quand c'est le cas, l'abréviation BN est généralement utilisée pour simplifier la structure et ses illustrations.
Hydrogènes benzyl
Les composés ci-dessus ont en commun non seulement le cycle aromatique ou phényle, mais aussi les hydrogènes benzyle; Ce sont ceux qui appartiennent au carbone spo3.
De tels hydrogènes peuvent être représentés comme: bn-ch3, Bn-ch2R ou bn-chr2. Le composé BN-Cr3 Il manque d'hydrogène benzyle, et par conséquent, sa réactivité est inférieure à celle des autres.
Ces hydrogènes sont différents de ceux qui sont généralement liés à un SP un carbone3.
Par exemple, considérez le méthane, Cho4, qui peut également être écrit comme Cho3-H. Pour briser le lien CHO3-H Dans une rupture hétérolytique (formation de radicaux), une certaine quantité d'énergie (104kj / mol) doit être fournie.
Cependant, énergie pour la même rupture de liaison C6H5Ch2-H est inférieur par rapport à celui du méthane (85 kJ / mol). Être moins d'énergie, implique que le radical C6H5Ch2· C'est plus stable que Cho3·. Il en va de même à un degré plus ou moindre avec d'autres hydrogènes benzyliques.
Par conséquent, les hydrogènes benzyl sont plus réactifs lors de la génération de radicaux ou de carbocations plus stables que ceux causés par d'autres hydrogènes. Parce que? La question est répondue dans la section suivante.
Peut vous servir: acide benzoïque (C6H5COOH)Carbocations et radicaux benzyiques
Le R radical était déjà considéré6H5Ch2·, Carbocation benzylique manquante: C6H5Ch2+. Dans le premier, il y a un électron disparu et solitaire, et dans le second une carence électronique. Les deux espèces sont très réactives et représentent des composés transitoires à partir desquels les produits finaux de la réaction proviennent.
Carbone sp3, Après avoir perdu un ou deux électrons pour former le radical ou le carbocation, respectivement, vous pouvez adopter l'hybridation SP2 (plan trigonal), de sorte qu'il y a la moindre répulsion possible parmi ses groupes électroniques. Mais, s'il devient sp2, Comme les carbones de l'anneau aromatique, une conjugaison peut-elle se produire? La réponse est oui.
Résonance dans le groupe Bcordo
Cette conjugaison ou cette résonance est le facteur clé pour expliquer la stabilité de ces espèces de benzyle ou de crayon. Dans l'image suivante, un tel phénomène est illustré:
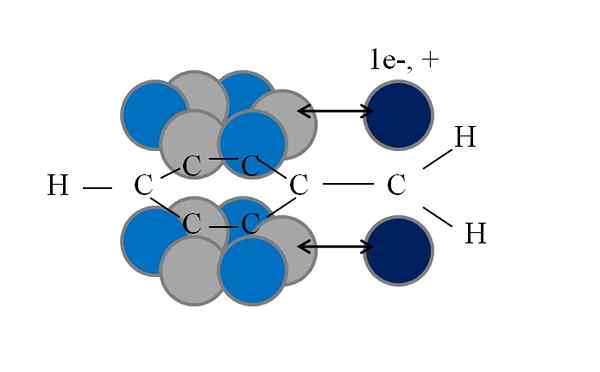 Conjugaison ou résonance dans le groupe Benchilo. Les autres hydrogènes ont été omis pour simplifier l'image. Source: Gabriel Bolívar.
Conjugaison ou résonance dans le groupe Benchilo. Les autres hydrogènes ont été omis pour simplifier l'image. Source: Gabriel Bolívar. Notez que là où l'un des hydrogènes benzyl était une orbitale p Avec un électron disparu (radical, 1E-), ou vide (carbocation, +). Comme on peut le voir, cette orbitale p Il est parallèle au système aromatique (les cercles gris et bleu), la double flèche indiquant le début de la conjugaison.
Ainsi, l'électron disparu et la charge positive peuvent être transférés ou dispersés par l'anneau aromatique, car le parallélisme de ses orbitales le favorise géométriquement. Cependant, ceux-ci ne sont situés dans aucune orbitale p de l'anneau aromatique; Uniquement dans ceux appartenant aux carbones en position ortho et pour le ch2.
Peut vous servir: analyse quantitative en chimie: mesures, préparationC'est pourquoi les cercles bleus clairs se démarquent au-dessus des gris: en eux la densité négative ou positive du radical ou du carbocation est concentrée, respectivement.
Autres radicaux
Il convient de mentionner que cette conjugaison ou cette résonance ne peut pas se produire dans les carbones SP3 plus éloigné de l'anneau aromatique.
Par exemple, radical c6H5Ch2Ch2· Il est beaucoup plus instable car l'électron disparu ne peut pas être conjugué avec l'anneau lorsque le groupe est déposé2 entre et avec l'hybridation SP3. Il en va de même pour C6H5Ch2Ch2+.
Réactions
En résumé: les hydrogènes benzyle sont sujets à réagir, générant un radical ou une carbocation, qui se termine à son tour, provoquant le produit final de la réaction. Par conséquent, ils réagissent par un mécanisme SN1.
Un exemple se compose de bromation du toluène sous rayonnement ultraviolet:
C6H5Ch3 + 1/2BR2 => C6H5Ch2BR
C6H5Ch2Br + 1/2Br2 => C6H5Chbr2
C6H5Chbr2 + 1/2BR2 => C6H5Cbr3
En fait, dans cette réaction, il y a des radicaux br ·.
D'un autre côté, le groupe Benchilo lui-même réagit pour protéger les groupes OH ou NH2 Dans une réaction de remplacement simple. Ainsi, un alcool ROH peut être «benzilad» en utilisant du bromure de benchilo et d'autres réactifs (Koh ou Nah):
Roh + bnbr => Robn + hbr
Robn est un éther benzylique, auquel son groupe OH initial peut être retourné s'il est soumis à un support réducteur. Cet éther doit rester inchangé tandis que d'autres réactions sont effectuées dans le composé.
Les références
- Morrison, R.T. Et Boyd, R. N. (1987). Chimie organique. (5e édition). Addison-wesley iberoamericana.
- Carey, F. POUR. (2008). Chimie organique. (6e édition). McGraw-Hill, Intermerica, rédacteurs.POUR.
- Graham Salomons t.W., Craig B. Fryhle. (2011). Chimie organique. Amines. (10e édition.). Wiley Plus.
- Wikipédia. (2019). Groupe benzyle. Récupéré de: dans.Wikipédia.org
- Docteur. Donald L. Robertson. (5 décembre 2010). Phényle ou benzyle? Récupéré de: à la maison.Miracosta.Édu
- Gamini Gunawardena. (12 octobre 2015). Carbocation benzylique. CHIMISTER BOOLISTexts. Récupéré de: Chem.Bibliothèque.org
- « Explication de proportionnalité composite, trois règles composées, exercices
- Fonctions du système hématopoyétique, tissus, histologie, organes »

