Structure d'alcool thermique, propriétés, risques et utilisations
- 2221
- 96
- Paul Dumas
Il Alcool thermique C'est un composé organique dont la formule est (ch3)3Coh ou t-buoh. C'est l'alcool tertiaire le plus simple de tous. Selon la température ambiante, il est présenté comme un solide ou un liquide incolore. Dans l'image inférieure, ils montrent, par exemple, leurs cristaux incolores.
Cet alcool n'est pas un substrat pour l'enzyme alcoolique déshydrogénase, ni pour l'activité peroxydasique de la catalase, il est donc classé comme un alcool non métabolisant. En raison de ses propriétés biochimiques, on pense qu'elle pourrait être utile dans la détection des hydroxils in vivo dans des cellules intactes.

C'est l'un des quatre isomères de l'alcool isobutilique, étant l'isomère moins sensible à l'oxydation et le moins réactif. Dans la nature, il se trouve dans le pois chiche et dans le manioc ou le manioc, racine qui est fermentée pour produire des boissons alcoolisées.
L'alcool thermique est très soluble dans l'eau et les solvants biologiques. Son utilisation principale est comme un solvant, remplissant ce rôle dans l'élaboration des plastiques, des parfums, des remurshes de peinture, etc.
Comme de nombreux composés organiques, il est un peu toxique, mais à fortes doses, il a un effet narcotique, caractérisé par des maux de tête, des vahidos, des étourdissements, des étourdissements et de la décroissance.
[TOC]
Structure d'alcool thermique
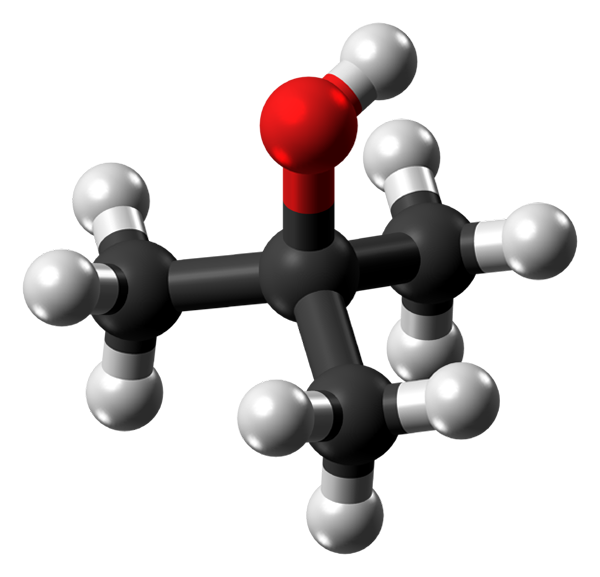
 Molécule d'alcool thermique. Source: Jynto via Wikipedia.
Molécule d'alcool thermique. Source: Jynto via Wikipedia. Dans l'image supérieure, vous avez la structure moléculaire de l'alcool thermique avec un modèle de sphères et de barres. La molécule entière a une géométrie tétraédrique mondiale, avec le 3ème carbone situé dans son centre, et les groupes3 Et oh dans ses sommets.
En observant cette structure, on comprend pourquoi cet alcool est tertiaire: le carbone du centre est lié à trois autres carbones. Poursuivant avec le tétraèdre, la partie inférieure peut être considérée comme apolaire, tandis que son sommet supérieur, polaire.
Il peut vous servir: réaction Fehling: préparations, agents actifs, exemples, utilisationsDans ce sommet est le groupe OH, qui crée un dipôle permanent et permet également aux molécules de T-Buoh d'interagir par des ponts d'hydrogène; de la même manière que avec les molécules d'eau et autres substances polaires.
Dans les cristaux T-buah, ces ponts d'hydrogène sont un facteur clé pour que les molécules restent ensemble; Bien qu'il n'y ait pas trop d'informations sur la structure cristalline de cet alcool.
Lorsque le groupe OH est si proche et entouré des groupes apolaires Cho3, Les molécules d'eau parviennent à hydrater presque tout l'alcool tout en interagissant avec OH. Cela expliquerait sa grande solubilité dans l'eau.
Propriétés
Noms chimiques
-Alcool thermique
-Teranol teranol
-2- méthyl-2-propanol
-2-méthylpropan-2-ol.
Formule moléculaire
C4HdixO o (cho3)3Coh.
Poids moléculaire
74 123 g / mol.
Description physique
Liquide solide incolore ou incolore, selon la température ambiante, car le point de fusion est de 77,9 ºF (25,4 ºC). Au-dessus de 77,9 ºF est un liquide.
Odeur
Semblable au camphre.
Point d'ébullition
82,4 ºC.
Point de fusion
77,9 ºF (25,4 ºC).
point d'allumage
52 ºF (11 ºC). COUPE FERMÉE.
Solubilité dans l'eau
Très soluble. En fait, quelles que soient les proportions, cet alcool est toujours miscible avec l'eau.
Solubilité dans les solvants organiques
Miscible avec de l'éthanol, de l'éther éthylique et soluble dans le chloroforme.
Densité
0,78 g / cm3.
Densité de vapeur
2,55 (avec relation aérienne = 1).
La pression de vapeur
4,1 kPa à 20 ºC.
Coefficient de partition octanol / eau
Log p = 0,35.
Thermostabilité
Instable en chaleur
Température d'auto-direction
896 ºF (470 ºC).
Peut vous servir: Aliquot (chimie)Décomposition
Lorsqu'il est chauffé peut libérer des vapeurs de monoxyde de carbone et d'isobutilene.
Chaleur de vaporisation
39.07 kJ / mol.
Capacité calorique
215,37 JK-1mol-1.
Enthalpie de formation
-360.04 à -358.36 Kjmol-1.
Température de stockage
2-8 ºC.
La stabilité
Il est stable, mais incompatible avec de forts agents oxydants, du cuivre, des alliages de cuivre, des métaux alcalins et en aluminium.
Potentiel d'ionisation
9,70 eV.
Seuil d'odeur
219 mg / m3 (Basse odeur).
Indice de réfraction
1 382 à 25 ° C.
Constante de dissociation
PKA = 19,20.
Concentration maximale de vapeur
5,53% à 25 ºC.
Réactions
-Il est désagréable par une base forte pour provoquer un anion alcoxyde; Plus précisément, un terbutoxyde, (ch3)3CO-.
-L'alcool thermique réagit avec le chlorure d'hydrogène pour former le chlorure terbutyl.
(Ch3)3Coh + hcl => (ch3)3CCL + H2SOIT
Les alcools tertiaires ont une plus grande réactivité avec des halogénures d'hydrogène que les alcools secondaires et primaires.
Des risques
L'alcool thermique par contact avec la peau produit des lésions légères, comme l'érythème et l'hyperémie non sérieuse. De plus, il ne traverse pas la peau. Au contraire, dans les yeux, il produit une grave irritation.
Lorsqu'il est inhalé, il produit une irritation dans le nez, la gorge et les bronches. En cas d'exposition élevée, des effets stupéfiants, un état de somnolence, ainsi que des fonds, des vaahidos et des maux de tête peuvent se produire.
Cet alcool est un agent tératogène expérimental, il a donc été observé chez les animaux qui peuvent influencer l'apparition de troubles congénitaux.
En ce qui concerne son stockage, son liquide et ses vapeurs sont inflammables, et donc dans certaines circonstances, il peut générer des incendies et des explosions.
L'OSHA a établi une limite de concentration de 100 ppm (300 mg / m3) Pour un jour de 8 heures.
Peut vous servir: pourcentage de solutionsApplications
-L'alcool thermique est utilisé pour l'incorporation du groupe thermique dans des composés organiques, afin de préparer les huiles solubles dans les huiles et le trinitro-tter-butletoluène, un musc artificiel. De plus, il constitue un matériau initial pour la préparation de peroxydes.
-Il a été approuvé par la FDA en tant qu'agent d'attentat à utiliser dans les composants et les matières plastiques qui sont en contact avec la nourriture. Il a été utilisé dans l'élaboration des fruits, plastiques et essences lacas.
-Il s'agit d'un intermédiaire pour la production de chlorure de terbutyl et de tributilphénol. Il agit comme un agent dénaturant de l'éthanol.
-Servir pour la fabrication d'agents de flottaison, comme solvant organique pour éliminer les peintures et pour dissoudre les essences utilisées dans les parfums.
-Il est utilisé comme amplificateur d'octane dans l'essence; carburant et additif de carburant; Solvant à utiliser dans le nettoyage et comme misérable.
-L'alcool thermique est un agent intermédiaire dans la production de l'éther terbutylmétyl (MTBE) et de l'éther tributtiléthyle (ETBE), réagissant respectivement avec le méthanol et l'éthanol.
-Il agit également de la même manière dans la production d'hydroperoxyde de tributyle (TBHP) par réaction avec du peroxyde d'hydrogène.
-Il est utilisé comme réactif dans le processus connu sous le nom de Curtius REALREGLO.
Les références
- Graham Salomons t.W., Craig B. Fryhle. (2011). Chimie organique. Amines. (dixe Édition.). Wiley Plus.
- Wikipédia. (2019). Alcool tert-butyle. Récupéré de: dans.Wikipédia.org
- CommonorganicChemistry. (s.F.). T-butanol. Récupéré de: CommonorganicChemistry.com
- Centre national d'information sur la biotechnologie. (2019). Tert butanol. Base de données PubChem. Récupéré de: pubchem.NCBI.NLM.NIH.Gouvernement
- Carey F. POUR. (2008). Chimie organique. (Sixième édition). Mc Graw Hill.
- « Caractéristiques et exemples du contenu des attitudes
- Qu'est-ce que les enfants et les jeunes du 21e siècle apprennent à agir dans le monde d'aujourd'hui? »

